
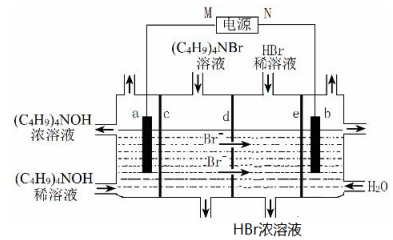
| A. | M为负极 | |
| B. | b极电极反应式:2H2O-4e-=O2↑+4H+ | |
| C. | c、e分别为阳离子交换膜和阴离子交换膜 | |
| D. | 制备 1mol(C4H9)4NOH,理论上 a极产生11.2L气体(标准状况下) |
分析 以四丁基溴化铵[(C4H9)4NBr]为原料,采用电渗析法合成(C4H9)4NOH的过程中,据溴离子的移动方向可知,a为阴极b为阳极,又据图分析,生成HBr浓溶液,说明阳极上不是溴离子放电,则e不是阴离子交换膜,是阳离子交换膜,阳极电极反应式为2H2O-4e-=O2↑+4H+,据左池产物分析,c也是阳离子交换膜,a电极为氢离子放电生成氢气,据此分析.
解答 解:A、据溴离子的移动方向可知,a为阴极b为阳极,所以M为负极,故A正确;
B、据图分析,生成HBr浓溶液,说明阳极上不是溴离子放电,阳极电极反应式为2H2O-4e-=O2↑+4H+,故B正确;
C、阳极上不是溴离子放电,则e不是阴离子交换膜,是阳离子交换膜,据左池产物分析,c也是阳离子交换膜,故C错误;
D、a电极为氢离子放电生成氢气,生成标准状况下11.2L氢气需要1mol氢离子放电,则生成1mol氢氧根离子,即 可制备1mol(C4H9)4NOH,故D正确;
故选C.
点评 本题考查了电解池的相关知识,注意根据离子的移动方向判断阴阳极是解决本题的关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | $\frac{mω}{28V}$mol•L-1 | B. | $\frac{mω}{56V}$ mol•L-1 | C. | $\frac{mω}{112V}$mol•L-1 | D. | $\frac{mω}{V}$ mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 盐酸浓度增加一倍,使用量减半 | |
| B. | 盐酸浓度增加一倍,使用量增加一倍 | |
| C. | 增加碳酸钠的用量 | |
| D. | 盐酸浓度不变,使用量减半 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol乙烷在光照条件下最多能与3 mol Cl2发生取代反应 | |
| B. | 石油裂解气能使溴的四氯化碳溶液、酸性KMnO4溶液褪色 | |
| C. | 水煤气可用来合成液态烃、甲醇等有机物 | |
| D. | 苯可通过取代反应制得硝基苯、氯苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
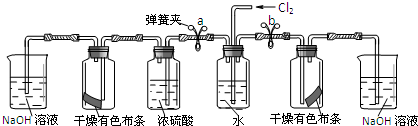
| 步骤 | 实验操作 | 预期现象和结论 |
| ① | 松开a处弹簧夹,夹上b处弹簧夹 | 装置左边集气瓶中的有色布条不褪色 删去,证明猜想一不正确. |
| ② | 松开b处弹簧夹,夹上a处弹簧夹 | 装置右边集气瓶中的有色布条褪色, 说明猜想二正确. |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com