
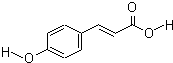
 对羟基肉桂酸是一种强效的导电材料,在液晶显示器工业中近年来研究广泛.结构简式如图:
对羟基肉桂酸是一种强效的导电材料,在液晶显示器工业中近年来研究广泛.结构简式如图:

科目:高中化学 来源: 题型:
| A、离子液体可以作为电池的电解质 |
| B、硝酸乙基铵水溶液呈碱性 |
| C、硝酸乙基铵水解的离子方程式表示为:C2H5NH3++H2O═C2H5NH2+H3O+ |
| D、相同温度下,相同物质的量浓度的硝酸乙基铵溶液和硝酸铵溶液前者的pH值小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一定条件下,2.3g金属钠与氧气完全反应失电子数为0.1NA |
| B、常温常压下,氧气和臭氧(O3)的混合物32g中含有NA个氧原子 |
| C、1molOH- 中含有的电子数为9NA |
| D、0.1mol/L硫酸铝溶液中含有硫酸根的个数为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Z与M形成的化合物中不可能含有非极性键 |
| B、对应氢化物的热稳定性:X>Y>M |
| C、单质的还原性:R>M>Y>X |
| D、X、Y、M、Z四种元素组成的离子化合物受热易分解 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1mol FeBr2中滴入含Cl2 0.1mol氯水:2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl- | ||||
| B、向氢氧化钙溶液中加入少量碳酸氢钠溶液:Ca2++HCO3-+OH-═CaCO3↓+H2O | ||||
| C、向Ca(HCO3)2溶液中滴加少量Ca(OH)2溶液:Ca2++HCO3-+OH-═CaCO3↓+H2O | ||||
D、向Ba(OH)2溶液中逐滴加入NH4HSO4溶液至刚好沉淀完全并加热溶液Ba2++2OH-+H++SO42-+NH4+
|
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

| n(CH3OH) |
| n(CO2) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com