
为探究铜与稀硝酸反应产生的气体主要是NO,某课外活动小组设计了下列实验。图中D为止水夹,F是装有一半空气的注射器,其中加热装置和固定装置均已略去。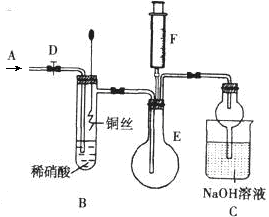
请回答有关问题:
(1)组装好装置后,关闭D,若装置的气密性良好,向外抽注射器活塞,C装置中有什么现象?
;
(2)反应开始前要向体系中通入气体A,为什么? ;A可以是 (填序号) ①N2 ②O2 ③空气 ④CO2
(3)当完成装置A的实验目的后,关闭D,再将装置B中的铜丝插入稀硝酸。B中反应的离子方程式是: 。
(4)反应一段时间后,将F中空气推入E中,证明生成了NO实验现象是: 。
(5)装置C的作用是: 。
(1)有一段水柱上升(2分)
(2)赶尽整个装置内的空气,避免对NO的检验造成干扰(2分)
①④(多选、少选、错选不给分)(2分)
(3)3Cu + 8H+ + 2NO3— = 3Cu2+ + 2NO↑ + 4H2O(2分)
(4)E中无色气体变为红棕色(2分)
(5)吸收多余的氮氧化物,防止污染空气(2分)
解析试题分析:本题为探究铜与稀硝酸反应产生的气体主要是NO的实验,明确NO容易被空气中的氧气氧化是解答本题的关键,结合实验的基本操作及氮的氧化物的性质来解答。(1)分析题给装置知,关闭D,若装置的气密性良好,向外抽注射器活塞,装置内气压降低,外界大气压把水压入C装置,C装置中有一段水柱上升;(2)反应开始前,体系中含有空气,其中的氧气能与一氧化氮反应生成二氧化氮,要向体系中通入气体A的目的是赶尽整个装置内的空气,避免对NO的检验造成干扰;A可以是 N2和CO2,选①④;(3)将装置B中的铜丝插入稀硝酸,二者反应生成硝酸铜、一氧化氮和水,反应的离子方程式是:3Cu + 8H+ + 2NO3— = 3Cu2+ + 2NO↑ + 4H2O;(4)反应一段时间后,将F中空气推入E中,NO和空气的氧气反应生成红棕色的NO2,实验现象是:E中无色气体变为红棕色;(5)NO、NO2都有毒,能污染环境,氮的氧化物能被NaOH溶液吸收,装置C的作用是:吸收多余的氮氧化物,防止污染空气。
考点:考查硝酸和氮的氧化物的性质及相关的实验基本操作。


 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:实验题
化学实验有助于理解化学知识,提升科学素养。某学习小组在实验室中用浓盐酸与MnO2共热制取Cl2并进行相关探究。
(1)已知发生装置如图所示。制备实验开始时,先检查装置气密性,接下来的操作依次是 (填序号)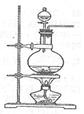
A.往烧瓶中加入MnO2粉末
B.加热
C.往烧瓶中加入浓盐酸。
(2)该小组关于实验中可制得氯气体积(标准状况)的讨论正确的是
A.若提供0.4 mol HCl,MnO2不足量,则可制得氯气2.24 L
B.若提供0.4 mol HCl,MnO2过量,则可制得氯气2.24 L
C.若有0.4 mol HCl参与反应,则可制得氯气2.24 L
D.若有0.4 mol HCl被氧化,则可制得氯气2.24 L
(3)将Cl2通入水中,所得溶液中具有氧化性的含氯粒子有________ (填微粒符号)
(4)下列收集Cl2的正确装置是________。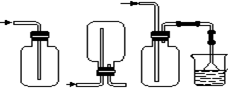
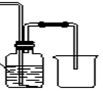
A B C D
(5)该小组利用刚吸收过少量SO2的NaOH溶液对Cl2进行尾气处理。
①请完成吸收初期的化学方程式:Cl2+Na2SO3+2 NaOH= ________________
②吸收一段时间后,某同学取出2mL吸收后的溶液(强碱性)于试管中,充分振荡后向其中滴加3~4滴淀粉-KI溶液,发现溶液先变蓝,随即又褪去。溶液先变蓝,说明吸收后的溶液中存在 (填微粒符号),用离子方程式表示蓝色褪去的可能原因: 。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某课外兴趣小组为探究铜跟浓硫酸反应情况,用下图所示装置进行实验。已知:①SO2难溶于饱和亚硫酸氢钠溶液;②SO2能与酸性高锰酸钾溶液发生氧化还原反应使之褪色(化学方程式为5SO2+2KMnO4+2H2O=K2SO4+2MnSO4+2H2SO4)。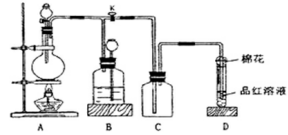
回答下列问题(注:E为止水夹,F为旋塞):
(1)检查A装置的气密性的方法 。
(2)装置A中反应的化学方程式为 。
(3)装置D中试管口放置的棉花应蘸有NaOH溶液,
其作用是 。
(4)装置B具有贮存气体的作用。当D处有明显的现象后,关闭旋塞F并移去酒精灯,由于余热的作用,A处仍有气体产生,此时B中的现象是 ,B中应放置的液体是(填字母) 。
| A.水 | B.饱和NaHSO3溶液 | C.酸性KMnO4溶液 | D.NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
现有如下仪器,仪器中已注入溶液,回答下列问题。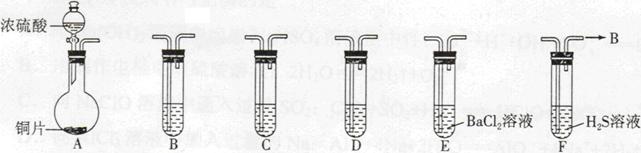
(1)加热装置A,写出铜与浓硫酸反应的化学方程式: ,烧瓶中的实验现象为 。
(2)验证碳、硅非金属性的相对强弱(已知酸性:H2SO3>H2CO3),若选择仪器A、B、C、D并相连接,则B、C、D中所选择的试剂分别为 、 、 。能说明碳的非金属性比硅强的实验现象是 。
(3)验证SO2的氧化性、还原性。若选择A、E、F仪器,并按A、E、F顺序连接。
①则证明SO2有氧化性的实验现象是 ,反应方程式为:
。
②若证明SO2具有还原性,在E中采取的实验操作为 ,其实验现象为 ,反应原理为 。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某课外活动小组欲利用CuO与NH3反应,研究NH3的某种性质并测定其组成,设计了如下实验装置(夹持装置未画出)进行实验。请回答下列问题: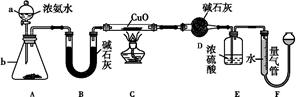
(1)仪器a的名称为 ;仪器b中可选择的试剂为 。
(2)实验室中,利用装置A,还可制取的无色气体是 (填字母)。
| A.Cl2 | B.O2 | C.CO2 | D.NO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
无水FeCl3呈棕红色,极易潮解,100℃左右时升华,工业上常用作有机合成催化剂。实验室可用下列装置(夹持仪器略去)制备并收集无水FeCl3。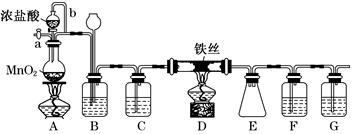
请回答:
(1)装置A中反应的离子方程式为__________________________________________。
(2)装置F中所加的试剂为_________________________________________________。
(3)导管b的作用为_____________________________________________________;
装置B的作用为________________________________________________________。
(4)实验时应先点燃A处的酒精灯,反应一会儿后,再点燃D处的酒精灯,原因为_______________________________________________________。
(5)反应结束后,拆卸装置前,必须进行的操作是_________________________________
(6)为检验所得产品中是否含有FeCl2,可进行如下实验:取E中收集的产物少许,加水溶解,向所得溶液中加入一种试剂,该试剂为________(填序号)。
①Fe粉 ②KSCN溶液 ③酸性KMnO4溶液 ④NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
氯水是实验室常需临时配制的一种试剂,图甲所示的是实验室配制氯水时的一种常用装置,图乙是某化学实验小组自行设计的一种配制氯水的装置(图中的鼓气球是一种具有气体单向阀的、可用于向瓶中鼓入空气的仪器)。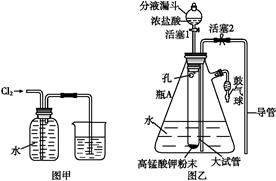
(1)氯水需临时配制的原因是: (用化学方程式表示)。
(2)图甲所示装置中,烧杯内的液体是 。
(3)图乙所示装置中,瓶A 内的大试管上端管壁钻有一个小孔,瓶A的名称叫 ,该仪器通常用于
实验中(填基本实验操作的名称)。
(4)用图乙所示装置配制氯水时,操作步骤如下:
①关闭活塞2,打开分液漏斗上口的玻璃塞,再打开活塞1,将少量浓盐酸注入大试管内。
②关闭活塞1,盖上分液漏斗上口玻璃塞。浓盐酸和大试管内的高锰酸钾粉末反应产生氯气。
③轻轻摇动瓶A,使氯气不断溶入水中。
用图乙装置能在较短时间内得到饱和氯水。除了在摇动过程中增大了气体和水的接触面以外,另一个重要原因是 。
分液漏斗中的盐酸应分数次加入试管内。若一次加入太多的盐酸,可能引起的后果是 。
(5)配制氯水完成后,不必拆卸装置即可从瓶A中取用少量氯水,方法是 。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某课外活动小组欲利用CuO与NH3反应,研究NH3的某种性质并测定其组成,设计了如下实验装置(夹持装置未画出)进行实验。请回答下列问题: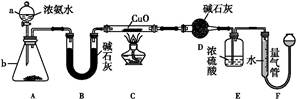
(1)仪器a的名称为 ;仪器b中可选择的试剂为 。
(2)实验室中,利用装置A,还可制取的无色气体是 (填字母)。
| A.Cl2 | B.O2 | C.CO2 | D.NO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
根据要求完成下列实验。(a、b 为弹簧夹,其他装置略去)
(一)验证酸性的相对强弱:碳酸>苯酚。(已知酸性:亚硫酸 >碳酸)
(1)铜与浓硫酸反应的化学方程式是_________________________________________,
装置A中的足量的试剂是 。
(2)连接仪器、 、加药品后,打开a关闭 b,然后滴入浓硫酸,加热。能说明碳酸的酸性比苯酚酸性强的实验现象是:____________________________。
(二)验证SO2具有氧化性、还原性和酸性氧化物的通性。
(3)打开b,关闭a。能验证SO2具有氧化性的化学方程式是_______________________。
(4)若过量的SO2通入NaOH溶液中,其化学方程式是:____________________________。
(5)BaCl2溶液中无任何现象,将其分成两份,分别滴加氨水和氯水,均产生白色沉淀,沉淀化学式分别是__________________,_________________。
(6)写出其中SO2显示还原性并生成白色沉淀的总的离子方程式___________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com