
| A、A可能是共价化合物 |
| B、A与金刚石的晶体类型相同 |
| C、A中不可能有共价键 |
| D、A溶于水中时一定破坏了A中的离子键 |


 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案科目:高中化学 来源: 题型:
| A、原电池中阳离子向负极移动 |
| B、用铝质铆钉接铁板,铁易被腐蚀 |
| C、马口铁(镀锡)表面一旦破损,铁腐蚀加快 |
| D、白铁(镀锌)表面一旦破损,铁腐蚀加快 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、阳离子被还原不一定得到金属单质 |
| B、在氧化还原反应中,非金属单质一定是氧化剂 |
| C、某元素从化合态变为游离态时.,该元素一定被还原 |
| D、在反3S+6KOH=K2SO3+2K2S+3H2O中,作还原剂和作氧化剂的硫原子个数比为2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、C2H4、CS2、H2O、CO32- |
| B、H2O2、BF3、CH3OH、ClO3- |
| C、C2H2、C6H6、CO2、SO42- |
| D、C2H6、C2F4、PH3、H3O+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、同主族元素的简单阴离子还原性越强,则对应元素的非金属性越强 |
| B、第二周期元素从左到右,最高正价从+1递增到+7 |
| C、IA族与ⅦA族元素间可形成共价化合物或离子化合物 |
| D、同周期金属元素的化合价越高,其原子失电子能力越强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、第二周期ⅠA族 |
| B、第二周期ⅡA族 |
| C、第三周期ⅠA族 |
| D、第三周期ⅡA族 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 原子 | N | S | O | Si |
| 半径 10-10m | 0.75 | 1.02 | 0.74 | 1.17 |
| A、0.08×10-10m |
| B、1.10×10-10m |
| C、1.20×10-10m |
| D、0.70×10-10m |
查看答案和解析>>
科目:高中化学 来源: 题型:
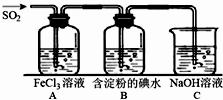
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com