
分析 (1)亚铁离子不稳定,易被空气中氧气氧化生成铁离子;
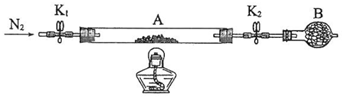
(2)①根据仪器的图形可判断仪器名称;
②实验时,为避免亚铁被氧化,应先通入氮气,冷却时注意关闭开关,防止氧气进入,冷却至室温再称量固体质量的变化;
③直至A恒重,记为m3 g,应为FeSO4和装置的质量,则m(FeSO4)=(m3-m1).m(H2O)=(m2-m3),以此计算n(H2O)、n(FeSO4),结晶水的数目等于$\frac{n({H}_{2}O)}{n(FeS{O}_{4})}$;若实验时按a、d次序操作,会导致硫酸亚铁被氧化;
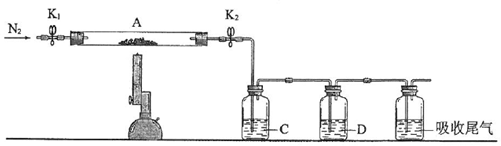
(3)硫酸亚铁高温分解可生成Fe2O3、SO3、SO2,C为氯化钡,用于检验SO3,D为品红,可用于检验SO2.
解答 解:(1)滴加KSCN溶液,溶液颜色无明显变化,可知硫酸亚铁与KSCN不反应,但亚铁离子不稳定,易被空气中氧气氧化生成铁离子,最终溶液变红色,
故答案为:硫酸亚铁与KSCN不反应;硫酸亚铁易被空气氧化为硫酸铁;
(2)①由仪器的图形可知B为干燥管,故答案为:干燥管;
②实验时,为避免亚铁被氧化,应先通入氮气,冷却时注意关闭开关,防止氧气进入,冷却至室温再称量固体质量的变化,则正确的顺序为dabcfe,
故答案为:dabcfe;
③直至A恒重,记为m3 g,应为FeSO4和装置的质量,则m(FeSO4)=(m3-m1),m(H2O)=(m2-m3),则n(H2O)=$\frac{{m}_{2}-{m}_{3}}{18}$、n(FeSO4)=$\frac{{m}_{3}-{m}_{1}}{152}$,结晶水的数目等于$\frac{n({H}_{2}O)}{n(FeS{O}_{4})}$=$\frac{76({m}_{2}{-}_{\;}{m}_{3})}{9({m}_{3}-{m}_{1})}$,
若实验时按a、d次序操作,会导致硫酸亚铁被氧化,则导致固体质量偏大,测定结果偏小,
故答案为:$\frac{76({m}_{2}{-}_{\;}{m}_{3})}{9({m}_{3}-{m}_{1})}$;偏小;
(3)①实验后反应管中残留固体为红色粉末,说明生成Fe2O3,则反应中Fe元素化合价升高,S元素化合价应降低,则一定生成SO2,可知硫酸亚铁高温分解可生成Fe2O3、SO3、SO2,C为氯化钡,用于检验SO3,可观察到产生白色沉淀,D为品红,可用于检验SO2,品红褪色,
故答案为:c、a;产生白色沉淀、品红褪色;
②硫酸亚铁高温分解可生成Fe2O3、SO3、SO2,方程式为2FeSO4$\frac{\underline{\;高温\;}}{\;}$Fe2O3+SO2↑+SO3↑,故答案为:2FeSO4$\frac{\underline{\;高温\;}}{\;}$Fe2O3+SO2↑+SO3↑.
点评 本题为2017年广西试题,以绿矾为载体,考查结晶水合物中结晶水数目的测定以及分解产物的鉴别,侧重考查学生的分析能力、实验能力和计算能力,注意把握实验原理、实验技能以及物质性质的分析,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | H+、S2O32-、SO42-、Na+ 能大量共存于同一溶液中 | |
| B. | 常温下,$\frac{c({H}^{+})}{c(O{H}^{-})}$=1×10-12的溶液:Ba2+、Na+、ClO-、NO3-能大量共存 | |
| C. | 在含1mol FeI2的溶液中,通入1mol Cl2发生的离子反应为:2Fe2++2I-+2Cl2═2Fe3++4Cl-+I2 | |
| D. | 在NH4HSO4溶液中滴加少量Ba(OH)2溶液:NH4++H++SO42-+Ba2++2OH-═BaSO4↓+NH3•H2O+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在标准状况下,VL气态烯烃(CnH2n)含碳碳双键的数目为$\frac{V}{22.4}$ NA | |
| B. | 在8.4 g NaHCO3晶体中,所含离子数目为0.3NA | |
| C. | 5.6g铁粉与稀硝酸反应,转移的电子数是0.3 NA | |
| D. | 在沸水中滴加含0.1 molFe3+的FeCl3饱和溶液,得到的Fe(OH)3胶粒数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ”,tián),Ts的原子核外最外层电子数是7,下列说法不正确的是( )
”,tián),Ts的原子核外最外层电子数是7,下列说法不正确的是( )| A. | Ts是第七周期第ⅦA族元素 | |
| B. | Ts的同位素原子具有相同的电子数 | |
| C. | Ts在同族元素中非金属性最弱 | |
| D. | 中子数为176的Ts核素符号是${\;}_{117}^{176}$Ts |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

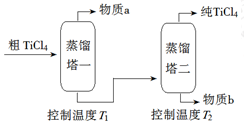
| 化合物 | SiCl4 | TiCl4 | AlCl3 | FeCl3 | MgCl2 |
| 沸点/℃ | 58 | 136 | 181(升华) | 316 | 1412 |
| 熔点/℃ | -69 | 25 | 193 | 304 | 714 |
| 在TiCl4中的溶解性 | 互溶 | - | 微溶 | 难溶 | |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用石灰、碳酸钠等碱性物质处理废水中的酸 | |
| B. | 用可溶性的铝盐和铁盐处理水中的悬浮物 | |
| C. | 用氯气处理水中的Cu2+、Hg2+等重金属离子 | |
| D. | 用烧碱处理含高浓度NH4+的废水并回收利用氨 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
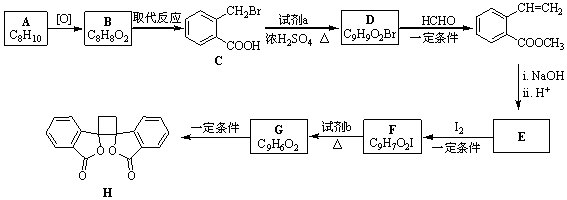
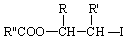
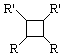
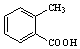 .
.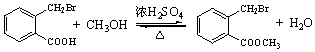 .
. ;此反应同时生成另外一个有机副产物且与F互为同分异构体,此有机副产物的结构简式是
;此反应同时生成另外一个有机副产物且与F互为同分异构体,此有机副产物的结构简式是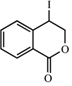 .
.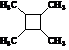 路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件).
路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
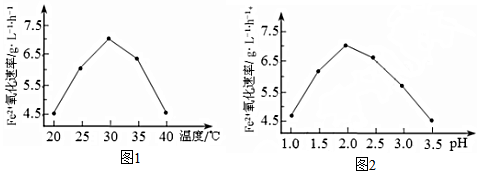
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com