
|
25℃,a L 0.1000 mol/L CH3COOH溶液与b L 0.1000 mol/L NaOH溶液混合,下列说法正确的是 | |
A. |
若a>b,则pH一定小于7 |
B. |
若a<b,则一定存在:n(OH-)-n(H+)>0.1(b-a) |
C. |
c(Na+)>c(CH3COO-)>c(OH-)>c(H+),则a≤b |
D. |
若pH=7,则a>b,且c(Na+)=c(CH3COO-)+c(CH3COOH) |
 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:四川省广元中学2010届高三第四次月考、化学试卷 题型:013
|
设NA为阿伏加德罗常数,下列说法不正确的是 | |
| [ ] | |
A. |
含12.0 g NaHSO4晶体中阳离子数约为0.2×6.02×1023 |
B. |
在H2O2+Cl2=2HCl+O2反应中,每生成32 g氧气,则转移2NA个电子 |
C. |
常温常压下,氧气和臭氧的混合物16 g中约含有6.02×1023个氧原子 |
D. |
一定温度下,1 L 0.50 mol·L-1 NH4Cl与2 L 0.25 mol·L-1 NH4Cl两种溶液含n(NH+4)不同 |
查看答案和解析>>
科目:高中化学 来源:浙江省杭州外国语学校2011届高三11月月考化学试题 题型:022
| |||||||||||||||||||||||||||||||||
查看答案和解析>>
科目:高中化学 来源:天利38套《2008全国各省市高考模拟试题汇编(大纲版)》、化学 大纲版 题型:022
水的电离平衡曲线如下图所示:
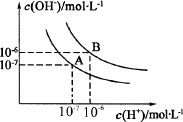
(1)若以A点表示25℃时水电离平衡时离子的浓度,当温度升高到100℃时,水的电离平衡状态变到B点,则此时水的离子积从________变到________,造成水的离子积变化的原因是________.
(2)已知25℃时,0.1 L 0.1 mol·L-1的NaA溶液的pH=10,则NaA溶液中所存在的离子的物质的量浓度由大到小的顺序为________.
(3)25℃时,将pH=11的NaOH溶液与pH=4的硫酸溶液混合,若所得混合溶液pH=9,则NaOH溶液与硫酸溶液的体积比为________.
(4)100℃时,若10体积的某强酸溶液与1体积的某强碱溶液混合后溶液呈中性,则混合之前,该强酸的pH与强碱的pH之间应满足的关系是________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com