
| A. | 盐酸 | B. | 硝酸 | C. | 氢氧化钠溶液 | D. | 浓硫酸 |
分析 A.Mg和Al都属于较活泼金属,都能和稀盐酸、稀硫酸反应生成氢气;
B.Mg和Al与稀硝酸混合生成氮的化合物而不是氢气;
C.只有Al能和NaOH溶液反应而Mg不反应;
D.常温下Al和浓硫酸发生钝化现象,且镁和浓硫酸反应生成二氧化硫.
解答 解:A.Mg和Al都属于较活泼金属,都能和稀盐酸、稀硫酸反应生成氢气;
B.稀硝酸具有强氧化性,能金属单质反应生成氮的化合物而不是氢气,所以Mg和Al与稀硝酸混合生成氮的化合物而不是氢气,产生氢气的量为0;
C.只有Al能和NaOH溶液反应生成偏铝酸钠和氢气,而Mg不反应,所以反应产生氢气的量小于A;
D.常温下Al和浓硫酸发生钝化现象,且镁和浓硫酸反应生成二氧化硫而不是氢气;
通过以上分析知,生成氢气量最多的是稀盐酸,
故选A.
点评 本题考查元素化合物知识,侧重考查硝酸、浓硫酸及铝的性质,明确硝酸和浓硫酸的强氧化性及铝的特殊性即可解答,易错选项是B.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
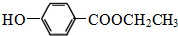
 .
.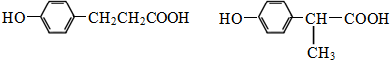 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ①③④ | C. | ②③④ | D. | ①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石油常压蒸馏得到的汽油属于纯净物 | |
| B. | 石油减压蒸馏、煤的液化和气化都是化学变化 | |
| C. | 石油催化裂化的目的是获得更多甲烷 | |
| D. | 石油催化裂化的产物能使溴水和酸性KMnO4溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
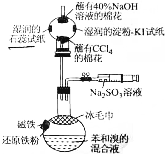 溴苯是一种化工原料,某课外小组用如图装置改进了苯的溴代反应.
溴苯是一种化工原料,某课外小组用如图装置改进了苯的溴代反应. ,冰毛巾覆盖在圆底烧瓶上半部分的目的是降低温度圆底烧瓶上部温度,起冷却回流作用;
,冰毛巾覆盖在圆底烧瓶上半部分的目的是降低温度圆底烧瓶上部温度,起冷却回流作用;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯水中只含Cl2和HClO两种分子 | |
| B. | 新制氯水只能使蓝色石蕊试纸变红 | |
| C. | 光照氯水有气泡逸出,该气体主要是Cl2 | |
| D. | 氯水放置数天后其pH将变小,酸性增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com