
【题目】苯酚是一种重要的化工原料。以苯酚为主要起始原料,经下列反应可制得香料M和高分子化合物N。(部分产物及反应条件已略去)
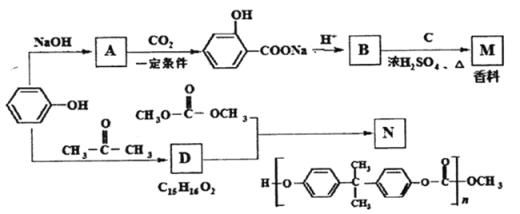
(1)B的官能团名称___。苯酚与浓溴水反应生成白色沉淀,可用于苯酚的定性检验和定量测定,反应的化学方程式为____。
(2)已知C的分子式为C5H12O,C能与金属Na反应,C分子中有3种不同化学环境的氢原子,则M的结构简式为___。
(3)生成N的反应的化学方程式___,反应类型为_____。
(4)以苯酚为基础原料也可以合成防腐剂F.已知F的相对分子质量为152,其中氧元素的质量分数为31.58%,F完全燃烧只生成CO2和H2O2。则F的分子式是____。
【答案】羧基、羟基 ![]() +3Br2
+3Br2 +3HBr
+3HBr  n
n![]() +n
+n![]()
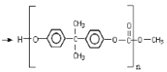 +(2n-1)CH3OH 缩聚反应 C8H8O3
+(2n-1)CH3OH 缩聚反应 C8H8O3
【解析】
苯酚与氢氧化钠反应生成苯酚钠,故A为![]() ,由转化关系可以知道B为
,由转化关系可以知道B为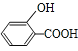 ,C的分子式为C5H12O,C能与金属Na反应,属于饱和一元醇,C分子中有3中不同化学环境的氢原子,故C的结构简式是
,C的分子式为C5H12O,C能与金属Na反应,属于饱和一元醇,C分子中有3中不同化学环境的氢原子,故C的结构简式是 ,B与C发生酯化反应生成M,M为
,B与C发生酯化反应生成M,M为 ,苯酚与丙酮反应生成D,D的分子式为C15H16O2,再结合N的结构可以知道D为
,苯酚与丙酮反应生成D,D的分子式为C15H16O2,再结合N的结构可以知道D为 ;
;
(1)根据上述分析可以知道,B的结构简式为 ,其含有的官能团为羧基、醛基;苯酚与浓溴水反应生成三溴苯酚和溴化氢,反应的方程式为:
,其含有的官能团为羧基、醛基;苯酚与浓溴水反应生成三溴苯酚和溴化氢,反应的方程式为: ,
,
答案为:羧基、醛基;  ;
;
(2)根据分析可以知道,M的结构简式为: ,
,
答案为: ;
;
(3)生成N的反应方程式为: ,该反应属于缩聚反应,
,该反应属于缩聚反应,
答案为:n![]() +n
+n![]()
 +(2n-1)CH3OH ;缩聚反应
+(2n-1)CH3OH ;缩聚反应
(4)以苯酚为基础原料也可以合成防腐剂F。经质谱分析F的相对分子质量为152,其中氧元素的质量分数为31%,则分子中氧原子数目为![]() =3,而F完全燃烧只生成二氧化碳和水,则只含有C、H、O三种元素,去掉3个氧原子剩余式量为152-48=14,分子中最大碳原子数目为
=3,而F完全燃烧只生成二氧化碳和水,则只含有C、H、O三种元素,去掉3个氧原子剩余式量为152-48=14,分子中最大碳原子数目为![]() =8.8,故F的分子式为C8H8O3;
=8.8,故F的分子式为C8H8O3;
答案为:C8H8O3;


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】明矾石是制取钾肥和氢氧化铝的重要原料,明矾石的组成和明矾相似,此外还含有氧化铝和少量氧化铁杂质。具体实验步骤如下图所示(明矾石焙烧后成分不变):
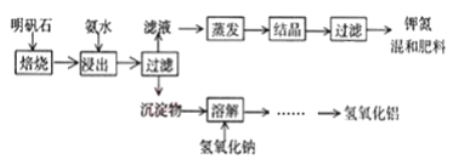
完成下列填空:
(1)“浸出”反应的离子方程式为_______。“浸出”所用稀氨水浓度为39.20g/L,配制500mL该氨水需251.28g/L的浓氨水________mL。
(2)“过滤”所需的玻璃仪器有______________。
(3)写出“溶解”过程中发生反应的化学方程式_________、________。
(4)检验滤液中是否含有SO42-的实验方法__________。
(5)为测定钾氨复合肥K2SO4、(NH4)2SO4中SO42-的质量分数,设计实验步骤如下:
①_____________________。
②溶于水,加入足量BaCl2溶液,待白色沉淀不再产生为止。
③过滤、______、________(依次填写实验操作名称)。
④冷却、称量所得沉淀的质量。
(6)若所取试样和所得沉淀的质量分别为mg、ng,试用含有m、n的代数式表示该钾氮复合肥中SO42-的质量分数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 是大气污染物,造成酸雨的主要原因,用如图所示装置可以既吸收工厂排放的废气中的
是大气污染物,造成酸雨的主要原因,用如图所示装置可以既吸收工厂排放的废气中的![]() ,又可以生成一定量的硫酸,下列说法不正确的是( )
,又可以生成一定量的硫酸,下列说法不正确的是( )

A.a为负极,b为正极
B.从左下口流出的硫酸的质量分数一定大于50%
C.生产过程中氢离子由左移向右
D.负极反应式为SO2+2H2O-2e-=SO42—+4H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向水槽中滴入浓![]() 溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验中,不考虑两球的浮力变化)( )
溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验中,不考虑两球的浮力变化)( )

A.杠杆为导体或绝缘体时,均为A端高B端低
B.杠杆为导体或绝缘体时,均为A端低B端高
C.当杠杆为导体时,A端高B端低;杠杆为绝缘体时,A端低B端高
D.当杠杆为导体时,A端低B端高;杠杆为绝缘体时,A端高B端低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以铝土矿(主要成分为![]() ,含少量
,含少量![]() 和
和![]() 等杂质)为原料生产铝和氮化铝的一种工艺流程如图[已知:
等杂质)为原料生产铝和氮化铝的一种工艺流程如图[已知:![]() 在“碱溶”时转化为铝硅酸钠(
在“碱溶”时转化为铝硅酸钠(![]() )沉淀]。
)沉淀]。

(1)用氧化物的形式表示铝硅酸钠的化学式____。
(2)溶液a中加入![]() 后,生成沉淀的离子方程式为___。
后,生成沉淀的离子方程式为___。
(3)有人考虑用熔融态![]() 电解制备铝,你觉得是否可行?请说明理由:___。
电解制备铝,你觉得是否可行?请说明理由:___。
(4)取一定量的氮化铝样品,用以下装置测定样品中AlN的纯度(夹持装置已略去)。打开![]() ,加入NaOH浓溶液,至不再产生
,加入NaOH浓溶液,至不再产生![]() 。打开
。打开![]() ,通入
,通入![]() 一段时间。
一段时间。

①写出AlN与NaOH溶液反应的化学方程式______。
②实验中需要测定的数据是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,将仪器A中的浓盐酸滴加到盛有MnO2的烧瓶中,加热后产生的气体依次通过装置B和C,然后再通过加热的石英玻璃管D(放置有铁粉)。请回答:
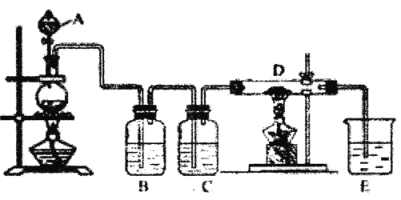
(1)仪器A的名称是_____,烧瓶中反应的化学方程式是______。
(2)装置B中盛放的液体是____,气体通过装置B的目的是_____。
(3)装置C中盛放的液体是____,气体通过装置C的目的是_____。
(4)D中反应的化学方程式是____。
(5)烧杯E中盛放的液体是___,反应的离子方程式是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A.1 mol H2 的体积是 22.4 L
B.O2 的摩尔质量是 48 g
C.标准状况下,22.4 L H2O 含有 6.02×1023 个 H2O
D.常温常压下,28g N2 与标准状况下 22.4 L CO2 含有相同的分子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用表示阿伏加德罗常数的值,下列叙述不正确的是
A.4.6gNa与含0.1molHCl的稀盐酸充分反应,转移电子数目为0.2![]()
B.25℃时,1L![]() 的
的![]() 溶液中由水电离的的数目为
溶液中由水电离的的数目为![]()
C.常温常压下,![]() 和
和![]() 混合气体所含的原子数为
混合气体所含的原子数为![]()
D.500℃时,![]() 和
和![]() 在密闭容器中充分反应后生成
在密闭容器中充分反应后生成![]() 的分子数为
的分子数为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科研人员以Zn和尖晶石型锰酸锌(ZnMn2O4)为电极材料,研制出一种水系锌离子电池。该电池的总反应方程式:xZn + Zn1xMn2O4![]() ZnMn2O4(0 < x < 1)。下列说法正确的是
ZnMn2O4(0 < x < 1)。下列说法正确的是
A. 充电时,Zn2+向ZnMn2O4电极迁移
B. 充电时,阳极反应:ZnMn2O4 2xe—=Zn1-xMn2O4+xZn2+
C. 放电时,每转移1mol e-,ZnMn2O4电极质量增加65g
D. 充放电过程中,只有Zn元素的化合价发生变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com