
 NO3溶液检验滤液中含有Cl-,此过程所发生的反应类型不包含 ( )
NO3溶液检验滤液中含有Cl-,此过程所发生的反应类型不包含 ( )| A.化合反应 | B.分解反应 | C.复分解反应 | D.氧化还原反应 |
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源:不详 题型:单选题
| A.MnO2+4HCl(浓)△ MnCl2+Cl2↑+2H2O |
| B.HCl+AgNO3= AgCl↓+HNO3 |
| C.Zn+2HCl =ZnCl2+H2↑ |
| D.2HCl 电解 H2↑+Cl2↑ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 原性HSO3->I-,氧化性IO3-> I2 > SO42-。
原性HSO3->I-,氧化性IO3-> I2 > SO42-。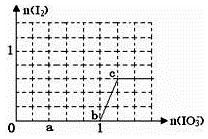
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.2.4 g/L | B.8 g/L | C.6 g/L | D.12 g/L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 ,还原剂是 ,氧化产物是 ,还原产物是 ,假如有2.5 molCl2生成,则该反应中电子转移数目为___________________。
,还原剂是 ,氧化产物是 ,还原产物是 ,假如有2.5 molCl2生成,则该反应中电子转移数目为___________________。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 3Fe+4CO2的反应中, 是氧化剂, 是还原剂, 元素被氧化, 元素被还原。
3Fe+4CO2的反应中, 是氧化剂, 是还原剂, 元素被氧化, 元素被还原。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 (4)测定血钙的含量的方法是:取2mL血液用蒸馏水稀释后,向其中加入足量(NH4)2C2O4溶液,反应生成CaC2O4沉淀,将沉淀用稀硫酸溶解得到H2C2O4后,再用KMnO4溶液滴定。
(4)测定血钙的含量的方法是:取2mL血液用蒸馏水稀释后,向其中加入足量(NH4)2C2O4溶液,反应生成CaC2O4沉淀,将沉淀用稀硫酸溶解得到H2C2O4后,再用KMnO4溶液滴定。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.FeO42-是还原产物 | B.ClO-是还原剂 |
| C.1molFe(OH)3得到3mol电子 | D.配平后OH- 的化学计量数为4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com