
某研究小组想研究碳与浓硝酸的反应。其实验过程如下。
| 操作 | 现象 |
|
| |
| b.把小块烧红的木炭迅速伸入热的浓硝酸中。 | 红热的木炭与热的浓硝酸接触发生剧烈反应,同时有大量红棕色气体产生,液面上木炭迅速燃烧,发出光亮。 |
(1)热的浓硝酸与红热的木炭接触会发生多个化学反应。
① 碳与浓硝酸的反应,说明浓硝酸具有 性。
② 反应产生的热量会使少量浓硝酸受热分解,产生红棕色气体、一种无色无味的单质气体X和水,气体X的化学式是 。
(2)实验现象中液面上木炭迅速燃烧,发出光亮。同学甲认为可能是木炭与气体X反应产生的现象;同学乙猜测NO2可能具有助燃性,木炭能在NO2中燃烧。他们设计了以下实验。
Ⅰ.制取NO2气体。
① 在虚线框内画出用铜与浓硝酸制取和收集NO2的装置简图(夹持仪器略)。
 |
② NaOH溶液的作用是吸收多余的NO2,该反应生成两种物质的量相等的正盐,写出反应的化学方程式 。
Ⅱ.探究实验。
实验操作:在空气中引燃木炭,使其燃烧并带有火焰,将带火焰的木炭伸入盛有NO2气体的集气瓶中。
实验现象:木炭在NO2气体中持续燃烧,火焰迅速变亮,集气瓶中气体颜色变浅直至无色,产生的气体能使澄清石灰水变浑浊,且遇空气不变色。
① 根据实验现象写出碳与NO2气体反应的化学方程式 。
② 试分析是否需要增加带火焰的木炭与纯净的X气体反应的实验 。
③ 通过实验探究,你认为甲、乙同学的预测是否合理,请简述理由 。
答案:(15分,画图3分,其他每空2分)
(1)① 强氧化性 ② O2
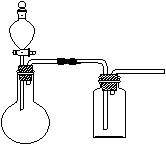 (2)Ⅰ①
(2)Ⅰ①
两处导气管进出长短对各1分,漏斗对1分)
② 2NO2 + 2NaOH  NaNO2 + NaNO3 + H2O(物质1分,配平1分)
NaNO2 + NaNO3 + H2O(物质1分,配平1分)
Ⅱ① 2NO2 + 2C 点燃 N2 + 2CO2(物质1分,配平1分)
② 当木炭燃烧时,体系中氧气浓度低于空气中氧气浓度,所以不用补充木炭在纯氧
中燃烧的实验。(按要求给分)
③ 主要是和NO2的燃烧反应,也会发生与氧气的燃烧反应,因为两种气体均存在。(按要求给分)
解析:(1)碳与浓硝酸的反应可联系实验现象,推测得到的是CO2、NO2、H2O,此过程中,浓硝酸体现出强氧化性。反应过程中浓硝酸受热分解:4HNO3 4NO2↑+O2↑+2H2O。
4NO2↑+O2↑+2H2O。
(2)实验室制取NO2可用Cu与浓硝酸反应,需固液不加热反应装置,又NO2密度比空气的大,且易与水反应,需用长进短出的向上排空气法收集;NO2有毒,多余的NO2可用NaOH溶液吸收,依题意发生反应:2NO2 + 2NaOH  NaNO2 + NaNO3 + H2O。
NaNO2 + NaNO3 + H2O。
Ⅱ.上述实验所得的气体中氧气浓度低于空气中氧气浓度,木炭在NO2气体中持续燃烧,火焰迅速变亮,说明NO2支持燃烧,不需要做木炭在纯氧中燃烧的对比试验。木炭被氧化,得到能使澄清石灰水变浑浊的CO2,NO2体现氧化性,N元素化合价降低,产生的气体遇空气不变色,可推测为N2,方程式为:2NO2 + 2C 点燃 N2 + 2CO2 。由题中实验可知,所得气体主要是NO2,也有O2,在此条件下,甲、乙同学的预测都有可能。


科目:高中化学 来源: 题型:
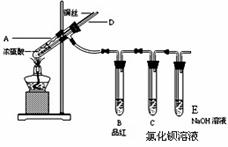 某实验小组同学为了探究铜与浓硫酸的反应,进行如下实验。
某实验小组同学为了探究铜与浓硫酸的反应,进行如下实验。
实验1:铜与浓硫酸反应,实验装置如图所示。
实验步骤:
①先连接好装置,检验气密性,加入试剂;
②加热A试管直到B中品红褪色,熄灭酒精灯;
③将Cu丝上提离开液面;
(1)能够证明铜与浓硫酸反应产生的气体的现象: 。
(2)在盛有氯化钡溶液的C试管中除了导管口有气泡外,无其他明显现象,若将其分为两份,分别滴加下列溶液,将产生沉淀的化学式填入下表相应位置。
| 滴加的溶液 | 氯水 | 氨水 |
| 沉淀的化学式 | __________________________ | __________________________ |
写出其中SO2显示还原性的离子方程式: 。
(3)熄灭酒精灯后,因为有导管D的存在,B中的液体不会倒吸,
其原因是: 。
(4)将SO2气体通入含有n mol Na2S溶液中,溶液中出现黄色浑浊,试分析该溶液最多能吸收SO2气体 mol。 (不考虑溶解的SO2)。
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,A是可用来对自来水进行消毒的黄绿色单质气体,A、B、C、D、E都含X元素,其转化关系如图所示。
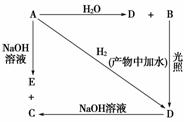
(1)请分别写出A、B、C、D、E的化学式(如为溶液请填溶质的化学式):
A________、B________、C________、D__________________________、
E________。
(2)写出下列反应的化学方程式:
A+H2O______________________________________________________;
A+NaOH___________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
四种短周期元素在周期表中的位置如图,其中只有M为金属元素。下列说法正确的是
A.原子半径Z > Y
B.X 的最简单气态氢化物的热稳定性比Z的小
C.Y的最高价氧化物对应水化物的酸性比X 的弱
D.M的最高价氧化物对应水化物不能与NaOH溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各项的叙述中都包含两个数值,前一数值大于后一数值的是
A.HCl中H—Cl键的极性和HF中H—F的极性
B.乙烯CH2=CH2中碳碳σ键的键能和碳碳π键的键能
C.1mol金刚石晶体中C-C键数目和1mol SiO2晶体Si—O键数目
D.MgCl2晶体的熔点与AlCl3晶体的熔点
查看答案和解析>>
科目:高中化学 来源: 题型:
“绿色化学”是指从技术、经济上设计可行的化学反应,尽可能减少对环境的负作用。下列化学反应,不符合绿色化学概念的是 ( )
A.消除硫酸厂尾气排放:SO2+2NH3+H2O==(NH4)2SO3
B.消除制硝酸工业尾气的氮氧化物污染:NO2+NO+2NaOH==2NaNO2+H2O
C.制CuSO4:2Cu+O2==2CuO,CuO+H2SO4==CuSO4+H2O
D.制Cu(NO3)2:Cu+4HNO3(浓)== Cu(NO3)2+2NO2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
已知H2(g)+Br2(l)=2HBr(g) △H= -72kJ·mol-1,蒸发1mol Br2(l)需要吸收的能量为30kJ,断裂1mol气态 H2、 Br2、HBr分子内的化学键分别需要吸收的能量为436kJ、akJ、369kJ,则数据a为
A.404 B.260 C.230 D.200
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com