
(12分)(1)图A是某短周期元素M的部分电离能变化情况。M元素位于周期表的第 族。
 (2)图B是部分同主族元素氢化物沸点的变化规律图像。两位同学对某主族元素氢化物沸点的变化趋势画出了两条折线a和b,正确的是 (填“a”或“b”),理由 。
(2)图B是部分同主族元素氢化物沸点的变化规律图像。两位同学对某主族元素氢化物沸点的变化趋势画出了两条折线a和b,正确的是 (填“a”或“b”),理由 。
A B
(3)甲、乙两种氢化物分子中,中心原子的轨道杂化方式相同,但甲、乙两分子的立体结构不同,原因是 。
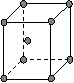
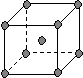
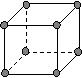 (4)下图是常见金属晶体的四种堆积模型:
(4)下图是常见金属晶体的四种堆积模型:

A B C D
(简单立方) (体心立方) (ABAB型) (ABCABC型)
请判断下列四种金属晶体分别对应的堆积模型:(填序号)
Po K Mg Cu
 特高级教师点拨系列答案
特高级教师点拨系列答案科目:高中化学 来源: 题型:
(12分)有三种金属单质A、B、C,其中A的焰色反应为黄色,B、C是常见金属。三种金属单质A、B、C能与气体甲、乙、丙及物质D、E、F、G、H之间发生如下转化关系(图中有些反应的产物和反应的条件没有标出)。
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:
A_____________;H ______________; G___________;乙____________。
(2)写出下列反应的化学方程式:
反应①___________________________________________________________;
反应②___________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(12分)有三种金属单质A、B、C,其中A的焰色反应为黄色,B、C是常见金属。三种金属单质A、B、C能与气体甲、乙、丙及物质D、E、F、G、H之间发生如下转化关系(图中有些反应的产物和反应的条件没有全部标出)
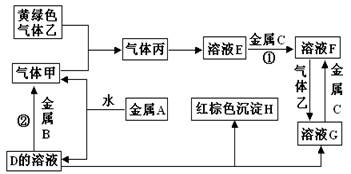
请根据以上信息回答下列问题
(1)写出下列物质的化学式:
A__________________;B_______________; G_____________;乙______________;
(2)写出下列反应的化学方程式
反应①_________________________________________________________________
反应②_________________________________________________________________
查看答案和解析>>
科目:高中化学 来源:2011-2012学年四川省南山中学高一5月月考化学试卷(带解析) 题型:填空题
(本题共12分)(1)现有A、B、C、D、E五种元素,A的原子核中没有中子;B、C元素处于同一周期,C的原子半径较小,B、C的质子数之和为27,质子数之差为5;54 g D的单质跟足量盐酸反应,生成D3+和67.2 L(标准状况)氢气;E和C能形成E2C型离子化合物,且E、C两元素的简单离子具有相同电子层结构。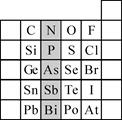
①B、D的最高价氧化物对应水化物相互反应的离子方程式为: 。
②用电子式表示C与E形成E2C的过程: 。
(2)元素在周期表中的位置,反映了元素的原子结构和元素的性质。右图是元素周期表的一部分。
①阴影部分元素N在元素周期表中的位置为 。
②在一定条件下,S与H2反应有一定限度(可理解为反应进行的程度),请判断:在相同条件下Se与H2反应的限度比S与H2反应限度 。(选填“更大”、“更小”或“相同”)
③Br2具有较强的氧化性,SO2具有较强的还原性,将SO2气体通入溴水后,反应离子方程式是__________________________________________。
④下列说法正确的是
A.C、N、O、F的原子半径随着原子序数的增大而减小
B.Si、P、S、Cl元素的非金属性随着核电荷数的增加而增强
C.干冰升华、液态水转变为气态都要克服分子内的共价键
D.HF、HCl、HBr、HI的热稳定性依次减弱
查看答案和解析>>
科目:高中化学 来源:2014届四川省高一5月月考化学试卷(解析版) 题型:填空题
(本题共12分)(1)现有A、B、C、D、E五种元素,A的原子核中没有中子;B、C元素处于同一周期,C的原子半径较小,B、C的质子数之和为27,质子数之差为5;54 g D的单质跟足量盐酸反应,生成D3+和67.2 L(标准状况)氢气;E和C能形成E2C型离子化合物,且E、C两元素的简单离子具有相同电子层结构。
①B、D的最高价氧化物对应水化物相互反应的离子方程式为: 。
②用电子式表示C与E形成E2C的过程: 。
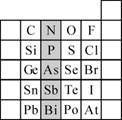
(2)元素在周期表中的位置,反映了元素的原子结构和元素的性质。右图是元素周期表的一部分。
①阴影部分元素N在元素周期表中的位置为 。
②在一定条件下,S与H2反应有一定限度(可理解为反应进行的程度),请判断:在相同条件下Se与H2反应的限度比S与H2反应限度 。(选填“更大”、“更小”或“相同”)
③Br2具有较强的氧化性,SO2具有较强的还原性,将SO2气体通入溴水后,反应离子方程式是__________________________________________。
④下列说法正确的是
A.C、N、O、F的原子半径随着原子序数的增大而减小
B.Si、P、S、Cl元素的非金属性随着核电荷数的增加而增强
C.干冰升华、液态水转变为气态都要克服分子内的共价键
D.HF、HCl、HBr、HI的热稳定性依次减弱
查看答案和解析>>
科目:高中化学 来源:2013届江苏省淮安五校高一上学期期末考试化学试卷 题型:填空题
(12分)有三种金属单质A、B、C,其中A的焰色反应为黄色,B、C是常见金属。三种金属单质A、B、C能与气体甲、乙、丙及物质D、E、F、G、H之间发生如下转化关系(图中有些反应的产物和反应的条件没有全部标出)
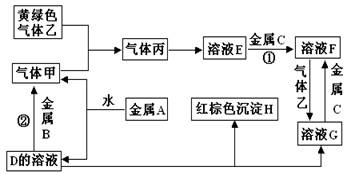
请根据以上信息回答下列问题
(1)写出下列物质的化学式:
A__________________;B_______________; G_____________;乙______________;
(2)写出下列反应的化学方程式
反应①_________________________________________________________________
反应②_________________________________________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com