
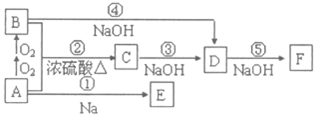
分析 F是生活中常见的气体燃料,也是含氢百分含量最高的有机物,则F为CH4,又D在氢氧化钠中反应生成F,则D为CH3COONa,B与NaOH反应生成D,则B为CH3COOH,又A通过两步氧化生成B,所以A为CH3CH2OH,A与Na反应生成E,则E为CH3CH2ONa,A与B在浓硫酸加热条件下发生酯化反应生成C为CH3COOCH2CH3,C在氢氧化钠条件下发生水解生成D,据此分析解答.
解答 解:(1)根据以上分析,A为CH3CH2OH,官能团的名称是羟基,故答案为:羟基;
(2)反应①为A与Na反应生成E,化学方程式为:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑,故答案为:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑;
(3)F为CH4,与氯气反应生成一元取代物的化学方程式为:CH4+Cl2 $\stackrel{光照}{→}$CH3Cl+HCl,故答案为:CH4+Cl2 $\stackrel{光照}{→}$CH3Cl+HCl;
(4)A.反应③为C在氢氧化钠条件下发生水解生成D,④为乙酸与NaOH发生中和反应,⑤为CH3COONa在氢氧化钠中反应生成CH4,所以3个反应中④⑤NaOH不起催化作用,故错误;
B.反应⑤为CH3COONa在氢氧化钠中反应生成碳酸钠和CH4,不属于加成反应,故错误;
C.A为CH3CH2OH,A的同分异构体为CH3OCH3,不能与金属钠反应生成氢气,故正确;
D.B为CH3COOH,C为CH3COOCH2CH3,所以1molB、1molC完全反应消耗NaOH的物质的量相同,故正确;
故选:CD.
点评 本题考查有机物推断,需要学生对给予的信息进行利用,确定F的结构是关键,再结合转化关系进行推断,需要学生熟练掌握官能团的性质与转化,难度中等.


科目:高中化学 来源: 题型:选择题
| 选项 | 化学性质 | 实际应用 |
| A | 碳元素的非金属性比硅强 | 石英和碳粉的混合物高温下反应制备粗硅 |
| B | 乙醇能使蛋白质变性 | 无水乙醇作医用消毒机 |
| C | 明矾溶液显酸性 | 明矾作净水剂 |
| D | 油脂在碱性条件下水解 | 热的NaOH溶液鉴别植物油和矿物质 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
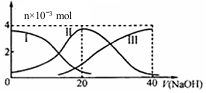 常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中I代表H2A,II代表HAˉ,III代表A2ˉ).根据图判断,下列说法正确的是( )
常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中I代表H2A,II代表HAˉ,III代表A2ˉ).根据图判断,下列说法正确的是( )| A. | 当V(NaOH)=20mL时,溶液中离子浓度大小关系:c(Na+)>c(A2-)>c(H+)>c(HA-)>c(OH-) | |
| B. | 等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水的大 | |
| C. | 当V(NaOH)=30 mL时,溶液中存在以下关系:2c(H+)+3c(H2A)+c(HA-)=c(A2-)+2c(OH-) | |
| D. | 向NaHA溶液加入水的过程中,pH可能增大也可能减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 反应一段时间后,X与Y的物质的量之比仍为1:1 | |
| B. | 达到平衡时,且反应放出0.1aKJ的热量 | |
| C. | 达到平衡后,若向平衡体系中充入稀有气体,Z的正反应速率将不发生变化 | |
| D. | X的体积分数保持不变,说明反应已达到平衡 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等质量的汽油和甲烷燃烧,甲烷产生的热量比汽油多,因此甲烷更高效 | |
| B. | 产生相同热量所生成的二氧化碳,汽油比甲烷多,因此甲烷更低效 | |
| C. | 甲烷含碳量低,燃烧更充分,不易积炭,不易产生CO,因此更环保 | |
| D. | 等物质的量的汽油和甲烷燃烧,汽油产生的热量比甲烷多,因此更环保 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1L1mol/L的盐酸溶液中,所含HCl分子数为NA | |
| B. | 常温常压下,71gCl2溶于水,转移的电子数目为0.1NA | |
| C. | 标准状况下,22.4LSO2和SO3的混合物,含硫原子的数目为NA | |
| D. | 0.5mol乙醇中含有的极性共价键数目为3.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
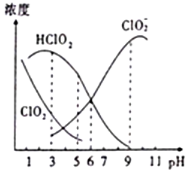 织物漂白剂亚氯酸钠(NaClO2)在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都只有漂白作用,但ClO2是有毒气体.25℃时,各组分浓度随pH变化情况如图所示(Cl-没有画出).下列说法不正确的是( )
织物漂白剂亚氯酸钠(NaClO2)在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都只有漂白作用,但ClO2是有毒气体.25℃时,各组分浓度随pH变化情况如图所示(Cl-没有画出).下列说法不正确的是( )| A. | 25℃时,ClO2-的水解平衡常数Ka=10-6 | |
| B. | 在pH约为4.0~4.5范围内使用该漂白剂较好 | |
| C. | 25℃时,等浓度的HClO2溶液和NaClO2溶液等体积混合后,混合溶液中:c(HClO2)+c(H+)+c(Na+)═c(ClO2-)+2c(OH-) | |
| D. | 当pH=5时往NaClO2溶液中滴入稀氢氧化钠溶液,溶液中主要反应的离子方程式是:HClO2+OH-═H2O+ClO2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 应用 | 解释 |
| A | 在相同条件下,在两支试管中各加入2mL 5% H2O2溶液,再向H2O2溶液中分别滴入1mL H2O和1mL 0.1mol•L-1 FeCl3溶液,对比观察现象 | 可以探究催化剂FeCl3对H2O2 分解速率的影响 |
| B | 向盛有1mL 0.01mol•L-1 AgNO3溶液的试管中滴加5滴0.01mol•L-1 NaCl溶液,有白色沉淀生成,再向其中滴加0.01mol•L-1 KI溶液,产生黄色沉淀. | 常温下,Ksp(AgCl)>Ksp(AgI) |
| C | 向两份蛋白质溶液中分别滴加饱和NaCl溶液和CuSO4溶液,均有固体析出 | 蛋白质均发生变性 |
| D | 保存硫酸亚铁溶液需加入少量稀盐酸和铁钉 | 防止 Fe2+水解以及被 O2 氧化 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol•L-1的HF溶液加水稀释过程中,HF的电离平衡常数逐渐增大 | |
| B. | pH=12的NaOH溶液与pH=2的醋酸溶液等体积混合后,溶液呈中性 | |
| C. | pH=5的NaHSO3溶液中水电离出的H+浓度小于10-71mol•L-1 | |
| D. | 向Na2CO3,Na2SO4的混合溶液中逐滴加入BaCl2溶液,一定先生成BaSO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com