
某同学欲配制0.1 mol/LBa(OH)2溶液,但只找到在空气中暴露已久的Ba(OH)2试剂。配制溶液时发现所取试剂在水中仅部分溶解,烧杯中存在大量未溶物。
(1)他猜测烧杯中未溶物为BaCO3。理由是_____________;检验方法是_______________。
(2)为准确测定样品中Ba(OH)2的含量。进行如下实验:
①配制250 mL约0.1 mol/L Ba(OH)2溶液:称取5.000 g试样,置于烧杯中,加适量蒸馏水,充分搅拌溶解,静置过滤,得滤液和沉淀,将滤液转入______中,洗涤,定容,摇匀。
②滴定:准确量取25.00 mL所配制Ba(OH)2溶液于锥形瓶中,滴加2滴甲基橙,将0.200 mol/L标准盐酸装入滴定管,滴定至终点,记录数据。重复滴定2次。平均消耗盐24.20 mL。计算样品中Ba(OH)2的质量分数为____________。
(3)上述滴定中,滴定管在注入标准盐酸之前,先用蒸馏水洗净,再用________________。在滴定中,准确读数应该是滴定管上蓝线的________________处所对应的刻度。滴定终点的现象是_______________。
(1)Ba(OH)2能与空气中的CO2反应,生成难溶于水的BaCO3;取适量沉淀于试管中,滴加稀盐酸,若有无色无味的气体产生,且产生的气体能使澄清石灰水变混浊,说明该试剂中含有BaCO3(2分)。
(2)①250 mL容量瓶中。②0.82764(或0.83)(2分)。
(3)标准盐酸溶液润洗2~3次,粗细交界点。溶液由黄色变为橙色,且半分钟内保持不变。
解析试题分析:(1)氢氧化钡溶液与空气中的二氧化碳反应生成碳酸钡沉淀和水,化学方程式为:
CO2+Ba(OH)2=BaCO3↓+H2O;沉淀中若含有碳酸钡,加入盐酸,碳酸钡与盐酸反应产生二氧化碳,会看到有气泡产生。
(2)①配制250 mL约0.1 mol/L Ba(OH)2溶液要用250 mL容量瓶。
②0.82764(或0.83)(2分)。
Ba(OH)2 ~ 2HCl
1mol 2mol
25.00 mL×cmol/L 0.200 mol/L×24.20mL
Ba(OH)2 浓度0.0968mol/L Ba(OH)2的质量0.0968mol/L×0.250 L×171g/mol =4.1382g
中Ba(OH)2的质量分数为4.1382÷5×100%=0.82764(或0.83)
(3)滴定管要用标准液润洗2~3次,准确读数应该是滴定管上蓝线粗细交界点,溶液由黄色变为橙色,且半分钟内保持不变。
考点:考查物质成分与含量测定。


科目:高中化学 来源: 题型:填空题
为了将混有K2SO4、MgSO4的KNO3固体提纯,并制得纯净的KNO3溶液,某学生设计如下实验方案: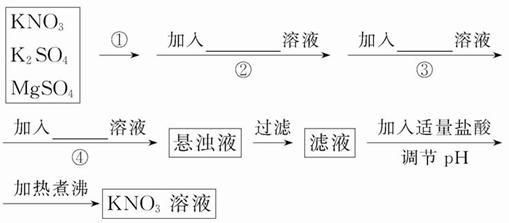
(1)操作①为___________________________。
(2)操作②~④加入的试剂依次可以为:___________________________________________________。
(3)如何判断SO42-已除尽?____________________________。
(4)实验过程中产生的多次沉淀_______ (填“需要”或“不需要”)多次过滤,其理由是_______________________________________________________。
(5)该同学的实验设计方案是否严密?请说明理由:___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
.(16分)化学实验是科学探究的基础。请回答有关实验问题:
(1)下面的四个实验装置有三个都存在明显缺陷,其中完全正确的是 :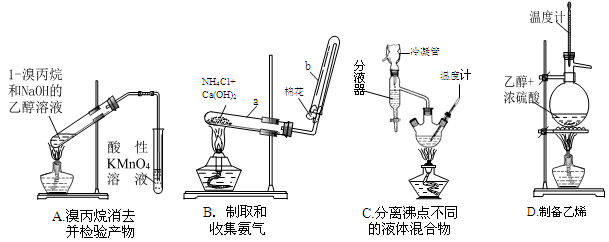
(2)要检验上面B装置氨气已集满的操作是 则试管已集满。
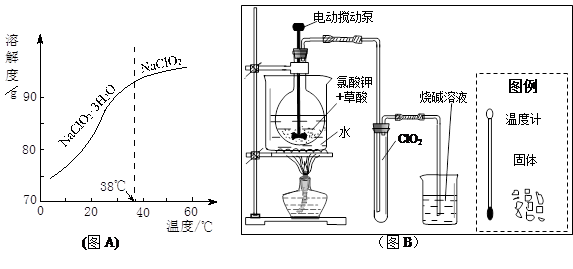
(3)ClO2是一种安全、高效、广谱、强力杀菌剂,其性质如右表:
①由下表可以看出:保存液态ClO2的条件是密封、 ;ClO2与碱反应的离子方程式 ;观察下“图A”,要从NaClO2溶液制得不含结晶水的晶体,操作是蒸发结晶,控制条件是 ;应控制析出晶体的温度范围是 。
| 色态 | 溶于碱 | 超过1Kpa、受热或遇光 | |
| 常温气体 | -59-11℃ 红黄色液体 | 生成亚氯酸盐和氯酸盐 | 爆炸 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
(15分)S2Cl2常用于橡胶硫化、有机物氯化的试剂,实验室可利用如下装置来制备S2Cl2。(部分夹持仪器已略去)
已知:①制备的反应方程式为:
②反应涉及的几种物质性质如下:
| 性质 物质 | 熔点 | 沸点 | 着火点 | 其他性质 |
| 单斜硫 | 119.2℃ | 446.6℃ | 363℃ | / |
| 斜方硫 | 112.8℃ | 446.6℃ | 363℃ | / |
| S2Cl2 | -77℃ | 137℃ | / | 遇水强烈分解生成S、SO2和HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
亚硝酸钠(NaNO2)是一种外观与食盐相似的食品添加剂。某化学兴趣小组进行如下实验。
【实验I】
用如下装置(已省略夹持装置)制NaNO2。
已知:2NO+Na2O2=2NaNO2;2NO2+Na2O2=2NaNO3。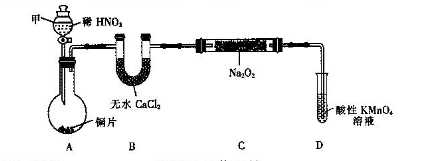
(1)仪器甲的名称是________.装置B的作用是_________________________。
(2)装置D可将剩余的NO氧化成NO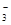 ,发生反应的离子方程式为_____________。
,发生反应的离子方程式为_____________。
(3)使用气密性良好的上述装置进行实验,NaNO2的纯度较低。为提高NaNO2纯度须对
上述实验装置或药品进行改进,其改进措施是________________________________。
【实验Ⅱ】
利用目视比色法(比较溶液颜色深浅以测定物质浓度)测定泡菜样品中NaNO2的含量。
步骤i:在5个有编号的试管中分别加入不同量的NaNO2溶液,各加入1 mL的M溶液 (M遇NaNO2呈紫红色,NaNO2浓度越大颜色越深),再加蒸馏水至总体积均为l0 mL并振荡,制成标准色阶。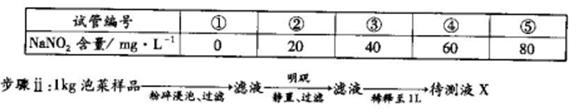
步骤ⅲ:取5 mL待测液X,加入1 mLM溶液,加蒸馏水至10mL振荡,与标准色阶比较。
(4)步骤ii获取待测液X的过程中,加入明矾的目的是__________。
(5)步骤iii比较结果与④号色阶颜色相同,此泡菜样品中NaNO2的含量为_________mg·kg-1
(6)用目视比色法证明泡菜中加入维生素C可以降低NaNO2的含量。设计并完成下列实
验报告。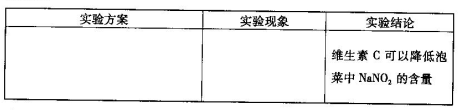
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
生铁中除铁外,还含有其他元素,如碳元素和硫元素。其中碳主要以碳化铁的形态存在,它使生铁性能坚硬而脆,所以生铁的用途不大,一般用做炼钢的原料。某兴趣小组设计按下图所示的实验装置,测定生铁中的含碳量。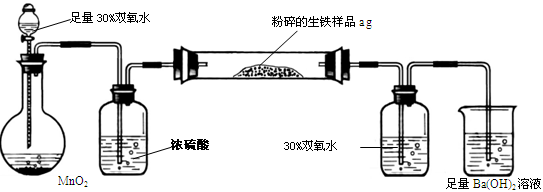
A B C D E
请回答下列问题:
(1)硫在生铁中是有害元素,它使生铁产生热脆性。硫元素在生铁中最有可能存在的价态是
| A.-2 | B.0 | C.+4 | D.+6 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
PCl3可用于半导体生产的外延、扩散工序。有关物质的部分性质如下:
| | 熔点/℃ | 沸点/℃ | 密度/g·mL-1 | 其他 |
| 黄磷 | 44.1 | 280.5 | 1.82 | 2P(过量)+3Cl2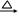 2PCl3;2P+5Cl2(过量) 2PCl3;2P+5Cl2(过量)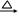 2PCl5 2PCl5 |
| PCl3 | -112 | 75.5 | 1.574 | 遇水生成H3PO3和HCl,遇O2生成POCl3 |
| POCl3 | 2 | 105.3 | 1.675 | 遇水生成H3PO4和HCl,能溶于PCl3 |
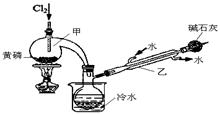
 H3PO4+2HI;b.(NH4)3BO3溶液可与HI和H3PO4反应生成H3BO3(弱酸);c.Na2S2O3溶液可定量测定碘:I2+2Na2S2O3→Na2S4O6+2NaI
H3PO4+2HI;b.(NH4)3BO3溶液可与HI和H3PO4反应生成H3BO3(弱酸);c.Na2S2O3溶液可定量测定碘:I2+2Na2S2O3→Na2S4O6+2NaI查看答案和解析>>
科目:高中化学 来源: 题型:实验题
(14分)绿矾晶体(FeSO4·7H2O,M=278g/mol)是治疗缺铁性贫血药品的重要成分。实验室利用硫酸厂的烧渣(主要成分为Fe2O3及少量FeS、SiO2),制备绿矾的过程如下: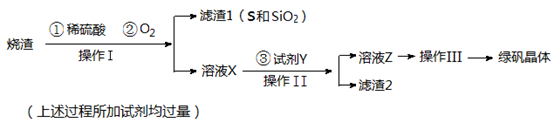
试回答:
(1)操作Ⅰ为 (填写操作名称)。
(2)试剂Y与溶液X反应的离子方程式为 。
(3)操作Ⅲ的顺序依次为: 、冷却结晶、过滤 、 、干燥。
(4)某同学用酸性KMnO4溶液测定绿矾产品中Fe2+含量:
a.称取11.5g绿矾产品,溶解,配制成1000mL溶液;b.量取25.00mL待测溶液于锥形瓶中;
c.用硫酸酸化的0.01000mol/L KMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL。
①步骤a配制溶液时需要的玻璃仪器除玻璃棒、量筒、烧杯、胶头滴管外,还需
②该同学设计的下列滴定方式,最合理的是 (夹持部分略去)(填字母序号)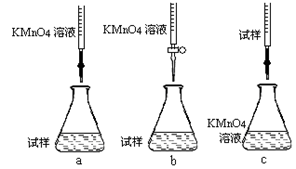
③滴定时发生反应的离子方程式为: 。
④判断此滴定实验达到终点的方法是 ;若在滴终点读取滴定管刻度时,俯视KMnO4溶液液面,其它操作均正确,则使测定结果 (填“偏高”“偏低”“无影响”)。
⑤计算上述样品中FeSO4·7H2O的质量分数为
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
硫酸亚铁铵(NH4)2Fe(SO4)2·6H2O是一种浅绿色晶体,在水中的溶解度较小,不溶于乙醇。某实验小组利用镀锌铁片来制备硫酸亚铁铵的过程如下:
(1)加入盐酸是为了除去锌镀层,判断锌镀层已被除去的现象是 。
(2)A物质可以是 (选填序号)。
a.CuCl2 b.CuO c.Cu(NO3)2 d.CuSO4
加入少量A物质的目的是 。
(3)操作Ⅱ的名称为 。
(4)采用晾干而不用加热烘干晶体的原因是 。
(5)工业上常用K2Cr2O7溶液测定硫酸亚铁铵的纯度,反应中Cr2O72—被还原成Cr3+。
写出硫酸亚铁铵溶液与酸性K2Cr2O7溶液反应的离子方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com