
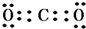 ,故答案为:
,故答案为: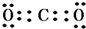 ;
;

 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:
| A、向CaCl2溶液中通入少量CO2气体:Ca2++CO2+H2O=CaCO3↓+2H+ |
| B、向次氯酸钙溶液通入SO2:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO |
| C、向NH4HSO4溶液中滴加少量NaOH溶液:H++OH-=H2O |
| D、碳酸钙溶于醋酸溶液:CaCO3+2H+=Ca2++CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| IA | 0 | |||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | ⅦA | |
| 2 | ⑩ | ② | ③ | ④ | ⑧ | |||
| 3 | ⑤ | ⑥ | ⑦ | ⑨ | ||||
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 除杂试剂 | 离子方程式 | 操作 | |
| (1)BaCl2(HCl) | 过量 |
过滤 | |
| (2)Cu(Zn) | |||
| (3)SiO2(Al2O3) | |||
| (4)CO(CO2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| [OH-] |
| [NH3?H2O] |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH4Cl溶液中:c(NH4+)>c(Cl-)>c(H+)>c(OH-) |
| B、NaHSO3溶液(呈酸性)中:c(Na+)>c(HSO3-)>c(SO32-)>c(H2SO3) |
| C、CH3COONa溶液中:c(CH3COOH)+c(H+)=c(OH-) |
| D、Na2CO3溶液中:2c(Na+)=c(CO32- )+c(HCO3- )+c(H2CO3) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com