
| A. | 称量NaOH固体时,放在烧杯中且称量较慢 | |
| B. | 定容时,俯视刻度线 | |
| C. | 定容时,加水超过刻度线,再用胶头滴及将过线的液体吸出 | |
| D. | 移液前,容量瓶中有少量蒸馏水 |
分析 分析操作对溶质的物质的量和溶液体积的影响,依据c=$\frac{n}{V}$进行误差分析,凡是使溶质的物质的量n偏大或者使溶液体积V偏小的操作,溶液浓度都偏高,反正溶液浓度偏低.
解答 解:A.氢氧化钠易潮解变质,称量NaOH固体时,放在烧杯中且称量较慢,导致配制的溶液中氢氧化钠的物质的量偏小,配制的溶液浓度偏低,故A错误;
B.定容时俯视刻度线,导致溶液体积偏小,溶液浓度偏高,故B正确;
C.定容时,加水超过刻度线,再用胶头滴及将过线的液体吸出,导致溶液中溶质的物质的量偏小,溶液浓度偏低,故C错误;
D.容量瓶不干燥,含有少量蒸馏水,对溶质的物质的量和溶液体积都不会产生影响,溶液浓度不受影响,故D错误;
故选B.
点评 本题考查了一定物质的量浓度溶液配制的误差分析,准确把握操作对溶质的物质的量和溶液体积的影响,依据c=$\frac{n}{V}$进行误差分析是解题关键,题目难度不大.


 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案科目:高中化学 来源: 题型:选择题
| A. | ①③④⑤⑥ | B. | ②④⑤⑥ | C. | ⑤⑥ | D. | ④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
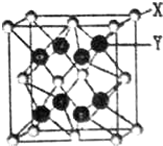 X与Y可形成离子化合物,其晶胞结构如下图所示.其中X离子的配位数为8,若该晶体的密度为pg•cm3,X和Y的相对原子质量分别为a和b,则晶胞中距离最近的X、Y之间的核间距离是$\frac{{\sqrt{3}}}{4}×\root{3}{{\frac{4a+8b}{{ρ•{{N}_A}}}}}$cm(NA表示阿伏伽德罗常数,用含p、a、b、NA的代数式表达).
X与Y可形成离子化合物,其晶胞结构如下图所示.其中X离子的配位数为8,若该晶体的密度为pg•cm3,X和Y的相对原子质量分别为a和b,则晶胞中距离最近的X、Y之间的核间距离是$\frac{{\sqrt{3}}}{4}×\root{3}{{\frac{4a+8b}{{ρ•{{N}_A}}}}}$cm(NA表示阿伏伽德罗常数,用含p、a、b、NA的代数式表达).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
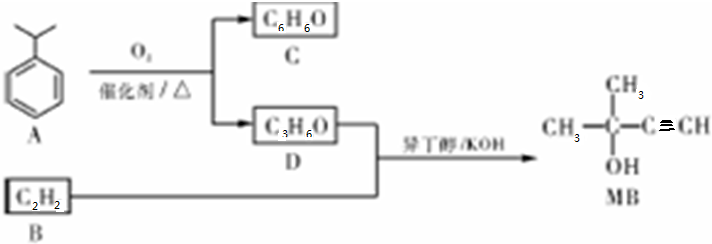
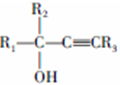
 ,D的官能团名称为羰基.
,D的官能团名称为羰基.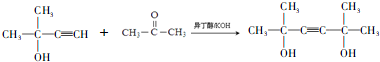 .
.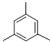 .
.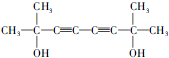 ,医药中间体,材料中间体)的合成路线
,医药中间体,材料中间体)的合成路线 或
或 .
.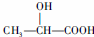 $→_{△}^{浓硫酸}$CH2=CH-COOH$→_{浓硫酸/△}^{CH_{3}OH}$CH-COOH3.
$→_{△}^{浓硫酸}$CH2=CH-COOH$→_{浓硫酸/△}^{CH_{3}OH}$CH-COOH3.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
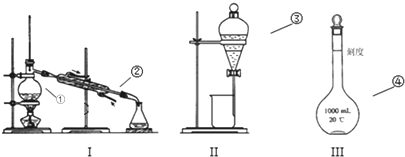
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol氯化钾含有6.02×1023个KCl分子 | |
| B. | 6.02×1024个CO2分子的物质的量是1mol | |
| C. | 1molN2O4含有1molN2分子和4molO原子 | |
| D. | 1molH2分子和1molH2O分子所含的氢原子数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 治理拥堵,减少汽车尾气排放,大力发展清洁能源可以有效减少雾霾 | |
| B. | 铜的金属活动性比铝弱,可以用铜罐代替铝罐储运浓硝酸 | |
| C. | 光化学烟雾的形成和氮的氧化物有关,硫的氧化物是形成硫酸型酸雨的主要物质 | |
| D. | 硫化钠和亚硫酸钠的固体如果长期暴露在空气中容易变质 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
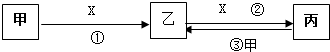
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com