
【题目】实验室需要配制1.0mol/L的氢氧化钠溶液480mL。完成下列各题。
(1)应选择规格为__mL的容量瓶,该容量瓶上除注明规格外,还标有_____(选填编号)。
a.温度 b.浓度 c.压强 d.刻度线
(2)用电子天平称取_____gNaOH。
(3)将称好的氢氧化钠固体加_____将其溶解,待冷却后将溶液移入容量瓶中。
(4)用少量蒸馏水冲洗____2~3次,将洗液移入容量瓶中。
(5)向容量瓶内加水至接近刻度1~2cm处,改用胶头滴管小心地加水至______________。
(6)最后塞好瓶塞,摇匀,将配好的溶液移入__(选填编号)中并贴好标签。
a.  b.
b.  c.
c.  d.
d. 
(7)分析下列操作可能会对氢氧化钠溶液浓度造成的影响(填“偏高”、“偏低”或“无影响”)。
①氢氧化钠溶解后,未冷却即转移___。
②定容时仰视_____。
【答案】500 ad 20.0 适量蒸馏水 烧杯和玻璃棒 刻度线 c 偏高 偏低
【解析】
配制480mL1.0mol/L的氢氧化钠溶液,实验室没有480mL容量瓶,需要选用500mL容量瓶进行配制;根据m=cVM计算出需要氢氧化钠的质量;根据溶液的配制过程回答各操作中的相关问题;根据c=n/V分析操作对溶质的物质的量或对溶液的体积的影响判断。
(1)实验室配制480mL1.0mol/L的氢氧化钠溶液,由于没有480mL容量瓶,需选用500mL容量瓶;容量瓶上注明有规格、温度、刻度线;
答案是: 500;ad;
(2)配制500mL1.0mol/L的氢氧化钠溶液,需要氢氧化钠的质量为:40g/mol×1.0mol/L×0.5L=20.0g;
故答案是:20.0;
(3)将称好的氢氧化钠固体加适量蒸馏水在烧杯中将其溶解,待冷却后将溶液移入容量瓶中;
故答案是:适量蒸馏水;
(4)为保证溶质全部转移进容量瓶内,用少量蒸馏水冲洗烧杯内壁和玻璃棒2~3次,将洗液移入容量瓶中;
故答案是:烧杯和玻璃棒;
(5)向容量瓶内加水至接近刻度1~2cm处,改用胶头滴管小心地加水至刻度线,使液体的凹液面与刻度线相切;
故答案是:刻度线;
(6)液体试剂应转移到细颈的玻璃试剂瓶中,并贴好标签,由于溶液显碱性,需用橡胶塞,故答案选c;
故答案是:c。
(7)①氢氧化钠溶解后,未冷却即转移进容量瓶,当溶液冷却到室温后,液面低于刻度线,溶液的体积偏小,根据c=n/V可知,所配溶液的浓度偏高;
②定容时仰视,溶液的体积偏大,根据c=n/V可知,所配溶液的浓度偏低;
故答案是:偏高;偏低。


科目:高中化学 来源: 题型:
【题目】下列物质的分子中既有σ键,又有π键,并含有非极性键的是( )
①H2O2 ②N2 ③H2O ④HCl ⑤C2H4 ⑥C2H2
A. ②⑤⑥ B. ①②⑤⑥ C. ②③④ D. ②④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙炔(C2H2)在气焊、气割及有机合成中用途非常广泛,可由电石(CaC2)直接水化法或甲烷在1500℃左右气相裂解法生产。
(1)电石水化法制乙炔是将生石灰与焦炭在3000℃下反应生成CaC2,CaC2再与水反应即得到乙炔。CaC2与水反应的化学方程式为___________________________。
(2)已知:CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH1=-890.3 kJ/mol
C2H2(g)+2.5O2(g)===2CO2(g)+H2O(l) ΔH2=-1299.6 kJ/mol
2H2(g)+O2(g)===2H2O(l) ΔH3=-571.6 kJ/mol
则甲烷气相裂解反应:2CH4(g)===C2H2(g)+3H2(g)的ΔH=________kJ/mol。
(3)哈斯特研究得出当甲烷分解时,几种气体平衡时分压(Pa)与温度(℃)的关系如图所示。

①T1℃时,向1 L恒容密闭容器中充入0.3 mol CH4只发生反应2CH4(g) ![]() C2H4(g)+2H2(g),达到平衡时,测得c(C2H4)=c(CH4)。该反应的ΔH_____0(填“>”或“<”),CH4的平衡转化率为________。上述平衡状态某一时刻,若改变温度至T2℃,CH4以0.01 mol/(L·s)的平均速率增多,经t s后再次达到平衡,平衡时,c(CH4)=2c(C2H4),则T1_____(填“>” 或“<”)T2,t=________s;
C2H4(g)+2H2(g),达到平衡时,测得c(C2H4)=c(CH4)。该反应的ΔH_____0(填“>”或“<”),CH4的平衡转化率为________。上述平衡状态某一时刻,若改变温度至T2℃,CH4以0.01 mol/(L·s)的平均速率增多,经t s后再次达到平衡,平衡时,c(CH4)=2c(C2H4),则T1_____(填“>” 或“<”)T2,t=________s;
②列式计算反应2CH4(g) ![]() C2H2(g)+3H2(g)在图中A点温度时的平衡常数K=__________________(用平衡分压代替平衡浓度计算,lg0.05=-1.3);
C2H2(g)+3H2(g)在图中A点温度时的平衡常数K=__________________(用平衡分压代替平衡浓度计算,lg0.05=-1.3);
③由图可知,甲烷裂解制乙炔有副产物乙烯生成,为提高甲烷制乙炔的转化率,除改变温度外,还可采取的措施有__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,试管中盛装的是气体呈红棕色,当倒扣在盛有水的水槽中时,试管内水面上升,但不能充满试管,当向试管内鼓入氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管内完全被水充满,原来试管中盛装的可能是

A.可能是N2与NO2的混和气体
B.只可能是NO2一种气体
C.可能是NO与NO2的混和气体
D.可能是H2与NO2的混和气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素 A、B、C、D 的原子序数依次增大,A 和B 形成的气态化合物的水溶液呈碱性,B 位于第ⅤA 族,A 和 C 同主族,D 原子最外层电子数与电子层数相等。下列叙述正确的是
A. 原子半径:D>C>B
B. 单质的还原性:D>C
C. 1molC 的氧化物固体中含离子总数为 4NA
D. 元素B、C、D 的最高价氧化物对应水化物能相互反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三种常见单萜类化合物的结构如下图所示。下列说法正确的是( )

A. 香叶醇和龙脑互为同分异构体,分子式均为![]()
B. 可用金属钠鉴别香叶醇和月桂烯
C. 龙脑分子中所有碳原子在同一个平面上
D. 1mol月桂烯最多能与![]() 发生加成反应
发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石墨烯电池是利用锂离子在石墨烯表面和电极之间快速大量穿梭运动的特性而研发的新型可充放电电池,其反应式为LixC6+Li1-xCoO2![]() C6+LiCoO2,其工作原理如下图所示。下列关于该电池的说法正确的是( )
C6+LiCoO2,其工作原理如下图所示。下列关于该电池的说法正确的是( )
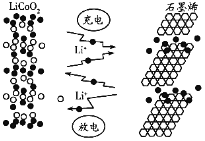
A. 充电时,![]() 嵌入
嵌入![]() 中
中
B. 放电时,![]() 极发生的电极反应为
极发生的电极反应为![]()
C. 放电时负极反应为:![]()
D. 充电时,若转移![]() ,石墨烯电极增重7g
,石墨烯电极增重7g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A 是由两种元素组成的化合物,质量比为 7:8,在真空中加热分解,生成 B、C。E 是常见的液体,C 和E 高温下能发生反应。F 为日常生活中常见的化合物,E、F 之间的反应常用于工业生产,I 为黄绿色气体单质。

(1)写出 A 的化学式:____
(2)写出 K 的电子式:______
(3)写出 C 和 E 高温下能发生反应的方程式:______
(4)写出 D 和 L 发生反应的离子方程式:_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
(1)将等体积等物质的量浓度的醋酸和氢氧化钠溶液混合后,溶液呈________(填“酸性”、“中性”或“碱性”,下同),溶液中c(Na+)______c(CH3COO-)(填“>”、“=”或“<”,下同)。
(2)pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈________性,溶液中c(Na+)________c(CH3COO-)
(3)常温下将0.2 mol·L-1 HCl溶液与0.2 mol·L-1 MOH溶液等体积混合,测得混合溶液的pH=6,则混合溶液中由水电离出的c(H+)________0.2 mol·L-1 HCl溶液中由水电离出的c(H+)。(填“>”、“<”或“=”,下同)
(4)常温下若将0.2 mol·L-1MOH溶液与0.1 mol·L-1 HCl溶液等体积混合,测得混合溶液的pH<7,则说明在相同条件下MOH的电离程度________MCl的水解程度。
(5)常温下若将pH=3的HR溶液与pH=11的NaOH溶液等体积混合,测得混合溶液的pH≠7,则混合溶液的pH________。(填“>7”、“<7”或“无法确定”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com