
把铁与铜的混合物放入稀硝酸中,充分反应后固体有剩余,然后过滤,把滤出的固体物质投入盐酸中无气体放出,则滤液中一定含有的金属盐是( )
A.Cu(NO3)2 B.Fe(NO3)3 C.Fe(NO3)2 D.Fe(NO3)2和Cu(NO3)2
科目:高中化学 来源: 题型:
有两种有机物Q( 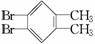 )与P(
)与P(  ),下列有关它们的说法中正
),下列有关它们的说法中正
确的是( )
A.二者的核磁共振氢谱中均只出现两种峰且峰面积之比为3∶1
B.二者在NaOH醇溶液中均可发生消去反应
C.一定条件下,二者在NaOH溶液中均可发生取代反应
D.Q的一氯代物只有1种、P的一溴代物有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:
CO(g) +H2O(g)  CO2(g) +H2 (g) △H<0。
CO2(g) +H2 (g) △H<0。
(1)CO和H2O浓度变化如右图,则在该温度下,该反应的平衡常数K= 。 0~4min的平均反应速率v(CO)=_____mol·L-1·min-1。若降低温度,该反应的K值将 ,该反应的化学反应速率将 (填“增大”“减小”或“不变”)。
(2)在相同容器中发生上述反应,当温度高于850℃时, 容器内各物质的浓度变化如下表。
| 时间(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
① 表中3min~4min之间反应处于______状态; c 1数值_____0.08 mol·L-1 (填大于、小于或等于)。
②反应在4min~5min间,平衡向逆方向移动,可能的原因是_________
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度
(3)在相同温度下(850℃),若起始时c(CO)=1mol·L-1,c(H2O)=2mol·L-1,反应进行一段时间后,测得H2的浓度为0.5 mol·L-1,则此时该反应是否达到平衡状态 (填“是”与“否”),此时v(正) v(逆)(填“大于”“小于”或“等于”),你判断的依据是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
按要求填空。
(1)根据常温下氯化铵、氢氧化钡两种晶体混合搅拌反应的现象判断:
该反应△S 0,△H 0(均填“<”、“>”或“=”,下同);
(2)已知:升高温度时,反应2CH4(g) C2H4(g)+2H2(g)的平衡转化率增大,现有:
C2H4(g)+2H2(g)的平衡转化率增大,现有:
C(s)+2H2(g) CH4(g) ΔH1;2C(s)+2H2(g)
CH4(g) ΔH1;2C(s)+2H2(g) C2H4(g) ΔH2 则2ΔH1 ΔH2
C2H4(g) ΔH2 则2ΔH1 ΔH2
(3)在常温常压下测得:C(s)的燃烧热为393 kJ/mol,而1molC(s)燃烧成CO(g)放热110kJ,且6FeO(s)+O2(g)=2Fe3O4(s) ΔH=−480 kJ/mol。
请写出CO(g)还原Fe3O4(s)生成FeO(s)的热化学方程式:
;
(4)已知由气态分子断裂1mol以下共价键吸收的能量为:C-H:410kJ O=O:500 kJ C=O:750 kJ O-H:460 kJ,且常温下1mol水气化时吸收热量45kJ。写出常温下甲烷燃烧的热化学方程式:
;
查看答案和解析>>
科目:高中化学 来源: 题型:
引起下列物质颜色变化的化学方程式(或离子方程式)表示正确的是 ( )
A.暴露在空气中,淡黄色Na2 O2变成白色固体:Na2O2 +H2O 2Na+ +2OH-+O2 ↑
B.降温至-15℃时,红棕色NO2变成无色液体:2NO2  N2O4
N2O4
C.向AgCl悬浊液中加入硫化钠变黑:2Ag+ +S2- Ag2S↓
D.向CuSO4溶液中加入Ba(OH)2溶液,观察到有色沉淀生成:Cu2+ +2OH- Cu(OH)2↓
查看答案和解析>>
科目:高中化学 来源: 题型:
已知0.1mol·L-1的醋酸溶液中存在电离平衡:
CH3COOH CH3COO-+H+,要使溶液中c(H+)/c(CH3COOH)
CH3COO-+H+,要使溶液中c(H+)/c(CH3COOH)
的值增大,可以采取的措施是 ( )
①加少量烧碱溶液 ②升高温度 ③加少量冰醋酸 ④加水
A.①② B.①③ C.②④ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
在温度t ℃下,某Ba(OH)2的稀溶液中c(H+)=10-amol/L,c(OH-)=10-bmol/L,已知a+b=12,
向该溶液中逐滴加入pH=b的盐酸,测得混合溶液的部分pH如下表所示:
| 序号 | 氢氧化钡的体积/mL | 盐酸的体积/mL | 溶液的pH |
| ① | 22.00 | 0.00 | 8 |
| ② | 22.00 | 18.00 | 7 |
| ③ | 22.00 | 22.00 | 6 |
(1)依据题意判断,t ℃____25℃(填“大于”、“小于”或“等于”),该温度下水的离子积Kw=_____。
(2)b=____________,原Ba(OH)2的稀溶液的物质的量浓度为_____________。
(3)该温度下,向1L硫酸与硫酸钠的混合溶液中加入3L该Ba(OH)2的稀溶液时,沉淀正好达
最大量,从所得溶液中取出4mL并加水稀释至20mL,测得溶液的pH为7,则原硫酸与硫酸
钠混合溶液的pH为_________,以及其中Na2SO4的物质的量浓度为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在恒温时,一固定容积的容器内发生如下反应:2NH3 (g) 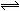 N2 (g)+3H2 (g),达平衡后,再向容器内通入一定量的NH3(g),重新达到平衡后,与第一次平衡时相比,NH3的体积分数( )
N2 (g)+3H2 (g),达平衡后,再向容器内通入一定量的NH3(g),重新达到平衡后,与第一次平衡时相比,NH3的体积分数( )
A.不变 B.增大 C.减小 D.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
分类法在化学学科的发展中起到了非常重要的作用。下列分类标准合理的是
①根据氧化物的组成元素将氧化物分成酸性氧化物、碱性氧化物等
②根据反应中是否有电子转移将化学反应分为氧化还原反应和非氧化还原反应
③根据分散系是否有丁达尔现象将分散系分为溶液、胶体和浊液
④根据水溶液是否能够导电将化合物分为电解质和非电解质
A.② B. ①③ C.②③ D. ②③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com