
��ѧ������ý����ƻ�ԭCCl4��SiCl4�Ƶ�һ��һάSiC����������ط�Ӧ�Ļ�ѧ����ʽΪ��8Na+CCl4+SiCl4=SiC+8NaCl������˵������ȷ����
A��һάSiC���װ����ȱ��������С�����н�ǿ����������
B��������Ӧ��SiC���������������ǻ�ԭ����
C��SiCl4���ɼ��Լ����ɵķǼ��Է���
D��ÿ����1mol SiCת��8mol����
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꽭��ʡ�߶��϶����¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�ں��¡������£��������·�Ӧ��2A��g��+2B��g�� C��g��+3D��g�����ִ�����;���ֱ���ƽ�⡣;����A��B����ʼŨ�Ⱦ�Ϊ2mol/L����;����C��D����ʼŨ�ȷֱ�Ϊ2mol/L��6mol/L������������ȷ���� �� ��
C��g��+3D��g�����ִ�����;���ֱ���ƽ�⡣;����A��B����ʼŨ�Ⱦ�Ϊ2mol/L����;����C��D����ʼŨ�ȷֱ�Ϊ2mol/L��6mol/L������������ȷ���� �� ��
A����ƽ��ʱ��;����ķ�Ӧ����V��A������;����ķ�Ӧ����V��A��
B����ƽ��ʱ��;�������û������Ũ�Ⱥ�;�������û�������Ũ�����
C����;�����մﵽƽ��ʱ����ϵ�ڻ������İٷ���ɲ�ͬ
D����;�����մﵽƽ��ʱ����ϵ�ڻ������İٷ������ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�찲��ʡ�����ϵ��Ĵζο���ѧ�Ծ��������棩 ���ͣ�ʵ����
��ƽ�������ʾ�����������в����ķϲ�����ĩ�к��ж�������(CeO2).
��1���ڿ���������Ce(OH)CO3���Ʊ�CeO2,�÷�Ӧ�Ļ�ѧ����ʽ
��2����֪��һ��������,�������״̬��CeO2���Ʊ�Ce,д�������ĵ缫��Ӧʽ ��
��3��ij�������������ϲ�����ĩ(����SiO2��Fe2O3��CeO2�Լ���������������ϡ�������)Ϊԭ��,�����ͼ1���̶���Դ���л���,�õ�Ce(OH)4���������.

�ٵõ�����Bʱ,��Ҫ�����������ϴ�Ӹɾ�.ϴ�ӵIJ����� ��
�ڷ�Ӧ��1�������ӷ���ʽΪ ��
�۲���I��������
����ͼ2,������ԭ�ζ����ⶨ�Ƶõ�Ce(OH)4��Ʒ�Ĵ���.
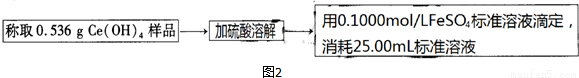
�ò�Ʒ��Ce(OH)4����������Ϊ (����С�������λ).���ζ�����FeSO4��Һ���ڿ�����¶����һ��ʱ��,���ø�Ce(OH)4��Ʒ�Ĵ��� (��ƫ�ߡ�����ƫ�͡�����Ӱ�족).
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016����������һ��ѧ�����ϵ������¿�����ѧ�Ծ��������棩 ���ͣ�ѡ����
��ѧ������������أ����й��������е�һЩ��������ѧ���� �� ��
A���ᳫʹ������
B��Al(OH)3������������
C����С�մ�����������ͷ
D���ý�Ũ������������Һϴ���·��ϵ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�찲������ɽ��������ͭ����У�����ϵ�����������ѧ�Ծ��������棩 ���ͣ������
����β����Ϊ������Ⱦ����Ҫ��Դ֮һ�����к��д������к����ʣ�����CO��NOx��̼�⻯����������������ȡ�������β��������ʹ���������������˾����ս���Իش��������⣺
��1����CH4����ԭNOx�������������������Ⱦ����֪��
��CH4��g��+4NO��g���T2N2��g��+CO2��g��+2H2O��g����H=-1160kJ•mol-1
��CH4��g��+4NO2��g���T4NO��g��+CO2��g��+2H2O��g����H=-574kJ•mol-1
����CH4��NO2��ɻ�ԭ��N2������CO2��ˮ�������Ȼ�ѧ����ʽ��____________________��
��2��NOxҲ�ɱ�NaOH��Һ���ն�����NaNO3��NaNO2����֪ij�¶��£�HNO2�ĵ��볣��Ka=9.7��10-4mol•L-1��NO2-��ˮ�ⳣ��ΪKh=8.0��10-10mol•L-1������¶���ˮ�����ӻ�����=______���ú�Ka��Kh�Ĵ���ʽ��ʾ������ʱ��Һ���¶�______25�棨������������������=������
��3������������CO�ϳɼ״�����Ӧ���Ȼ�ѧ����ʽΪ��CO��g��+2H2��g�� CH3OH��g����H=-90.8KJ•mol-1����ͬ�¶��£�CO��ƽ��ת��������ͼ��ʾ��ͼ��T1��T2��T3�ĸߵ�˳����________��������______��
CH3OH��g����H=-90.8KJ•mol-1����ͬ�¶��£�CO��ƽ��ת��������ͼ��ʾ��ͼ��T1��T2��T3�ĸߵ�˳����________��������______��

��4�������ϻ���������CH3OH����CH3OCH3���������Ϊ1.0L�ĺ����ܱ������з�����Ӧ��2CH3OH(g) CH3OCH3(g)+H2O(g)��
CH3OCH3(g)+H2O(g)��
������� | �¶ȣ��棩 | ��ʼ���ʵ�����mol�� | ƽ�����ʵ�����mol�� | |
CH3OH | CH3OCH3 | H2O | ||
�� | 387 | 0.20 | 0.080 | 0��080 |
�� | 207 | 0.20 | 0.090 | 0.090 |
�÷�Ӧ������ӦΪ________��Ӧ������ȡ��������ȡ���������ʼ�����������г���CH3OH0.15mol��CH3OCH30.15mol��H2O0.10mol����Ӧ����_____������У�����������桱����
��5��CH3OHȼ�ϵ���ڱ�ЯʽͨѶ�豸���������������Ź㷺��Ӧ�á���֪��ع���ʱ���ܷ�Ӧ����ʽΪ��2CH3OH+3O2=2CO2+4H2O����ع���ʱ��ʾ��ͼ����ͼ��ʾ��
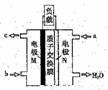
���Ӵ�������Ĥ����_____�缫�����M������N�����������ĵ缫��ӦʽΪ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�������������������ѧ��һ��10�»�ѧ���������棩 ���ͣ�ѡ����
��������Ĵ�С�����������й�.���¶Ⱥ�ѹǿ��ͬʱ,���������Ҫȡ����
A����������ʵ��� B���������֮���ƽ������
C��������ӱ����Ĵ�С D�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�츣��ʡ������ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ������
������������Ӱ�����ǵ����������������������������������Ҫԭ��֮һ��
��.��PM2.5����������ˮ�����Ƴɴ���������
��1��ijͬѧ��ø���������ˮ���������ӵĻ�ѧ��ּ���ƽ��Ũ���г��±�������ȱ�ٵ�������H+��OH�����䣩��
���� | K+ | Na+ | NH4+ | SO32- | NO3- | Cl- |
Ũ��/mol•L-1 | 7��10-6 | 3��10-6 | 2��10-5 | 3��10-5 | 5��10-5 | 2��10-5 |
���ݱ��������жϸ�������pH=_______���ñ���һ����������ָ��_____________________��
��.������������������ж��ַ�����
������һ ������ҵ�ϱ䡰�ϡ�Ϊ�������չ�ҵβ��SO2��NO���ɻ��Na2S2O4�������������ƣ���NH4NO3 ��Ʒ������ͼ��ͼ1��CeΪ��Ԫ�أ���
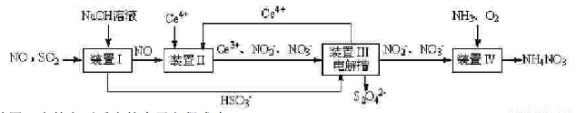
��2��װ�â��е���Ҫ��Ӧ�����ӷ���ʽΪ_____________________________��
��3��װ�â����ʹCe4+�����������ü���ȼ�յ�ص���װ���е���Һ��������24g����ʱ�������Ͽ�����______________mol Ce4+��
��4��������������������dz�ȥSO2�ij����������Ƚ���SO2�ķ�������ˮ�����ñ���ʯ�ҽ����գ�
���¶��£�����Һ��c(Ca2+)һֱ����Ϊ0.70mol/L����֪Ksp(CaSO3)=1.4��10-7.������Һ�е�SO32����Ũ��_____________�����������2λ��Ч���֣�
�������� ����NH3����ԭ�������SCR��������ĿǰӦ����㷺���������������ѳ���������Ӧԭ����ͼ2��ʾ��
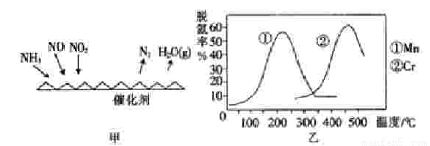
��5��ͼ���Dz�ͬ����Mn��Cr�ڲ�ͬ�¶��¶�Ӧ�������ʣ���ͼ�ۺϿ��ǿ�֪��ѵĴ�������Ӧ���¶ȷֱ�Ϊ____________��
��6����Fe������ʱ���ڰ�������������£���ͬ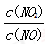 =1��1����Ч����ѣ���֪����11.2L N2���꣩��Ӧ�ų�������ΪQkJ����ʱ��Ӧ�����ⷴӦ���Ȼ�ѧ����ʽΪ_____________________��
=1��1����Ч����ѣ���֪����11.2L N2���꣩��Ӧ�ų�������ΪQkJ����ʱ��Ӧ�����ⷴӦ���Ȼ�ѧ����ʽΪ_____________________��
�������� ���û���̿��ԭ�����Դ����������
��Ӧԭ����1/2C(s)+NO(g) 1/2N2(g)+1/2CO2(g) ��H=-QkJ/mol
1/2N2(g)+1/2CO2(g) ��H=-QkJ/mol
��T1��ʱ����Ӧ���е���ͬ��ʱ���ø����ʵ�Ũ�����£�
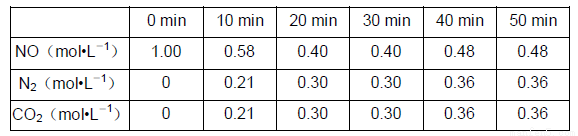
��7��T1��ʱ���÷�Ӧ��ƽ�ⳣ��K=_________________________��
��8��30min��ֻ�ı�ijһ��������Ӧ���´ﵽƽ�⣬�����ϱ��е������жϸı������������______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�������ʡ������ѧ��12���¿���ѧ�Ծ��������棩 ���ͣ������
���Ų��Ͽ�ѧ�ķ�չ�����������仯����õ���Խ��Խ�㷺��Ӧ�ã�������Ϊ���Ͻ�ά���ء�����ҵ�ϻ��շϷ�����������V2O5��VOSO4��K2SO4��SiO2���з�����Ҫ�������£�
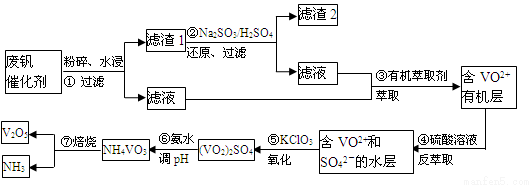
��֪����1��V2O5��NH4VO3��Ϊ�����VOSO4��(VO2)2SO4��Ϊ�����
��2�� VO2++H2C2O4+H+ �� VO2+ + CO2��+ H2O
�ش��������⣺
��1������ڵ�Ŀ���� ��
��2������۵ı仯���̿ɼ�Ϊ(HA��ʾ�л���ȡ��)��
VOSO4 (ˮ��)+ 2HA���л��㣩 VOA2(�л��㣩+ H2SO4(ˮ��)��������п�ѡ������������ȡ��ԭ���� ��
VOA2(�л��㣩+ H2SO4(ˮ��)��������п�ѡ������������ȡ��ԭ���� ��
��3����ClO3-������ԭΪCl-,��д������з�����Ӧ�����ӷ���ʽΪ ��
��4���������ữ��H2C2O4��Һ�ζ�(VO2)2SO4��Һ���Բⶨ�����ݺ���Һ�к������IJ���Ϊ��ȡ10.0mL0.1mol/LH2C2O4��Һ����ƿ�У�����ָ�����������Һʢ���ڵζ����У��ζ����յ�ʱ�����Ĵ���Һ�����Ϊ10.00mL���ɴ˿�֪(VO2)2SO4��Һ��Ԫ�صĺ���Ϊ g/L��
��5��V2O5���ý���(��Ca��Al)�Ȼ�ԭ����÷�����������Ȼ�ԭ�Ƶ÷��Ļ�ѧ����ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�켪��ʡ�����ϵ�����ģ�⿼�����ۻ�ѧ�Ծ��������棩 ���ͣ�ʵ����
����ѧ����ѡ��2����ѧ�뼼����
����п�̸ɵ�����й�������ȣ���������뻷�����������Σ����ij��ѧ��ȤС����������´����������շϵ���еĸ�����Դ��
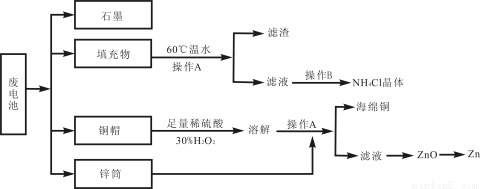
��1���������60����ˮ�ܽ⣬Ŀ���� ��
��2������A������Ϊ ��
��3��ͭñ�ܽ�ʱ����H2O2��Ŀ���� ���û�ѧ����ʽ��ʾ����ͭñ�ܽ���ȫ�ɲ���_________������ȥ��Һ�й�����H2O2��
��4������п�̸ɵ�ص����ΪKOH���ܷ�ӦZn+2MnO2+2H2O=2MnOOH+Zn(OH)2���为���ĵ缫��ӦʽΪ ��
(5)��������Ҫ�ɷ�Ϊ���̻������̻�����м���һ������ϡ���ᡢϡ���ᣬ�����Ͻ�����������Ϊֹ����Ҫ��ӦΪ2MnO(OH)+MnO2+2H2C2O4+3H2SO4=3MnSO4+4CO2��+6H2O��
�ٵ�1 mol MnO2�μӷ�Ӧʱ������ mol���ӷ���ת�ơ�
��MnO(OH)��Ũ�����ڼ���������Ҳ�ɷ�����Ӧ����д����Ӧ�Ļ�ѧ����ʽ�� ��
��6��п�̸ɵ�������Ĺ�����KMnO4��Һ���ա��ڲ�ͬpH�£�KMnO4��Һ��Hg�������ʼ���Ҫ��������ͼ��ʾ��
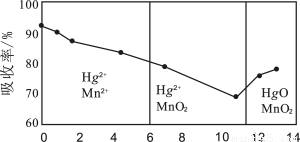
������ͼ��֪��
��pH��Hg�����ʵ�Ӱ���������pH���ߣ����������� ��
����ǿ���Ի�����Hg�������ʸߵ�ԭ�������KMnO4������������ ǿ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com