
【题目】高炉炼铁是冶炼铁的主要方法。
(1)从炼铁高炉口排出的尾气中含有一定量的有毒气体___(填化学式),会污染空气。100多年前,人们曾耗巨资改建高炉,结果尾气中的该物质含量并未减少。高炉炼铁的主要反应方程式为(设铁矿石用磁铁矿)____。
(2)已知:①4Fe(s) + 3O2=2Fe2O3(s) ΔH1
②4Fe3O4(s)+O2(g)=6Fe2O3(s) ΔH2
③3Fe(s)+2O2(g)=Fe3O4(s) ΔH3
则ΔH2=___(用含上述ΔH的代数式表示)。
(3)高铁酸钠(Na2FeO4)是铁的一种重要化合物,可用电解法制备,阳极材料为铁,其电解质溶液应选用___(填H2SO4、HNO3、KOH、NaOH、Na2SO4)溶液,阳极反应式为___。
(4)某温度下,HX的电离平衡常数K=1×10-5。则该温度下0.100mol/L的HX溶液中c(H+)=___(平衡时HX的浓度以0.100mol/L计,水的电离忽略不计。)
【答案】CO Fe3O4(s)+4CO(g)![]() 3Fe(s)+4CO2(g) 3ΔH1-4ΔH3 NaOH Fe-6e-+ 8OH-= FeO42-+ 4H2O 1×10-3mol·L-1
3Fe(s)+4CO2(g) 3ΔH1-4ΔH3 NaOH Fe-6e-+ 8OH-= FeO42-+ 4H2O 1×10-3mol·L-1
【解析】
(1)高炉炼铁,原料是铁矿和焦炭,先加焦炭,让焦炭转化成CO,然后加入铁矿石,CO还原铁的氧化物,得到铁单质,为了提高氧化铁的利用率,CO一定过量,即尾气中有毒的气体为CO,高炉炼铁的主要反应为4CO+Fe3O4 ![]() 4CO2+3Fe;
4CO2+3Fe;
答案为CO;4CO+Fe3O4 ![]() 4CO2+3Fe;
4CO2+3Fe;
(2)根据盖斯定律,②为目标反应方程式,因此有3×①-4×③,即△H2=3△H1-4△H2;
答案为3△H1-4△H2;
(3)因为制备高铁酸钠,根据电解原理,铁作阳极,即有Fe-6e-→FeO42-,电解质不能是酸,因为铁能与酸反应,因此只能选碱为电解质溶液,KOH不能选择,引入杂质K+,因此电解质溶液为NaOH,根据电荷守恒,有Fe-6e-+8OH-→FeO42-,根据原子守恒,阳极反应式为Fe-6e-+8OH-=FeO42-+4H2O;
答案为NaOH;Fe-6e-+8OH-=FeO42-+4H2O;
(4)根据电离平衡常数的表达式,即HX的电离平衡常数表达式为K=![]() ,HX的电离方程式为HX
,HX的电离方程式为HX ![]() H++X-,因为忽略水的电离,因此c(H+)=c(X-),c(HX)=0.1mol·L-1,电离平衡常数K=
H++X-,因为忽略水的电离,因此c(H+)=c(X-),c(HX)=0.1mol·L-1,电离平衡常数K=![]() =
=![]() =1×10-5,解得c(H+)=1×10-3mol·L-1;
=1×10-5,解得c(H+)=1×10-3mol·L-1;
答案为c(H+)=1×10-3mol·L-1。


 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案科目:高中化学 来源: 题型:
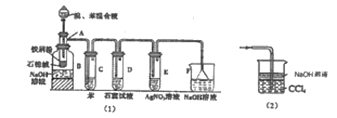
【题目】图(1)是实验室合成溴苯并检验其部分生成物的装置,下列说法错误的是( )
A.苯和液溴在A中发生反应的化学方程式为:![]() +Br2
+Br2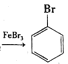 +HBr
+HBr
B.实验中C中的液体逐渐变为浅红色,是因为溴具有挥发性
C.D、E、F均具有防倒吸的作用,其中F不可以用图(2)所示装置代替
D.D中石蕊试液慢慢变红,E中产生浅黄色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,用浓度为0.100 0 mol·L1的NaOH溶液滴定20.00 mL浓度均为0.100 0 mol·L1的三种酸HX、HY、HZ,滴定曲线如图所示。下列说法正确的是
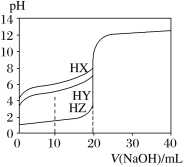
A.在相同温度下,同浓度的三种酸溶液的导电能力顺序:HZ<HY<HX
B.根据滴定曲线可得Ka(HX)的数量级是107
C.HX、HY与HZ溶液中均存在两种平衡
D.HY与HZ混合,达到平衡时c(H+)=![]() +c(Z)+c(OH)
+c(Z)+c(OH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应①CO(g)+CuO(s)![]() CO2(g)+Cu(s)和反应②H2(g)+CuO(s)
CO2(g)+Cu(s)和反应②H2(g)+CuO(s)![]() Cu(s)+H2O(g)在相同的某温度下的平衡常数分别为K1和K2,该温度下反应③CO(g)+H2O(g)
Cu(s)+H2O(g)在相同的某温度下的平衡常数分别为K1和K2,该温度下反应③CO(g)+H2O(g)![]() CO2(g)+H2(g)的平衡常数为K。则下列说法正确的是( )
CO2(g)+H2(g)的平衡常数为K。则下列说法正确的是( )
A. 反应①的平衡常数K1=c(CO2).c(Cu)/c(CO).c(CuO)
B. 反应③的平衡常数K=K1/K2
C. 对于反应③,恒容时,温度升高,H2浓度减小,则该反应的焓变为正值
D. 对于反应③,恒温恒容下,增大压强,H2浓度一定减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知可逆反应:X(s)+aY(g)![]() bZ(g);ΔH,反应达到平衡时,温度、压强对可逆反应的影响如右图所示(图中p为压强,其中p1>p2)。下列有关判断正确的是( )
bZ(g);ΔH,反应达到平衡时,温度、压强对可逆反应的影响如右图所示(图中p为压强,其中p1>p2)。下列有关判断正确的是( )
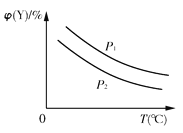
A. 可逆反应的焓变ΔH<0
B. 反应的化学计量数a<b
C. 该可逆反应的平衡常数K=![]()
D. 温度、压强不变,若使用合适的催化剂,可以提高Y的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲胺铅碘(CH3NH3PbI3)用作全固态钙钛矿敏化太阳能电池的敏化剂,可由CH3NH2、PbI2及HI为原料合成,回答下列问题:
(1)制取甲胺的反应为CH3OH(g)+NH3(g)![]() CH3NH2(g)+H2O(g) ΔH。已知该反应中相关化学键的键能数据如下:
CH3NH2(g)+H2O(g) ΔH。已知该反应中相关化学键的键能数据如下:
共价键 | C—O | H—O | N—H | C—N | C—H |
键能/kJ·mol-1 | 351 | 463 | 393 | 293 | 414 |
则该反应的ΔH=____kJ·mol-1。
(2)上述反应中所需的甲醇工业上利用水煤气合成CO(g)+2H2(g)![]() CH3OH(g) ΔH<0。在一定条件下,将1 mol CO和2 mol H2通入密闭容器中进行反应,当改变某一外界条件(温度或压强)时,CH3OH的体积分数φ(CH3OH)变化趋势如图所示:
CH3OH(g) ΔH<0。在一定条件下,将1 mol CO和2 mol H2通入密闭容器中进行反应,当改变某一外界条件(温度或压强)时,CH3OH的体积分数φ(CH3OH)变化趋势如图所示:
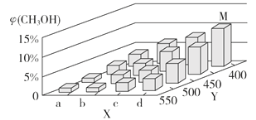
①平衡时,M点CH3OH的体积分数为10%,则CO的转化率为___。
②X轴上a点的数值比b点____ (填“大”或“小”)。某同学认为上图中Y轴表示温度,你认为他判断的理由是_________________。
(3)工业上可采用CH3OH CO+2H2 来制取高纯度的CO和H2。我国学者采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用*标注。
CO+2H2 来制取高纯度的CO和H2。我国学者采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用*标注。
甲醇(CH3OH)脱氢反应的第一步历程,有两种可能方式:
方式 A:CH3OH* →CH3O* +H* Ea= +103.1kJ·mol-1
方式 B:CH3OH* →CH3* +OH* Eb= +249.3kJ·mol-1
由活化能E值推测,甲醇裂解过程主要历经的方式应为___(填A、B)。
下图为计算机模拟的各步反应的能量变化示意图。
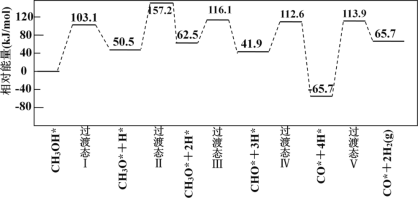
该历程中,放热最多的步骤的化学方程式为________。
(4)PbI2与金属锂以LiI-Al2O3固体为电解质组成锂碘电池,其结构示意图如下,电池总反应可表示为:2Li+PbI2=2LiI+Pb,则b极上的电极反应式为:_____。

(5)CH3NH2的电离方程式为CH3NH2+H2O![]() CH3NH3++OH-电离常数为kb,已知常温下pkb=-lgkb=3.4,则常温下向CH3NH2溶液滴加稀硫酸至c(CH3NH2)=c(CH3NH3+)时,溶液pH=______。
CH3NH3++OH-电离常数为kb,已知常温下pkb=-lgkb=3.4,则常温下向CH3NH2溶液滴加稀硫酸至c(CH3NH2)=c(CH3NH3+)时,溶液pH=______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铬为高效催化剂的主要成分元素,从铬铁矿[主要含Ag2S、Cu2(OH)2CO3、FeO、Cr2O3、SiO2]中提取Cr、Ag的工艺流程如图:
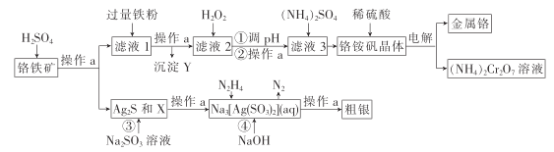
已知:①部分阳离子以氢氧化物开始沉淀和完全沉淀的pH如下表(金属离子浓度为0.01mol·L-1)
沉淀物 | Fe(OH)2 | Fe(OH)3 | Cr(OH)3 |
开始沉淀的pH | 7.6 | 2.7 | 4.9 |
开始沉淀的pH | 9.6 | 3.7 | 6.8 |
②铬铵矾晶体:[NH4Cr(SO4)2·12H2O]
(1)操作a为___;X和Y分别为____、___。
(2)写出加入H2O2发生反应的离子方程式:___。
(3)调节pH值可用的物质的化学式为___,pH值应当控制的范围为__;由滤液3获得铬酸铵晶体的正确操作方法是___、过滤、洗涤、干燥。
(4)将铬铵矾晶体溶于硫酸而不是直接溶于水的主要原因是___。
(5)步骤④发生反应的离子方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】500 ℃条件下,在恒容密闭容器中,充入1 mol NO2存在如下平衡:2NO2(g) ![]() N2O4(g)。平衡后,向容器内再充入1 mol NO2,下列说法正确的是
N2O4(g)。平衡后,向容器内再充入1 mol NO2,下列说法正确的是
A. 平衡向正反应方向移动 B. 平衡常数K增大
C. NO2的转化率变小 D. 容器内气体颜色先变深后变浅,最后比原来还要浅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知充分燃烧a g乙炔气体时生成1 mol二氧化碳气体和液态水,并放出热量b kJ,则乙炔燃烧的热化学方程式正确的是
A. 2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l);△H=+b kJ/mol
B. C2H2(g)+![]() O2(g)=2CO2(g)+H2O(l);△H=+2b kJ/mol
O2(g)=2CO2(g)+H2O(l);△H=+2b kJ/mol
C. 2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l);△H=-2b kJ/mol
D. 2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l);△H=-4b kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com