
【题目】丁苯酞![]() 是治疗轻、中度急性脑缺血的药物,合成J的一种路线如下
是治疗轻、中度急性脑缺血的药物,合成J的一种路线如下

已知:![]()
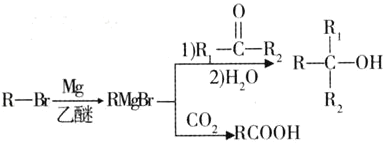
![]() 的核磁共振氢谱只有一组峰;
的核磁共振氢谱只有一组峰;
![]() 能发生银镜反应;
能发生银镜反应;
![]() 是一种酯,分子中除苯环外还含有一个五元环。
是一种酯,分子中除苯环外还含有一个五元环。
![]() 苯环上的卤原子在常压下遇到NaOH的溶液很难水解。
苯环上的卤原子在常压下遇到NaOH的溶液很难水解。
回答下列问题:
![]() 中官能团的名称:________、________。
中官能团的名称:________、________。
![]() 的系统命名是________;J的结构简式为________。
的系统命名是________;J的结构简式为________。
![]() 由A生成B的化学方程式为________,反应类型为________。
由A生成B的化学方程式为________,反应类型为________。
![]() 与新制的氢氧化铜悬浊液反应的化学方程式为________。
与新制的氢氧化铜悬浊液反应的化学方程式为________。
![]() 在一定条件下生成高分子化合物的结构简式为________。
在一定条件下生成高分子化合物的结构简式为________。
![]() 的同分异构体中核磁共振氢谱有4组峰且能与
的同分异构体中核磁共振氢谱有4组峰且能与![]() 溶液发生显色反应,任写出其中两种符合上述条件的同分异构体的结构简式________。
溶液发生显色反应,任写出其中两种符合上述条件的同分异构体的结构简式________。
![]() 由甲醛、化合物A与液溴为原料经下列步骤可得到
由甲醛、化合物A与液溴为原料经下列步骤可得到![]() 苯基乙醇。
苯基乙醇。
![]()
反应条件1为________;反应条件2所选择的试剂为________;L的结构简式为________。
【答案】羟基 溴原子 2-甲基-1-丙烯 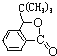
![]()
![]()
![]()

![]() 取代反应
取代反应 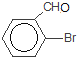
![]()
![]()
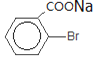
![]()

 光照 镁、乙醚
光照 镁、乙醚 ![]()
【解析】
E的核磁共振氢谱只有一组峰,则E为![]() ,可知D为
,可知D为![]() ,根据信息
,根据信息![]() 可知F为
可知F为![]() ,C能发生银镜反应,由G的结构逆推可知C为
,C能发生银镜反应,由G的结构逆推可知C为 ,则B为
,则B为 ,A为
,A为![]() ;根据题中已知
;根据题中已知![]() ,由G可推知H为
,由G可推知H为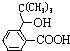 ,J是一种酯,分子中除苯环外,还含有一个五元环,则J为
,J是一种酯,分子中除苯环外,还含有一个五元环,则J为 ,
, 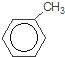 与溴发生取代生成K为
与溴发生取代生成K为 ,K在镁、乙醚的条件下生成L为
,K在镁、乙醚的条件下生成L为 ,L与甲醛反应生成2-苯基乙醇,据此答题。
,L与甲醛反应生成2-苯基乙醇,据此答题。
(1)根据流程图中G的结构简式,![]() 中官能团的名称:羟基、溴原子;
中官能团的名称:羟基、溴原子;
(2)![]() 为
为![]() ,系统命名是:
,系统命名是:![]() 甲基
甲基![]() 丙烯,J的结构简式为:
丙烯,J的结构简式为: ;
;
(3)由A生成B的化学方程式为:![]()
![]()

![]() ,属于取代反应;
,属于取代反应;
(4)![]() 与新制的氢氧化铜悬浊液反应的化学方程式:
与新制的氢氧化铜悬浊液反应的化学方程式:
![]()
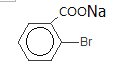
![]() ;
;
(5)![]()
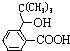
![]() 在一定条件下生成高分子化合物的结构简式为:
在一定条件下生成高分子化合物的结构简式为: ;
;
(6)![]() 的同分异构体中核磁共振氢谱有4组峰,且能与
的同分异构体中核磁共振氢谱有4组峰,且能与![]() 溶液发生显色反应,说明含有酚羟基,可能结构简式为:
溶液发生显色反应,说明含有酚羟基,可能结构简式为:
 ;
;
(7)由信息![]() 中的转化可知,甲苯与溴在光照条件下得到
中的转化可知,甲苯与溴在光照条件下得到![]() ,再与
,再与![]() 乙醚反应得到
乙醚反应得到![]() ,最后与HCHO反应、水解得到
,最后与HCHO反应、水解得到![]() 苯基乙醇,L的结构简式为
苯基乙醇,L的结构简式为![]() 。
。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】A、B、C、D是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,己是由C元素形成的单质,已知甲+乙=丁+己,甲+丙=戊+己,0.1mol·L-1丁溶液的pH为13(25℃)。下列说法正确的是
A. 原子半径:D>C >B>A
B. B元素只能形成一种二元含氧酸,且B元素的含氧酸对应的酸酐一定是氧化物
C. 1mol甲与足量乙反应转移电子的数目为NA
D. 1.0L 0.1mol·L-1戊溶液中阴离子总的物质的量小于0.1mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,向a L密闭容器中加入1molX气体和2 molY气体,发生如下反应:X(g) + 2Y(g)![]() 2Z(g)此反应达到平衡的标志是
2Z(g)此反应达到平衡的标志是
A.容器内压强不随时间变化
B.容器内各物质的浓度完全相同
C.容器内X、Y、Z的浓度之比为1∶2∶2
D.单位时间消耗0.1molX同时生成0.2molZ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A是制备血管紧张素抑制剂卡托普利的原料,其核磁共振氢谱图中有3个吸收峰,吸收峰的面积比为![]() ,已知B的结构中只有一个甲基,下图是以B为主要原料的合成路线。试回答下列问题:
,已知B的结构中只有一个甲基,下图是以B为主要原料的合成路线。试回答下列问题:
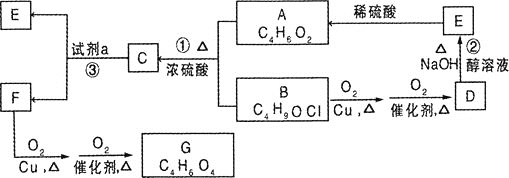
(1)![]() 的名称是________,D含有的官能团名称是________。
的名称是________,D含有的官能团名称是________。
(2)写出反应![]() 的化学方程式:________,该反应的反应类型是________,反应
的化学方程式:________,该反应的反应类型是________,反应![]() 的反应类型是________。
的反应类型是________。
(3)反应![]() 中的试剂a是:________;
中的试剂a是:________;
(4)写出G的结构简式:________;
(5)![]() 的同分异构体有多种,能发生水解反应的有________种,写出其中既能发生水解反应,又能发生银镜反应的有机物的结构简式:________。
的同分异构体有多种,能发生水解反应的有________种,写出其中既能发生水解反应,又能发生银镜反应的有机物的结构简式:________。![]() 写出一种即可
写出一种即可![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某一容积为2 L的密闭容器中加入0.6molH2O(g)和0.4molCO,在一定条件下发生如下反应:CO(g) + H2O(g )![]() CO2(g) + H2(g)
CO2(g) + H2(g)
(1)若反应2min后,容器中CO仅剩0.2mol,则0~2min间CO的平均反应速率为___。
(2)该反应为放热反应,若升高温度,化学反应速率___;CO的转化率___。(填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上从电解精炼铜的阳极泥(成分为CuS、Cu2Se、Cu2Te 和少量金属单质Au) 中回收碲、硒的工艺流程如下:

已知:①TeO2是两性氧化物。
②Se和TeO2的物理性质如下:
物理性质 | 熔点 | 沸点 | 水溶性 |
Se | 221℃ | 685℃ | 难溶于水 |
TeO2 | 733℃ | 1260℃ | 微溶于水 |
(1)Se在周期表中的位置为____________。
(2)SeO2与SO2的混合烟气可用水吸收制得单质Se,当有2 mol电子转移时,会生成______mol Se。过滤所得粗硒可采用真空蒸馏的方法提纯获得纯硒,采用真空蒸馏的目的是_______________。
(3)“碱浸”过滤得到滤渣的主要成分是_______(填化学式)。
(4)“沉碲”时控制溶液的pH为4.5-5.0,生成TeO2沉淀。如果H2SO4的浓度过大,将导致“沉碲”不完全,原因为_______________________________________。
(5)“酸溶”将TeO2先溶于硫酸得到Te(SO4)2,然后加入Na2SO3溶液进行还原,还原碲的离子反应方程式是_______________________________________。
(6)常温下,SeO2与NaOH溶液反应所得NaHSeO3溶液的pH______7(填“>”“<”或“=”),请通过计算说明_____________________________。(已知25℃时,亚硒酸(H2SeO3)的Ka1=2.5×10-3,Ka2=2.5×10-7)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】热化学方程式C(s)+H2O(g) ![]() CO(g)+H2(g);△H =+131.3kJ/mol表示( )
CO(g)+H2(g);△H =+131.3kJ/mol表示( )
A. 碳和水反应吸收131.3kJ能量
B. 1mol碳和1mol水反应生成一氧化碳和氢气并吸收131.3kJ热量
C. 1mol固态碳和1mol水蒸气完全反应生成一氧化碳气体和氢气,并吸热131.3kJ热量
D. 1个固态碳原子和1分子水蒸气反应吸热131.1kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() (环戊二烯)容易发生聚合生成二聚体,该反应为可逆反应。不同温度下,溶液中环戊二烯浓度与反应时间的关系如图所示,下列说法不正确的是( )
(环戊二烯)容易发生聚合生成二聚体,该反应为可逆反应。不同温度下,溶液中环戊二烯浓度与反应时间的关系如图所示,下列说法不正确的是( )

A.T1小于T2
B.a点的反应速率小于c点的反应速率
C.a点的正反应速率大于b点的逆反应速率
D.b点时二聚体的浓度为0.45 mol·L1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20mL 0.1mol/L氨水中滴加一定浓度的稀盐酸,溶液中由水电离的氢离子浓度随加入盐酸体积的变化如图所示。则下列说法正确的是( )
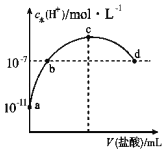
A.常温下,0.1 mol/L氨水中,c (OH﹣)=1×10﹣5 mol/L
B.b点代表溶液呈中性
C.c点溶液中c(NH4+)=c(Cl﹣)
D.d点溶液中:c(Cl﹣)>c(NH4+)>c(OH﹣)>c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com