
【题目】用下列实验装置进行有关实验,能达到实验目的的是

A. 用装置甲制取少量SO2
B. 用装置乙蒸发FeCl3溶液制取FeCl3晶体
C. 用装置丙分离CH3COOH和CH3COOCH2CH3的混合液
D. 用装置丁除去Cl2中混有的少量HCl气体
科目:高中化学 来源: 题型:
【题目】从葡萄籽中提取的原花青素结构为:有关原花青素的下列说法不正确的( )
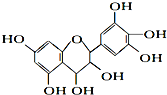
A.该物质既可看作醇类,也可看作酚类
B.1mol该物质可与4mol Br2反应
C.1mol该物质可与7mol Na反应
D.1mol该物质可与7mol NaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列各组微粒:
A.12C和14C B.O2和O3
C.H、D、T D.金刚石和石墨
E.CH3OH和![]()
F. 和
和![]()
用序号填空:
(1)互为同位素的是______;
(2)互为同素异形体的是______;
(3)互为同分异构体的是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:

(1)在这些元素中,化学性质最不活泼的是______(填元素符号,下同)。
(2)从①到③的元素中,非金属性最强的是_____。
(3)在最高价氧化物的水化物中,酸性最强的化合物的化学式是______,碱性最强的化合物的电子式是______。
(4)最高价氧化物是两性氧化物的元素是______;写出它的最高价氧化物与氢氧化钠反应的离子方程式______________________。
(5)用结构式表示元素①与③形成的一种可溶于水的化合物_____,该化合物的常见固体是______晶体。
(6)写出元素④的单质与水反应的化学方程式_________________。
(7)写出元素①的单质和元素⑥最高价氧化物对应水化物的浓溶液反应的化学方程式_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示________,K值大小与温度的关系是:温度升高,K值_______。(填增大、减小、不变、或可能增大也可能减小)。
(2)在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:CO(g) + H2O(g) ![]() CO2(g) + H2(g) △H<0,CO和H2O浓度变化如下图,则0~4min的平均反应速率v(CO)= mol·L-1·min-1。
CO2(g) + H2(g) △H<0,CO和H2O浓度变化如下图,则0~4min的平均反应速率v(CO)= mol·L-1·min-1。

(3 )t℃(高于850℃ ),在相同容器中发生上述反应,容器内各物质变化如下表。

①表中3 min~4 min之间反应________(达到平衡,正向进行,逆向进行);C1数值________0.08 mol·L-1(填大于、小于或等于)。
②反应在4 min~5 min问,平衡向逆方向移动,可能的原因是________(单选),表中5 min~6 min之间数值发生变化,可能的原因是________(单选).
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在与Al反应能放出H2的无色溶液中,一定能大量共存的离子组是
①K+、Cl-、NO3-、S2- ②K+、Fe2+、I-、SO42-③Na+、Cl-、NO3-、SO42- ④Na+、Ca2+、Cl-、HCO3- ⑤K+、Ba2+、Cl-、NO3-
A.①③B.③⑤C.③④D.②⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2和氮氧化物的转化和综合利用既有利于节约资源,又有利于保护环境。
⑴H2还原法是处理燃煤烟气中SO2的方法之一。已知:
2H2S(g)+SO2(g)=3S(s)+2H2O(l) ΔH=a kJ·mol—1
H2S(g)= H2(g)+S(s) ΔH=b kJ·mol—1
H2O(l)= H2O(g) ΔH=c kJ·mol—1
写出SO2(g)和H2(g)反应生成S(s)和H2O(g)的热化学方程式:_____________。
⑵20世纪80年代Townley首次提出利用电化学膜脱除烟气中SO2的技术:将烟气预氧化使SO2转化为SO3,再将预氧化后的烟气利用如图所示原理净化利用。
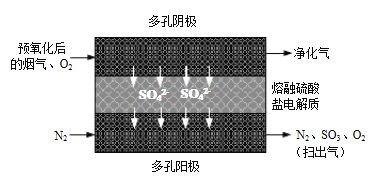
①阴极反应方程式为_____________。
②若电解过程中转移1mol电子,所得“扫出气”用水吸收最多可制得质量分数70%的硫酸_____________g。
⑶利用脱氮菌可净化低浓度NO废气。当废气在塔内停留时间均为90s的情况下,测得不同条件下NO的脱氮率如图Ⅰ、Ⅱ所示。
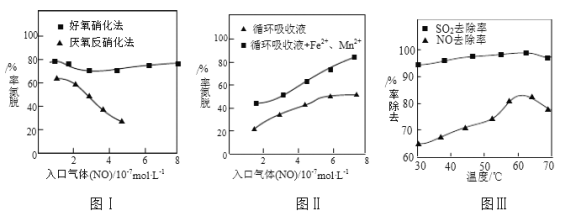
①由图I知,当废气中的NO含量增加时,宜选用____________法提高脱氮效率。
②图Ⅱ中,循环吸收液加入Fe2+、Mn2+提高了脱氮的效率,其可能原因为_____________。
⑷研究表明:NaClO2/H2O2酸性复合吸收剂可同时有效脱硫、脱硝。图Ⅲ所示为复合吸收剂组成一定时,温度对脱硫脱硝的影响。
①温度高于60℃后,NO去除率随温度升高而下降的原因为_____________。
②写出废气中的SO2与NaClO2反应的离子方程式:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国自主研发的新一代动车组在京沪高铁上跑出过486.1公里的世界列车最高时速,这得益于全路铺设的优质无缝平滑的超长钢轨。下列有关说法不正确的是
A. 制造钢轨的材料是钢,钢是用量最大的合金
B. 钢的熔点比铁的熔点高,而铁的用途更广泛
C. 我国在商代就开始使用铜合金
D. 铝合金的强度、硬度比组成合金各成分金属的大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com