
ClO2与Cl2的氧化性相近,在自来水消毒和果蔬保鲜等方而应用广泛。某兴趣小组通过题9图1 装置(夹持装置略)对其制备、吸收、释放和应用进行了研究。
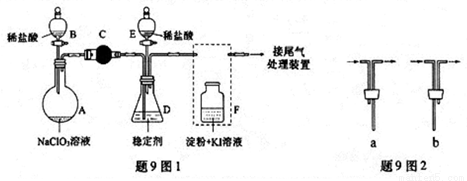
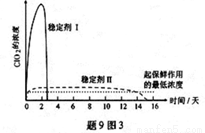
(1)仪器D的名称是_______。安装F中导管时,应选用题9图2中的______打开B的活塞,A中发生反应:2NaClO3+ 4HCl=2ClO2↑+ Cl2↑+ 2NaCl+ 2H2O
(2)为使ClO2在D中被稳定剂充分吸收,滴加稀盐酸的速度宜___(填“快”或“慢”)。
(3)关闭B的活塞,ClO2在D中被稳定剂完全吸收生成NaClO2,此时F中溶液的颜色不变,
则装置C的作用是_________________。
(4)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为:___________,在ClO2释放实验中,打开E的活塞,D中发生反应,则装置F的作用是______。
(5)已吸收ClO2气体的稳定剂I和稳定剂Ⅱ,加酸后释放ClO2的浓度随时间的变化如题9图3所示。若将其用于水果保鲜,你认为效果较好的稳定剂是________,原因是__________。
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源:2016-2017学年河北省高二上9月调研化学试卷(解析版) 题型:实验题
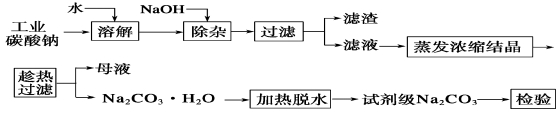
碳酸钠是造纸、玻璃、纺织、制革等行业的重要原料。工业碳酸钠(纯度约98%)中含有Ca2+、Mg2+、Fe3+、Cl-和SO42-等杂质,提纯工艺流程如下:
已知碳酸钠的溶解度(S)随温度变化的曲线如下图所示:
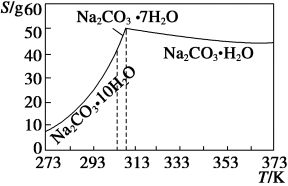
回答下列问题:
(1)滤渣的主要成分为_______________________________。
(2)“趁热过滤”的原因是___________________________。
(3)若在实验室进行“趁热过滤”,可采取的措施是_____(写出一种)。
(4)已知:Na2CO3·10H2O (s)===Na2CO3(s)+10H2O(g) ΔH1= +532.36 kJ·mol-1
Na2CO3·10H2O(s)===Na2CO3·H2O(s)+9H2O(g) ΔH2= +473.63 kJ·mol-1
写出Na2CO3·H2O脱水反应的热化学方程式____________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高一上开学测化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.向某固体上滴加稀盐酸,有气泡产生,则该固体一定是碳酸盐
B.把燃着的木条插入某瓶无色气体中,木条熄灭,证明瓶中的气体是二氧化碳
C.取少量溶液于试管中,滴加氯化钡溶液,有白色沉淀生成,证明该溶液中一定有硫酸根离子
D.不用任何试剂就可以把KOH、HN03、CuSO4、MgCl2四种溶液鉴别出来
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高二上开学测化学试卷(解析版) 题型:选择题
铜和镁的合金2.14g完全溶于一定浓度的硝酸,若反应中硝酸被还原为NO2、NO、N2O三种气体而且在标准状况下它们的体积均为0.224 L。在反应后的溶液中,加入足量的氢氧化钠溶液,生成的沉淀经过滤、洗涤、低温干燥后称量,质量为( )
A.4.18g B.3.12g C.4.68g D.5.08g
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高二上开学测化学试卷(解析版) 题型:选择题
下列有关物质性质和应用的说法正确的是( )
A.碳酸钠受热易分解,可用于生产食品发酵粉
B.次氯酸钠具有强氧化性,可用于配制消毒液
C.二氧化硅不与强酸反应,可用石英玻璃容器盛放氢氟酸
D.二氧化硫有漂白、杀菌性能,可在食品生产中大量使用
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高二上开学测化学试卷(解析版) 题型:选择题
根据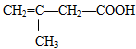 的结构,它不可能发生的反应是( )
的结构,它不可能发生的反应是( )
A.使溴的四氯化碳溶液褪色
B.与银氨溶液反应析出银
C.与乙醇在浓硫酸催化下发生酯化反应
D.与新制氢氧化铜反应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高二上开学测化学试卷(解析版) 题型:选择题
部分短周期元素的有关信息如图表所示
元素代号 | 元素性质或原子结构 |
T | 第二层上的电子数是第一层的3倍 |
R | 与T 同一族 |
L | L2+与T2-的核外电子数相等 |
Z | 元素最高正价是+3价,与L同周期 |
根据表中信息,判断以下叙述正确的是( )
A.氢化物的稳定性为H2T<H2R
B.单质与稀盐酸反应的速率为L<Z
C.Z与T形成的化合物具有两性
D.L与R通过离子键形成的化合物阴阳离子的核外电子数相等
查看答案和解析>>
科目:高中化学 来源:2017届湖北省高三上9月调考化学试卷(解析版) 题型:选择题
还原沉淀法是处理含铬(含Cr2O72-和CrO42-)工业废水的常用方法,过程如下: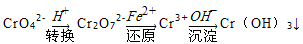 ,已知转化过程中的反应为2CrO42-(aq)+2H+(aq)
,已知转化过程中的反应为2CrO42-(aq)+2H+(aq) Cr2O72-(aq)+H2O(1)。转化后所得溶液中铬元素的含量为28.6g/L, CrO42-有10/11转化为Cr2O72-,下列说法不正确的是
Cr2O72-(aq)+H2O(1)。转化后所得溶液中铬元素的含量为28.6g/L, CrO42-有10/11转化为Cr2O72-,下列说法不正确的是
A.溶液颜色保持不变,说明上述可逆反应达到平衡状态
B.若用绿矾(FeSO4·7H2O)作还原剂,处理1 L废水,至少需要458.7g
C.常温下转化反应的平衡常数K=1×1014,则转化后所得溶液的pH=5
D.常温下Ksp=1×10-32,要使处理后废水中的c(Cr3+)降至1×10-5mol/L,应调溶液的pH=5
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上第一次月考化学试卷(解析版) 题型:选择题
某化学小组用右图所示装置验证卤素单质氧化性的相对强弱。下列说法不正确的是( )
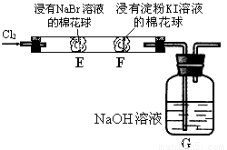
A.E处棉花球变成黄色,说明Cl2的氧化性比Br2强
B.F处棉花球变成蓝色,说明Br2的氧化性比I2强
C.E处发生反应的离子方程式为:Cl2+ 2Br-=2Cl-+ Br2
D.G装置中NaOH溶液与Cl2反应的离子方程式为:2OH- + Cl2 = ClO-+ Cl-+ H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com