
| A. | 某温度时,KW=10-12,此温度下PH=6的溶液一定显酸性 | |
| B. | 25℃时,0.1mol/L的NaHSO3溶液pH=4,说明HSO3-在水溶液中只存在电离 | |
| C. | NH4Cl、CH3COONa、NaHCO3、NaHSO4溶于水,对水的电离都有促进作用 | |
| D. | 稀释 0.1mol/L CH3COONa溶液过程中,c(OH-)/c(CH3COO-)增大 |
分析 A.100℃时,KW=10-12,纯水呈中性,c(H+)=c(OH-)=1×10-6mol/L,此温度下PH=6的溶液中:c(H+)=c(OH-)=1×10-6mol/L,该溶液一定为中性;
B.25℃时,0.1mol/L的NaHSO3溶液pH=4,溶液显示酸性,亚硫酸是弱酸,说明HSO3-在水溶液中的电离程度大于其水解程度;
C.NaHSO4溶于水电离出大量的氢离子,抑制了水的电离;
D.醋酸钠溶液中醋酸根离子水解,溶液显碱性,加水稀释促进平衡正向进行,平衡状态下离子浓度减小,溶液中存在离子积常数,氢离子浓度减小,氢氧根离子浓度增大;
解答 解:A.水的离子积KW=10-12,纯水中c(H+)=c(OH-)=1×10-6mol/L,此温度下PH=6,溶液显示中性,故A错误;
B.25℃时,0.1mol/L的NaHSO3溶液pH=4,溶液显酸性,亚硫酸是弱酸,说明HSO3-在水溶液中的电离程度大于亚硫酸氢根离子的水解程度,溶液显示酸性,故B错误;
C.NH4Cl、CH3COONa、NaHCO3对水的电离都有促进作用,而NaHSO4溶于水会电离出氢离子,抑制了水的电离,故C错误;
D.醋酸钠溶液中醋酸根离子水解,溶液显碱性,CH3COO-+H2O?CH3COOH+OH-,加水稀释促进平衡正向进行,平衡状态下离子浓度减小,溶液中存在离子积常数,氢离子浓度减小,氢氧根离子浓度增大,醋酸根离子浓度减小,$\frac{c(O{H}^{-})}{c(C{H}_{3}CO{O}^{-})}$增大,故D正确;
故选D.
点评 本题考查了水的电离及其电离平衡影响因素、盐的水解等知识,题目难度中等,注意判断溶液酸碱性时,要根据溶液中氢离子与氢氧根离子的浓度大小进行判断,选项D为易错点,注意水溶液中的离子积常数的应用.


科目:高中化学 来源: 题型:解答题

 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol氢气完全燃烧生成液态水放出的热量小于241.8KJ | |
| B. | 1mol水蒸气完全分解成氢气与氧气,需吸收241.8kJ热量 | |
| C. | 2mol氢气与1mol氧气的总能量小于2mol 水蒸气的总能量 | |
| D. | 2mol氢氢键和1mol氧氧键拆开所消耗的能量大于4mol氢氧键成键所放出的能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用酒精清洗做过碘升华的烧杯 | |
| B. | 用水清洗做过银镜反应的试管 | |
| C. | 用浓盐酸清洗做过高锰酸钾分解实验的试管 | |
| D. | 用氢氧化钠溶液清洗盛过苯酚的试管 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
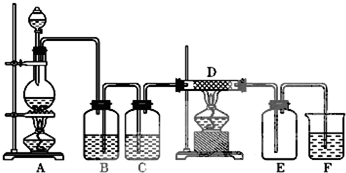
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等质量的乙烯和丙烯中含有的共用电子对数 | |
| B. | 等物质的量的水与重水含有的中子数 | |
| C. | 同温、同压、同体积的CO和NO含有的质子数 | |
| D. | 等物质的量的铁和铝分别与足量盐酸完全反应时转移的电子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com