
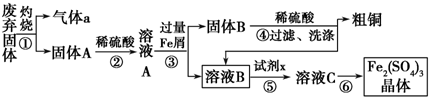
���� ����������Ҫ�ɷ�Cu2S��Fe2O3�����շ������巢����ӦCu2S+2O2$\frac{\underline{\;����\;}}{\;}$SO2+2CuO����������a��SO2������A��CuO��Fe2O3������A��ϡ�����ϣ������ķ�ӦΪCuO+H2SO4=CuSO4+H2O��Fe2O3+3H2SO4=Fe2��SO4��3+3H2O��������ҺA�гɷ�ΪCuSO4��Fe2��SO4��3������ҺA�м������Feм��������ӦCuSO4+Fe=FeSO4+Cu��2Fe2��SO4��3+Fe=3FeSO4�����Թ���B�ɷ���Fe��Cu����ҺB�ɷ�ΪFeSO4������B��ϡ�����ϣ�Fe��ϡ���ᷴӦ����FeSO4��Cu��ϡ�����Ӧ�����˵õ������ͭ��
����ҺB�м����Լ�X�õ���ҺC������ҺCŨ���ᾧ�õ����������壬��ҺB�гɷ���FeSO4����Ҫ����������˫��ˮ��FeSO4����Ϊ�������������Լ�x��H2O2��
��1���۵�ʵ������ǹ��ˣ�
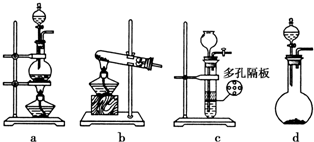
��2�������ڡ����о�����ϡ������м�������������Ԣۢܲ�������H2���ɣ�ʵ������Zn��ϡ���ᷴӦ��ȡ��������Һ��Ӧ����Ҫ���ȣ�cd���ɣ�
��3��Fe2+�ڿ��������ױ���������Fe3+����KSCN��Һ�����Ժ�ɫ��
��4��Cl2��KMnO4��Fe2+��Ӧ��������µ����ʣ���������Ϊ��ɫ��������
��5������ҺCŨ���ᾧ�õ����������壮
��� �⣺��1������������Ҫ�ɷ�Cu2S��Fe2O3�����շ������巢����ӦCu2S+2O2$\frac{\underline{\;����\;}}{\;}$SO2+2CuO����������a��SO2������A��CuO��Fe2O3������A��ϡ�����ϣ������ķ�ӦΪCuO+H2SO4=CuSO4+H2O��Fe2O3+3H2SO4=Fe2��SO4��3+3H2O��������ҺA�гɷ�ΪCuSO4��Fe2��SO4��3������ҺA�м������Feм��������ӦCuSO4+Fe=FeSO4+Cu��2Fe2��SO4��3+Fe=3FeSO4�������۷��������Թ������Һ�����Ըò����ǹ��ˣ�����B�ɷ���Fe��Cu����ҺB�ɷ�ΪFeSO4����ʵ��������õ��IJ����������ձ�����������©����
�ʴ�Ϊ���ձ���©������������
��2���ۢܲ����л���һ���������ɣ�������������������ʵ�����Ʊ������壬������п��ϡ���ᷴӦ��ȡ���÷�Ӧ�ķ�Ӧ��Ϊ��Һ��ϡ�����Ҫ���ȣ�����Ӧ��ѡȡ��Һ��ϲ�������װ�ã����Կ�ѡ��cdװ�ã�
�ʴ�Ϊ��cd��
��3����ҺB�гɷ���FeSO4��FeSO4���ȶ����ױ��������������������������Ӻ�KSCN��Һ��Ӧ������������軯����������Һ��Ѫ��ɫ�����Կ�����KSCN��Һ�������������Ƿ���ʣ�����鷽���ǣ�ȡ������Һ�����Թ��У����Թ��м��뼸��KSCN��Һ�������Һ��ΪѪ��ɫ��˵�����������ӣ����������ӣ�
�ʴ�Ϊ��ȡ������ҺB���Թ��У�����KSCN��Һ���Ƿ��Ϊ��ɫ�������Ϊ��ɫ��֤������Fe3+����ԭ��Һ�ѱ��ʣ�
��4����ҺB��ϡ�����ữ���ǿ������x���ҷ�Ӧ���ܲ������ʣ�������������ܽ�������������Ϊ�����ӣ��������µ����ʣ�˫��ˮ������������Ӧ������������ˮ���������µ����ʣ���ѡb��˫��ˮ���������ԣ��ܽ�������������Ϊ����������������ԭΪˮ�������Լ�x����������������ҺB��Ӧ�����ӷ���ʽΪ��2Fe2++H2O2 +2H+=2Fe3++2H2O��
�ʴ�Ϊ��b��2Fe2++H2O2 +2H+=2Fe3++2H2O��
��5������ҺC������Ũ������ȴ�ᾧ�����˵Ȳ����ɵ�Fe2��SO4��3���壬
�ʴ�Ϊ������Ũ������ȴ�ᾧ��
���� ���⿼������ķ�����ᴿ�����ؿ���ѧ���������⡢ʵ�������˼ά�����Ե���������ȷ���ʵ������ǽⱾ��ؼ����ܴ������Ϸ����������跢���ķ�Ӧ������ȷ��д��Ӧ�Ļ�ѧ����ʽ�����ӷ���ʽ����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaCl��HCl��H2O��NaOH | B�� | Cl2��Na2S��HCl��SO2 | ||
| C�� | Na2O2��H2O2��H2O��O3 | D�� | HBr��CO2��H2O��CS2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ������
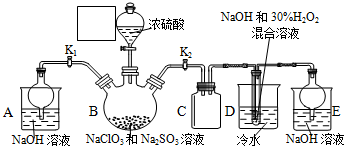
������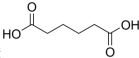 ��һ�ֹ�ҵ�Ͼ�����Ҫ������л���Ԫ�ᣬ�ڻ����������л��ϳɹ�ҵ��ҽҩ��������ȷ��涼����Ҫ���ã��ܹ��������η�Ӧ��������Ӧ�ȣ��������Ԫ�����۳ɸ߷��Ӿۺ���ȣ���������������ж�Ԫ�����еĵڶ�λ��ʵ���Һϳɼ�����ķ�Ӧԭ����ʵ��װ��ʾ��ͼ��ͼ��
��һ�ֹ�ҵ�Ͼ�����Ҫ������л���Ԫ�ᣬ�ڻ����������л��ϳɹ�ҵ��ҽҩ��������ȷ��涼����Ҫ���ã��ܹ��������η�Ӧ��������Ӧ�ȣ��������Ԫ�����۳ɸ߷��Ӿۺ���ȣ���������������ж�Ԫ�����еĵڶ�λ��ʵ���Һϳɼ�����ķ�Ӧԭ����ʵ��װ��ʾ��ͼ��ͼ��
| ���� | �ܶȣ�20�棩 | �۵� | �е� | �ܽ��� | ��Է������� |
| ������ | 0.962g/cm3 | 25.9�� | 160.8�� | 20��ʱˮ���ܽ��3.6g���ɻ������Ҵ����� | 100 |
| ������ | 1.36g/cm3 | 152�� | 337.5�� | ��ˮ�е��ܽ�ȣ�15��ʱ1.44g��25��ʱ2.3g���������Ҵ��������ڱ� | 146 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
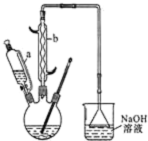
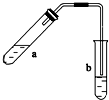 ����ͼʾװ����ȡ������������������ͼ�о�����ȥ��������գ�
����ͼʾװ����ȡ������������������ͼ�о�����ȥ��������գ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
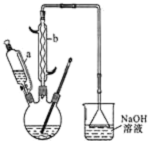
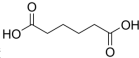 ��һ�ֹ�ҵ�Ͼ�����Ҫ������л���Ԫ�ᣬ�ڻ����������л��ϳɹ�ҵ��ҽҩ��������ȷ��涼����Ҫ���ã��ܹ��������η�Ӧ��������Ӧ�ȣ��������Ԫ�����۳ɸ߷��Ӿۺ���ȣ���������������ж�Ԫ�����еĵڶ�λ��ʵ���Һϳɼ�����ķ�Ӧԭ����ʵ��װ��ʾ��ͼ��ͼ��
��һ�ֹ�ҵ�Ͼ�����Ҫ������л���Ԫ�ᣬ�ڻ����������л��ϳɹ�ҵ��ҽҩ��������ȷ��涼����Ҫ���ã��ܹ��������η�Ӧ��������Ӧ�ȣ��������Ԫ�����۳ɸ߷��Ӿۺ���ȣ���������������ж�Ԫ�����еĵڶ�λ��ʵ���Һϳɼ�����ķ�Ӧԭ����ʵ��װ��ʾ��ͼ��ͼ��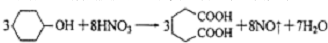
| ���� | �ܶȣ�20�棩 | �۵� | �е� | �ܽ��� | ��Է������� |
| ������ | 0.962g/cm3 | 25.9�� | 160.8�� | 20��ʱˮ���ܽ��3.6g���ɻ������Ҵ����� | 100 |
| �Ҷ��� | 1.36g/cm3 | 152�� | 337.5�� | ��ˮ�е��ܽ�ȣ�15��ʱ��1.44g��25��ʱ2.3g���������Ҵ��������ڱ� | 146 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
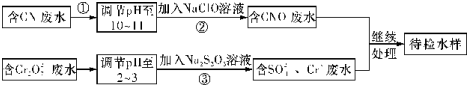
 ��ͼ��һ����ѧ���̵�ʾ��ͼ������ݸ�ʾ��ͼ���������Ŀ��
��ͼ��һ����ѧ���̵�ʾ��ͼ������ݸ�ʾ��ͼ���������Ŀ���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com