
| A. | C4H10和C20H42 | B. | 邻二甲苯和对二甲苯 | ||
| C. | C4H8O2和C3H6O2 | D. | 一溴乙烷和1,2-二溴乙烷 |
分析 结构相似,在分子组成上相差一个或若干个CH2原子团的物质互称为同系物,同系物的官能团以及官能团的数目必须相同.
解答 解:A.C4H10和C20H42都属于烷烃,是同系物,故A符合;
B.邻二甲苯和对二甲苯的分子式相同,结构不同,属于同分异构体,故B不符合;
C.C4H8O2和C3H6O2的官能团不一定相同,若一个含有酯基,另一个含有羧基,则不是同系物,若官能团相同,则是同系物,故C不符合;
D.一溴乙烷和1,2-二溴乙烷,含有的Br原子数目不同,即官能团的个数不同,不是同系物,故D不符合.
故选A.
点评 本题考查同系物的概念与判断,难度不大,注意把握概念的内涵与外延,侧重于考查学生的分析能力和应用能力.


 导学教程高中新课标系列答案
导学教程高中新课标系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 阳离子 | Al3+、Fe2+、Ba2+、Na+、NH4+ |
| 阴离子 | Cl-、CO32-、SO42-、NO3-、I- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 某化学学习小组利用下列药品和实验装置测定镁铝合金中镁的质量分数.
某化学学习小组利用下列药品和实验装置测定镁铝合金中镁的质量分数.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶质的质量分数为ω=$\frac{a}{ρV}$×100% | |
| B. | 溶质的物质的量浓度c=17 V/1 000 a mol•L-1 | |
| C. | 溶液中c(OH-)=V/1 000b mol•L-1 | |
| D. | 上述溶液中再加入V mL水后,所得溶液的质量分数小于0.5ω |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
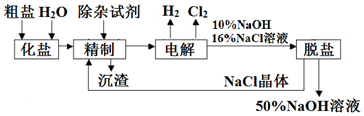
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com