
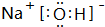 ; 用电子式表示G与Q形成化合物的过程
; 用电子式表示G与Q形成化合物的过程 ;
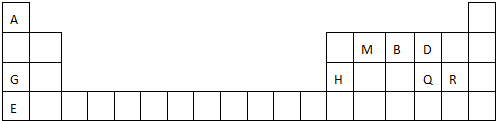
;分析 根据元素在周期表中的位置,可知A是H,M是C,B是N,D是O,G是Na,H是Al,Q是S,R是Cl,E是K.
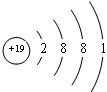
(1)由Q位置可知其位于第三周期ⅥA族;E为K,原子核外有19个电子,有4个电子层,各层电子数为2、8、8、1;
(2)电子层结构相同,核电荷数越大离子半径越小;
(3)C、O两元素形成的化合物有CO、CO2,原子之间均形成共价键,二氧化碳中碳和氧原子间形成2对共用电子对;
(4)NaOH由钠离子与氢氧根离子构成;G与Q形成化合物为Na2S,由钠离子与硫离子构成,用Na原子、S原子电子式表示其形成;
(5)利用单质之间的相互置换反应进行验证,如氯气与硫化钠反应生成硫与NaCl,可以证明Cl的非金属性强于硫;氢氧化铝与氢氧化钠反应生成偏铝酸钠与水,说明氢氧化钠的碱性更强,可以说明Na的金属性强于铝.
解答 解:根据元素在周期表中的位置,可知A是H,M是C,B是N,D是O,G是Na,H是Al,Q是S,R是Cl,E是K.
(1)由Q位置可知其位于第三周期ⅥA族;E为K,原子核外有19个电子,有4个电子层,各层电子数为2、8、8、1,原子结构示意图为 ,
,
故答案为:第三周期ⅥA族; ;
;
(2)电子层结构相同,核电荷数越大离子半径越小,故离子半径:S2->Cl->K+,
故答案为:S2->Cl->K+;
(3)C、O两元素形成的化合物有CO、CO2,原子之间均形成共价键,二氧化碳中碳和氧原子间形成2对共用电子对,结构式为:O=C=O,故答案为:共价键;O=C=O;
(4)NaOH由钠离子与氢氧根离子构成,电子式为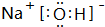 ;G与Q形成化合物为Na2S,由钠离子与硫离子构成,用Na原子、S原子电子式表示其形成为:
;G与Q形成化合物为Na2S,由钠离子与硫离子构成,用Na原子、S原子电子式表示其形成为: ,
,
故答案为: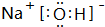 ;
; ;
;
(5)氯气与硫化钠反应生成硫与NaCl,可以证明Cl的非金属性强于硫,反应方程式为:Na2S+C12=2NaC1+S↓;
氢氧化铝与氢氧化钠反应生成偏铝酸钠与水,说明氢氧化钠的碱性更强,可以说明Na的金属性强于铝,反应方程式为:Al(OH)3+NaOH=NaAlO2+2H2O,
故答案为:Na2S+C12=2NaC1+S↓;Al(OH)3+NaOH=NaAlO2+2H2O.
点评 本题考查元素周期表与元素周期律,难度不大,关键是要在有一个完整准确的元素周期表判断元素,(5)中用化学方程式说明金属性、非金属性强弱,但体现了新课标的要求.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
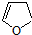 ,顺丁烯二酸酐
,顺丁烯二酸酐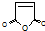 等药物中间体,广泛用于涂料行业的顺丁烯二酸二甲酯其合成流程图如下:
等药物中间体,广泛用于涂料行业的顺丁烯二酸二甲酯其合成流程图如下: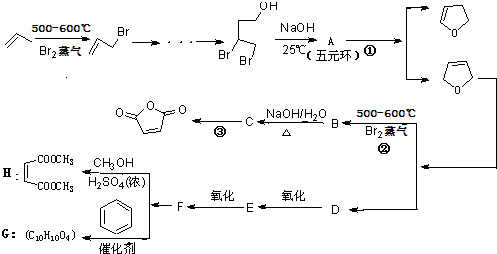
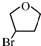 .D的结构简式HOCH2CH=CHCH2OH
.D的结构简式HOCH2CH=CHCH2OH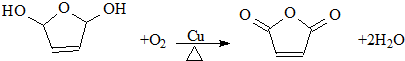 .
.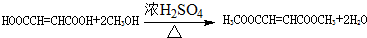 .
.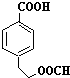 、
、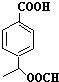 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③⑥ | B. | ②④⑥ | C. | ③⑤⑥⑦ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题

| A. | X能发生取代反应、酯化反应、加成反应和水解反应 | |
| B. | Y分子中的所有碳原子不可能共平面 | |
| C. | X、Y均能与溴水反应 | |
| D. | X、Y均能与饱和碳酸钠溶液反应放出CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验目的 | 实验操作 |
| A | 检验蔗糖水解产物中的葡萄糖 | 取1ml 20%蔗糖溶液,加入少量稀硫酸,水浴加热后取少量溶液,加入几滴新制Cu(OH)2,加热 |
| B | 除去乙烷中混有的少量乙烯 | 将混合气体通入足量酸性KMnO4溶液中 |
| C | 验证Mg(OH)2沉淀可以转化为Fe(OH)3沉淀 | 向2ml 1mol/L NaOH溶液中加入几滴1mol/L MgCl2溶液,生成白色沉淀,再加入几滴1mol/LFeCl3 |
| D | 硅酸胶体的制备 | 向Na2SiO3溶液(饱和溶液1:2用水稀释)中加入几滴酚酞,再逐滴滴入盐酸,边加边震荡,至溶液红色变浅并接近消失 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com