
| A.固态的溴化碘是分子晶体 |
| B.在许多反应中溴化碘是强氧化剂 |
| C.溴化碘跟水反应时,既是氧化剂,又是还原剂 |
| D.溴化碘与NaOH反应时,生成NaBr、NaIO和H2O |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
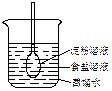
| A.细玻管内液面上升 | B.细玻管内液面不变 |
| C.蒸馏水遇碘酒变蓝 | D.蒸馏水遇硝酸银溶液有白色沉淀生成 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
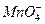 被还原成Mn2+。试写出用高锰酸钾跟浓盐酸在室温下制取氯气的化学反应方程式:____________________________。
被还原成Mn2+。试写出用高锰酸钾跟浓盐酸在室温下制取氯气的化学反应方程式:____________________________。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.AgNO3 |
| B.Na2CO3 |
| C.Na2SO3 |
| D.NaNO3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.硝酸和氢氧化钠 | B.盐酸和氨水 |
| C.硫酸和氢氧化钾 | D.醋酸和氢氧化钡 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.小于0.1mol | B.等于0.1mol |
| C.大于0.1mol,小于0.2mol | D.等于0.2mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com