
【题目】研究化学反应的热效应有利于更好的利用化学能。下列说法正确的是( )
A.放热反应任何条件下一定能自发进行
B.升高温度可以增加分子的活化能
C.生成物总能量高于反应物总能量的反应为放热反应
D.生成物的键能总和大于反应物的键能总和的反应为放热反应
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 一定温度下,反应MgCl2(1)= Mg(1)+Cl2(g)的 △H>0,△S>0
B. 常温下,NH4Cl溶液加水稀释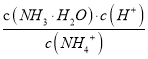 增大
增大
C. 电解饱和食盐水产生了11.2LH2,则反应中转移的电子数为6.02×1023
D. 在NaCl和KBr的混合溶液中滴加AgNO3溶液,一定先产生淡黄色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高纯硝酸锶[Sr(NO3)2]用于制造信号灯、光学玻璃等。
I.工业级硝酸锶中常含有硝酸钙、硝酸钡等杂质,其中硝酸钙可溶于浓硝酸,而硝酸锶、硝酸钡不溶于浓硝酸。提纯硝酸锶的实验步骤如下:
①取含杂质的硝酸锶样品,向其中加入浓HNO3溶解,搅拌。
②过滤,并用浓HNO3洗涤滤渣。
③将滤渣溶于水中,加略过量CrO3使Ba2+沉淀,静置后加入肼(N2H4)将过量CrO3还原,调节pH至7~8,过滤。
④将滤液用硝酸调节pH至2~3,蒸发浓缩,冷却结晶,过滤,洗涤。
⑤将得到的Sr(NO3)2·2H2O晶体在100℃条件下干燥,得到高纯硝酸锶。
(1)步骤②用浓HNO3洗涤滤渣的目的是______________。
(2)步骤③中肼将CrO3还原为Cr3+,同时产生一种无色无味的气体,该反应的离子方程式为_____________。
(3)肼具有很好的还原性,且氧化产物无污染,故可用于除去锅炉等设备供水中的溶解氧,现欲除去100L锅炉水中的溶解氧(含氧气8.8mg/L),需要肼的质量为__________。
Ⅱ.Sr(NO3)2受热易分解,生成Sr(NO2)2和O2;在500℃时Sr(NO2)2进一步分解生成SrO及氮氧化物。
(4)取一定质量含Sr(NO2)2的Sr(NO3)2样品,加热至完全分解,得到7.28gSrO固体和6.92g混合气体。计算该样品中Sr(NO3)2的质量分数__________(写出计算过程,计算结果精确到0.01%)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组从甲苯出发,按下列路线合成染料中间体X 和医药中间体Y。
已知:①化合物A.E.F 互为同分异构体。
② ;
;![]()
(1)X 中的官能团名称为________ 和________。
(2)A→B 的反应类型为________ 。
(3)B+C→D 的化学方程式是________ 。
(4)G 的结构简式为________ 。
(5)写出同时满足下列条件的E 的所有同分异构体的结构简式:________ 。
①红外光谱检测表明分子中含有醛基和羟基;
②1H- NMR 谱显示分子中含有苯环,且苯环上有两种不同化学环境的氢原子。
(6)为探索新的合成路线,采用苯和乙烯为原料制备化合物F,请写出该合成路线的流程图( 无机试剂可任选)。合成路线流程图示例如下:![]() ___________________________。
___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知1 g氢气完全燃烧生成液态水时放出热量143kJ, 18g水蒸气变成液态水放出44kJ的热量。其他相关数据如下表:
O=O | H-H | H-O(g) | |
1mol化学键断裂需要吸收的能量/kJ | 496 | 436 | x |
则表中x为
A. 188 B. 463 C. 557 D. 920
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于硝酸性质的说法不正确的是( )
A. 硝酸能与水易任意比互溶
B. 质量分数足够大时可形成发烟硝酸
C. 不易挥发,有刺激性气味
D. 浓硝酸因分解生成的二氧化氮又溶于硝酸而呈黄色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据糖类的现代定义分析,下列物质不属于糖类的是( )
①CH2(OH)—CH(OH)—CH(OH)—CHO
②CH3—CH(OH)—CHO
③CH2(OH)—CH(OH)—CH(OH)—COOH
④CH2(OH)—CO—CH(OH)—CH2OH
A.②③B.①④C.③④D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源、环境与生产生活和社会发展密切相关。
一定温度下,在两个容积均为2 L的密闭容器中,分别发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH = -49.0 kJ·mol-1。相关数据如下:
CH3OH(g)+H2O(g) ΔH = -49.0 kJ·mol-1。相关数据如下:
容器 | 甲 | 乙 |
反应物投入量 | 1 mol CO2(g)和3 mol H2(g) | 32g CH3OH(g)和18g H2O(g) |
平衡时c(CH3OH) | c1 | c2 |
平衡时能量变化 | 放出29.4 kJ | 吸收a kJ |
(1)c1____(填“>”、“<”或“=”)c2,a=____。
(2)该反应的平衡常数表达式为K=____;若甲中反应10 s 时达到平衡,则0~10 s内甲中的平均反应速率v(H2)=______。
(3)下列情况能说明该反应一定达到平衡状态的是____(填字母)。
a. v(CO2)消耗=v(CH3OH)生成 b. 气体的密度不再随时间改变
c. CO2和CH3OH的浓度之比不再随时间改变 d. 气体的平均相对分子质量不再随时间改变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com