
【题目】用一定量的铁与足量稀硫酸及足量的氧化铜制单质铜,设计了以下两种方案:
先用铁与稀硫酸反应产生氢气,再用氢气还原氧化铜得到单质铜;
先用稀硫酸溶解氧化铜得到硫酸铜溶液,再与铁发生置换反应得到单质铜。
若按实验原则进行操作,则两者制得单质铜的质量( )
A.一样多
B.①多
C.②多
D.无法判断
科目:高中化学 来源: 题型:
【题目】铜是重要金属,Cu及其化合物在科学研究和工业生产中具有许多用途。请回答以下问题:
(1)CuSO4可由金属铜与稀硫酸并通入氧气反应制备,该反应的化学方程式为_______;
(2)无水CuSO4粉末常用来检验一些有机物中的微量水分,现象是________________;
(3)![]() 的立体构型是________,其中S原子的杂化轨道类型是_______;
的立体构型是________,其中S原子的杂化轨道类型是_______;
(4)元素金(Au)处于周期表中的第六周期,与Cu同族,Au原子最外层电子排布式为______;一种铜合金晶体具有面心立方最密堆积的结构,在晶胞中Cu原子处于面心,Au原子处于顶点位置,该合金中每一层均为__________(填“密置层”、“非密置层”),金原子的配位数为__________;该晶体中,原子之间的作用力是________;
(5)上述晶体具有储氢功能,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中。若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构与CaF2的晶胞结构结构相似,该晶体储氢后的化学式应为___________。若Cu原子与Au原子的距离为a cm,则该晶体储氢后的密度为_________。(含a的表达式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 为阿伏加德罗常数的值,下列有关说法正确的是
为阿伏加德罗常数的值,下列有关说法正确的是
A.![]() 的溶液中:
的溶液中:![]() 、NH
、NH![]() 、Cu2+、
、Cu2+、![]() 一定能大量共存
一定能大量共存
B.标准状况下,![]() 和
和![]() 的混合气体中含有的分子总数为
的混合气体中含有的分子总数为![]()
C.从外观上无法区分![]() 溶液和
溶液和![]() 胶体
胶体
D.常温下,由水电离出的![]() 的溶液中:
的溶液中:![]() 、
、![]() 、NO
、NO![]() 、
、![]() 可能大量共存
可能大量共存
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过滤在实验、生产、生活中有着广泛的应用。某研究性学习小组在实验室测定某含NaCl杂质的碳酸钠样品中Cl-的含量,其实验步骤如下:
①将100g样品溶于水得到溶液A。
②向A中加入稀HNO3酸化后,再加入沉淀剂B,使Cl-完全沉淀下来。
③进行如图所示操作,得到固体C,洗涤,干燥。
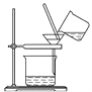
④称量得固体C的质量为2.87 g。
(1)沉淀剂B为________(填化学式)。
(2)向A中加入稀HNO3酸化的目的是_______________________。
(3)如何洗涤固体C: __________________。如果得到固体C后直接干燥、称量,会使样品中氯元素的质量分数________(填“偏大”“偏小”或“不变”)。
(4)该样品中氯元素的质量分数为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应2SO2(g)+O2(g)![]() 2SO3(g)△H<0,在一定条件下达到平衡状态,时间为t1时改变条件.化学反应速率与反应时间的关系如图所示.下列说法正确的是( )
2SO3(g)△H<0,在一定条件下达到平衡状态,时间为t1时改变条件.化学反应速率与反应时间的关系如图所示.下列说法正确的是( )
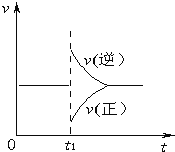
A. 维持温度、容积不变,t1时充入SO3(g)
B. 维持压强不变,t1时升高反应体系温度
C. 维持温度、容积不变,t1时充入一定量Ar
D. 维持温度、压强不变,t1时充入SO3(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4 mol A气体和2mol B气体在2 L的密闭容器中混合,并在一定条件下发生如下反应:2A(g)+B(g)![]() 2C(g),反应2 s后测得C的物质的量为1.2mol。下列说法不正确的是
2C(g),反应2 s后测得C的物质的量为1.2mol。下列说法不正确的是
A.用物质B表示2s内的平均反应速率为0.15 mol/(L·s)
B.用物质A表示2 s内的平均反应速率为0.3 mol/(L·s)
C.2 s后物质B的浓度为0.35 mol/L
D.2 s后物质A的转化率为30%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用一张已除去表面氧化膜的铝箔紧紧包裹在试管外壁(如图所示),将试管浸入硝酸汞溶液中,片刻取出,然后置于空气中,不久铝箔表面生出“白毛”,红墨水柱右端上升,根据实验现象判断下列说法错误的是( )

A.实验中发生的反应都是氧化还原反应
B.铝是一种较活泼的金属
C.铝与氧气反应放出大量的热量
D.铝片上生成的白毛是氧化铝和氧化汞的化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇与水蒸气重整可获得清洁能源,在催化剂作用下发生如下两步反应∶
反应①∶CH3OH(g)==CO(g)+2H2(g) △H1
反应②∶CO(g) + H2O(g)==CO2(g)+H2(g) △H2
根据能量变化示意图,下列说法不正确的是( )
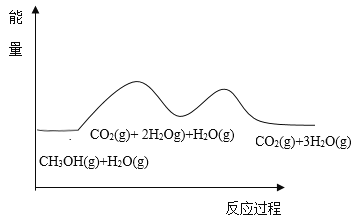
A.总反应的热化学方程式为∶ CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ![]()
B.1mol CO(g)和1mol H2O(g)的总键能大于lmol CO2(g)和1mol H2(g)的总键能
C.甲醇与水蒸气催化重整的总反应速率取决于反应①
D.催化剂在反应中改变了活化能,加快了反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知化学反应2C(s)+O2(g)![]() 2CO(g)、2CO(g)+O2(g)
2CO(g)、2CO(g)+O2(g)![]() 2CO2(g)都是放热反应。据此判断,下列说法不正确的是(其他条件相同)( )
2CO2(g)都是放热反应。据此判断,下列说法不正确的是(其他条件相同)( )
A.12g C所具有的能量一定高于28g CO所具有的能量
B.56 g CO和32 g O2所具有的总能量大于88 g CO2所具有的总能量
C.12 g C和32 g O2所具有的总能量大于44 g CO2所具有的总能量
D.将一定质量的C燃烧,生成CO2比生成CO时放出的热量多
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com