
【题目】下列叙述中正确的是()
A.摩尔是物质的量的单位B.2mol水的摩尔质量36g/mol
C.阿伏加德罗常数是12g碳中所含有碳原子数D.阿伏加德罗常数符号为NA,通常用6.02×1023表示
科目:高中化学 来源: 题型:
【题目】能源与材料、信息被称为现代社会发展的三大支柱,化学与能源有着密切联系。
(1)下表中的数据表示破坏1mol化学键需消耗的能量(即键能,单位为kJ·mol-1)
化学键 | H-H | Cl-Cl | H-Cl |
键能 | 436 | 243 | 431 |
请根据以上信息可知,1mol氢气在足量的氯气着燃烧生成氯化氢气体放出热量___________。
(2)天然气是一种重要的情节能源和化工原料,其主要成分为CH4。以CH4、空气、KOH溶液为原料,石墨为电极可构成燃料电池。该电池的负极反应式为___________。
(3)工业上有一种方法是用 CO2来生产燃料甲醇,可以将CO2变废为宝。在体积为1L的密闭容器中,充入1molCO2和3molH2,一定条件下发生反应:CO2+3H2![]() CH3OH(g)+H2O(g),测得CO2(g)和CH3OH(g)的浓度随时间变化如下图所示。
CH3OH(g)+H2O(g),测得CO2(g)和CH3OH(g)的浓度随时间变化如下图所示。
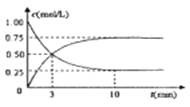
①从反应开始到平衡,CH3OH的平均反应速率v(CH3OH)=___________;H2的转换率α(H2)=___________。
②若反应CO2+3H2![]() CH3OH(g)+H2O(g)在四种不同情况下的反应速率分别为:
CH3OH(g)+H2O(g)在四种不同情况下的反应速率分别为:
A.V(CO2)=0.15mol·L-1·min-1B.V(H2)=0.01mol·L-1·s-1
C.v(CH3OH)=0.2mol·L-1·min-1D.v(H2O)=0.45mol·L-1·min-1
该反应进行由快到慢的顺序为___________(填字母)。
(4)海水化学资源的利用具有非常广阔的前景。从海水中提取溴的工业流程如图:
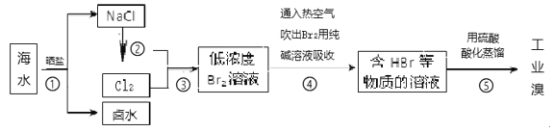
①流程④中涉及的离子反应如下,请在下面方框内填入适当的化学计量数:
□Br2+□CO32-=□BrO3-+□Br-+□CO2↑______
②以上五个过程中涉及氧化还原反应的有___________个。
③步骤③中已获得游离态的溴,步骤④又将之转变成化合态的溴,其目的是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列图示的说法中正确的是( )
A.由图①所示实验可得出三种元素的非金属性强弱顺序是:氯>碳>硅
B.图②可用于干燥、收集氯化氢,并吸收多余的氯化氢
C.图③表示可逆反应CO(g)+H2O(g)CO2(g)+H2(g)的△H>0
D.对反应:A(s)+2B(g)xC(g),根据图④可以求出x=2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物M是一种治疗恶性肿瘤的合成药物。制备M的一种合成路线如图所示:
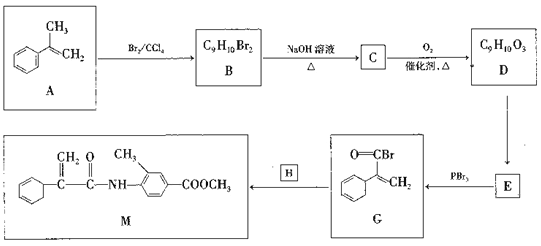
已知: 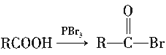 (R为烃基)。
(R为烃基)。
(1)A的化学名称是________。
(2)由A生成B和B生成C的反应类型分别是_________、________。
(3)由C生成D的化学方程式是____________________。
(4)写出E的结构简式:________,X是E的同分异构体,且X满足下列条件:
①能发生银镜反应;②遇浓FeCl3溶液变色;③分子结构中只含一个碳环结构。
符合上述条件的X有_____种,其中核磁共振氢谱显示有5种不同化学环境的氢,峰面积比为2:2:2:1:1的结构简式是_____________。
(5)根据题给信息,写出用CH3CHO和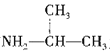 为原料制备
为原料制备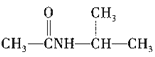 的合成路线:_________________(其他试剂任选)。
的合成路线:_________________(其他试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中某些气体的制取、收集及尾气处理装置如下图所示(省略夹持和净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是
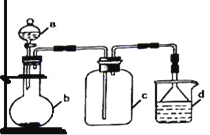
选项 | A中的物质 | B中的物质 | C中收集的气体 | D中的物质 |
A | 浓氨水 | CaO | NH3 | H2O |
B | 浓盐酸 | MnO2 | Cl2 | NaOH溶液 |
C | 稀硝酸 | Cu | NO2 | H2O |
D | 浓硫酸 | Na2SO3 | SO2 | NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠(NaNO2)是一种常见的食品添加剂。某兴趣小组用如图所示装置制备NaNO2并对其性质作如下探究(A中加热装置已略去)。

查阅资料可知:
①2NO+Na2O2=2NaNO2;2NO2+Na2O2 =2NaNO3。
②NO能被酸性KMnO4氧化成NO3-。
(1)A中滴入浓硝酸之前,应先通入N2一段时间,目的是____________。 A中反应的化学方程式_____________。
(2)装置B中观察到的主要现象______________。
(3)装置C中盛放的试剂是______________。
(4)装置E的作用是______________。
(5)写出NO被酸性KMnO4氧化的离子反应方程式______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物CH3—CH=CHCl能发生的反应有( )
①取代反应 ②加成反应 ③消去反应 ④使酸性KMnO4溶液褪色 ⑤与AgNO3溶液反应生成白色沉淀 ⑥聚合反应
A. 以上反应均能发生 B. 只有⑥不能发生 C. 只有⑤不能发生 D. 只有②不能发生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】热激活电池可用作火箭、导弹的工作电源。一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为:PbSO4+2LiCl+Ca=CaCl2+Li2SO4+Pb ,下列说法不正确的是( )
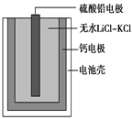
A. 工作时,电池的正极质量逐渐减轻
B. 放电过程中,Li+向正极移动
C. 每转移0.1 mol电子,理论上生成20.7 g Pb
D. 常温时,在正负极间接上电流表,指针不偏转
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com