
 工业上常用天然气作为制备甲醇CH3OH的原料.已知:
工业上常用天然气作为制备甲醇CH3OH的原料.已知:| c(CH3OH) |
| c(CO)×c2(H2) |
| 0.5a mol |
| V L |
| a |
| 2V |
| a |
| V |
| 2a |
| V |
| a |
| 2V |
| a |
| V |
| a |
| 2V |
| a |
| 2V |
| a |
| V |
| a |
| 2V |
| c(CH3OH) |
| c(CO)×c2(H2) |
| ||||
|
| V2 |
| a2 |
| V2 |
| a2 |


 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案 导学与测试系列答案
导学与测试系列答案科目:高中化学 来源: 题型:
| A、N2和H2一定条件下反应制取NH3 |
| B、硝酸工厂用NH3氧化制取NO |
| C、雷雨时空气中的N2转化为NO |
| D、由NH3制碳酸氢铵和硫酸氨 |
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
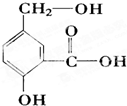 如图有机物A的分子,所含有的官能团的名称是
如图有机物A的分子,所含有的官能团的名称是查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
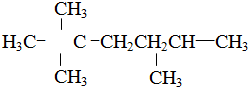 ,请按要求回答下列问题:
,请按要求回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 陈述I | 陈述Ⅱ |
| A | 常温下铁与浓硫酸、浓硝酸均不反应 | 可用铁槽车密封运送浓硫酸、浓硝酸 |
| B | Fe2+、SO2都能使酸性KMnO4褪色 | Fe2+表现还原性,SO2表现漂白性 |
| C | Al有还原性 | 利用铝热反应冶炼金属Mn |
| D | 将水蒸气通过灼热的铁粉,铁粉变红褐色 | 铁粉与水蒸气在高温下发生反应 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com