
【题目】铁镍可充电电池以KOH溶液为电解液,放电时的总反应为Fe+Ni2O3+3H2O=Fe(OH)2+2Ni(OH)2,下列有关该电池的说法正确的是
A.放电时,正极反应式为Fe-2e-+2OH-=Fe(OH)2
B.放电时,K+向Fe电极迁移
C.充电时,阴极反应式为2Ni(OH)2-2e-+2OH-=Ni2O3+3H2O
D.充电时,阳极附近溶液的pH减小
【答案】D
【解析】
根据放电时的总反应式,可知放电时,Fe化合价升高,失去电子,发生氧化反应而作负极,再结合环境呈碱性,则负极反应式为![]() ,Ni2O3中Ni元素化合价降低,得到电子,发生还原反应而作正极,则正极电极反应式为:
,Ni2O3中Ni元素化合价降低,得到电子,发生还原反应而作正极,则正极电极反应式为:![]() ,充电时,阴、阳极与负极、正极反应式正好相反,据此分析解答。
,充电时,阴、阳极与负极、正极反应式正好相反,据此分析解答。
根据放电时的总反应式,可知放电时Fe化合价升高失去电子发生氧化反应而作负极,再结合环境呈碱性,则负极反应式为![]() ,Ni2O3中Ni元素化合价降低得到电子发生还原反应而作正极,则正极电极反应式为:
,Ni2O3中Ni元素化合价降低得到电子发生还原反应而作正极,则正极电极反应式为:![]() ,充电时,阴、阳极与负极、正极反应式正好相反,
,充电时,阴、阳极与负极、正极反应式正好相反,
A. 根据分析知,放电时,正极反应式为![]() ,A项错误;
,A项错误;
B. 放电时,阳离子向正极移动,即K+向Ni2O3电极迁移,B项错误;
C. 充电时,阴极反应式为![]() ,C项错误;
,C项错误;
D. 充电时,阳极反应式为:![]() ,则阳极附近溶液的pH减小,D项正确;
,则阳极附近溶液的pH减小,D项正确;
答案选D。


科目:高中化学 来源: 题型:
【题目】下列有关电解质溶液的说法正确的是( )
A.向K2S溶液中加水稀释![]() 会减小
会减小
B.向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液中:c(Na+)<c(NO3-)
C.取c(H+)=0.01mol·L-1的盐酸和醋酸各1L,分别加入0.3g锌粉,在相同条件下充分反应,盐酸与锌反应的平均速率大
D.向CuS和FeS均饱和的混合溶液中加入少量Na2S固体,![]() 保持不变
保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由含碘废水制取碘酸钾的一种工艺如下:
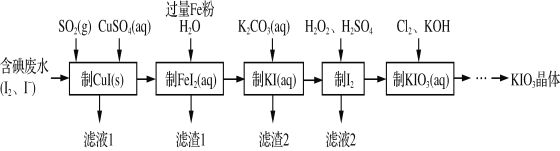
⑴ 写出KIO3在日常生活中的一个重要应用________________________。
⑵ 检验“含碘废水”中是否含有单质I2的常用试剂是________(写试剂名称)。
⑶ 通入SO2的目的是将I2还原为I-,该反应的离子方程式为______________________。
⑷ 工艺中五种物质的制备反应中,不涉及氧化还原反应的步骤是“制________”。
⑸ “制KI(aq)”时,该温度下水的离子积为Kw=1.0×10-13,Ksp[Fe(OH)2]=9.0×10-15。
为避免0.9 mol·L-1 FeI2溶液中Fe2+水解生成胶状物吸附I-,起始加入K2CO3必须保持溶液的pH不大于______。
⑹ “制KIO3溶液”反应的离子方程式为__________________。

⑺ KCl、KIO3的溶解度曲线如图所示。流程中由“KIO3(aq)”得到KIO3晶体的操作步骤为_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由H、C、N、O、S等元素形成多种化合物在生产生活中有着重要应用。
I.化工生产中用甲烷和水蒸气反应得到以CO和H2为主的混合气体,这种混合气体可用于生产甲醇,回答下列问题:
(1)对甲烷而言,有如下两个主要反应:
①CH4(g)+1/2O2(g)=CO(g)+2H2(g)△H1=-36kJ·mol-1
2CH4(g)+H2O(g)=CO(g)+3H2(g)△H2=+216kJ·mol-1
若不考虑热量耗散,物料转化率均为100%,最终炉中出来的气体只有CO、H2,为维持热平衡,年生产lmolCO,转移电子的数目为______________________。
(2)甲醇催化脱氢可制得重要的化工产品一甲醛,制备过程中能量的转化关系如图所示。

①写出上述反应的热化学方程式________________________________。
②反应热大小比较:过程I________过程II(填“大于”、“小于”或“等于”)。
II.(3)汽车使用乙醇汽油并不能减少NOx的排放,这使NOx的有效消除成为环保领城的重要课题。某研究性小组在实验室以Ag-ZSM-5为催化剂,删得NO转化为N2的转化率随温度变化情况如图所示。若不使用CO,温度超过775K,发现NO的分解率降低。其可能的原因为_____________________________________,
在n(NO)/n(CO)=1的条件下,为更好的除去NOx物质,应控制的最佳温度在_______K左右。

(4)车辆排放的氮氧化物、煤燃烧产生的二氧化硫是导致雾霾天气的“罪魁祸首”。活性炭可处理大气污染物NO。在5L密闭容器中加入NO和活性炭(假设无杂质),一定条件下生成气体E和F。当温度分别在T1℃和T2℃时,测得各物质平衡时物质的量(n/mol)如下表:
物质 温度℃ | 活性炭 | NO | E | F |
初始 | 3.000 | 0.10 | 0 | 0 |
T1 | 2.960 | 0.020 | 0.040 | 0.040 |
T2 | 2.975 | 0.050 | 0.025 | 0.025 |
①写出NO与活性炭反应的化学方程式_________________________________________;
②若T1<T2
③上述反应T1℃时达到化学平衡后再通入0.1mol NO气体,则达到新化学平衡时NO的转化率为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铃兰醛[ ]具有甜润的百合香味,对皮肤的刺激性小,对碱稳定,广泛用于百合、丁香、玉兰、茶花以及素心兰等东方型香型日用香精的合成。常用作肥皂、洗涤剂的香料,还可用作花香型化妆品的香料。其合成路线如图所示:
]具有甜润的百合香味,对皮肤的刺激性小,对碱稳定,广泛用于百合、丁香、玉兰、茶花以及素心兰等东方型香型日用香精的合成。常用作肥皂、洗涤剂的香料,还可用作花香型化妆品的香料。其合成路线如图所示:

(1)B中官能团的名称是______。
(2)①的反应类型是______。
(3)写出反应②的化学方程式:______。
(4)乌洛托品的结构简式如图所示:
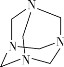
其二氯取代物有______种,将甲醛的水溶液与氨水混合蒸发可制得乌洛托品,该反应的化学方程式是______。
(5)写出满足下列条件的A的同分异构体______。
Ⅰ.有两个取代基 Ⅱ.取代基在邻位
(6)已知:RCH2COOH![]() RCHClCOOH。仿照上述流程,写出以CH3CH2CHO为原料制备聚乳酸
RCHClCOOH。仿照上述流程,写出以CH3CH2CHO为原料制备聚乳酸 的合成路线______(无机试剂自选)。
的合成路线______(无机试剂自选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z的原子序数依次增大,A、B、C、D、E均是由上述元素组成的中学化学常见的物质,其中A是单质,C是酸性氧化物,A的水溶液和C均具有漂白性,B是自然界最常见的液体,E是三元化合物,物质之间存在如图所示的关系。下列说法错误的是

A.简单离子半径大小关系:Y>Z>X>WB.图示反应中有离子键的形成
C.简单阴离子的还原性:Y>ZD.D的水溶液中含有阴、阳离子及共价键形成的分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.计算下列溶液的pH值(25 ℃),(请写出计算过程)将20mL0.01 mol·L-1 KOH溶液与30mL0.005mol·L-1H2SO4溶液混合并加水至100ml.
(1)求KOH溶液的pH值_______________;
(2)求H2SO4溶液的pH值_______________;
(3)求混合液的pH值_______________。
II.将10体积的某强酸溶液与1体积的某强碱溶液混合后溶液呈中性,则混合之前,该强酸的pH(酸)与强碱的pH(碱)之间应满足的关系__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】流动电池是一种新型电池.其主要特点是可以通过电解质溶液的循环流动,在电池外部调节电解质溶液,以保持电池内部电极周围溶液浓度的稳定。我国某研究小组新开发的一种流动电池如图所示.下列说法不正确的是( )
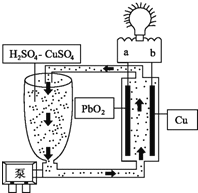
A.电子由b极流出,经导线流向a极
B.该电池工作时,H+移向a极得电子
C.b极的电极反应为Cu-2e-═Cu2+
D.该电池工作一段时间后,需要补充H2SO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com