
| A£® | 80% | B£® | 60% | C£® | 40% | D£® | 33.3% |
·ÖĪö CH4ŗĶO2»ģŗĻĘųĢå·ÅČė×ćĮæNa2O2ÓƵē»š»ØŅżČ¼£¬Éś³É¶žŃõ»ÆĢ¼”¢Ė®Óė¹żŃõ»ÆÄĘ·“Ó¦£ŗ2CO2+2Na2O2=2Na2CO3+O2£¬2H2O+2Na2O2=4NaOH+O2£¬Ķعż·½³ĢŹ½æÉŅŌ擳ö£¬¹ĢĢåÖŹĮæµÄŌö¼ÓĮæ¾ĶŹĒŌ»ģŗĻĘųĢåÖŠ2CH4ŗĶO2µÄÖŹĮæŗĶ£¬¾Ż“Ė¼ĘĖć£®
½ā“š ½ā£ŗCH4ŗĶO2»ģŗĻĘųĢå·ÅČė×ćĮæNa2O2ÓƵē»š»ØŅżČ¼£¬Éś³É¶žŃõ»ÆĢ¼”¢Ė®Óė¹żŃõ»ÆÄĘ·“Ó¦£ŗ2CO2+2Na2O2=2Na2CO3+O2£¬2H2O+2Na2O2=4NaOH+O2£¬Ķعż·½³ĢŹ½æÉŅŌ擳ö£¬¹ĢĢåÖŹĮæµÄŌö¼ÓĮæ¾ĶŹĒŌ»ģŗĻĘųĢåÖŠ2CH4ŗĶO2µÄÖŹĮæŗĶ£¬Ōņ¼×ĶéµÄÖŹĮæĪŖ£ŗ8g”Į$\frac{16”Į2}{16”Į2+32}$=4g£¬ĖłŅŌ»ģŗĻÖŠO2µÄÖŹĮæ·ÖŹżŹĒ$\frac{20g-4g}{20g}”Į100%$=80%£¬¹ŹŃ”A£®
µćĘĄ ±¾Ģāæ¼²é»ģŗĻĪļµÄ¼ĘĖć£¬ĢāÄæÄѶČÖŠµČ£¬¹Ų¼üŌŚÓŚøł¾Ż·“Ó¦·½³ĢŹ½ÅŠ¶Ļ¹żŃõ»ÆÄĘ¹ĢĢåÖŹĮæŌö¼ÓŹµÖŹĪŖĒāĘųÓė¼×Č©µÄÖŹĮ森


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ģ¼ĖįÄĘČÜŅŗ³Ź¼īŠŌ£¬æÉÓĆČȵēæ¼īČÜŅŗ³żČ„ÓĶÖ¬ | |
| B£® | ĻõĖįÓėĢś·¢Éś»Æѧ·“Ó¦£¬²»æÉÓĆĢśÖĘČŻĘ÷Ź¢×°ÅØĻõĖį | |
| C£® | ĀĮ±ķĆęŅ׊Ī³ÉÖĀĆܵÄŃõ»ÆĤ£¬ĀĮÖĘĘ÷Ćóæɳ¤Ź±¼äŹ¢·ÅĻĢ²ĖµČėēÖĘŹ³Ę· | |
| D£® | H2ÓėCl2¹āÕÕ·¢Éś±¬ÕØ£¬¹¤ŅµÉĻ²»ÄÜÓĆH2ÓėCl2×öŌĮĻÉś²śHCl |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | Cl2ŗĶHCl | B£® | N2ŗĶO2 | C£® | SO2ŗĶCO2 | D£® | CO2ŗĶO2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½«0.2 mol/LµÄNH4Al£ØSO4£©2ČÜŅŗÓė0.3 mol/LµÄBa£ØOH£©2ČÜŅŗµČĢå»ż»ģŗĻ£ŗ2NH4++Al3++3SO42-+3Ba2++6OH-ØTAl£ØOH£©3”ż+AlO2-+3BaSO4”ż+2H2O | |
| B£® | ½«ŗ¬ÓŠµČĪļÖŹµÄĮæČÜÖŹµÄNaHCO3ČÜŅŗŗĶBa£ØOH£©2ČÜŅŗ»ģŗĻ£ŗBa2++HCO${\;}_{3}^{-}$+OH-ØTBaCO3”ż+H2O | |
| C£® | ŌŚÖŲøõĖį¼ŲČÜŅŗÖŠ£¬¼ÓĖįŗóČÜŅŗ±äĪŖ»ĘÉ«£ŗCr2O72-+H2OØT2 CrO42-+2H+ | |
| D£® | ¹żĮæĀČĖ®ÓėFeI2ČÜŅŗ×÷ÓĆ£ŗ2Fe2++2I-+2Cl2ØT2 Fe3++I2+4Cl- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓÉ·“Ó¦æÉČ·¶Ø£ŗŃõ»Æ²śĪļŹĒO2 | |
| B£® | ČōĀČĖį·Ö½āĖłµĆ»ģŗĻĘųĢålmol»ģŗĻĘųĢåÖŹĮæĪŖ45g£¬Ōņ·“Ó¦·½³ĢŹ½æɱķŹ¾ĪŖ£ŗ3HClO3ØT2O2”ü+C12”ü+HClO4+H2O | |
| C£® | ÓÉ·Ē½šŹōŠŌCl£¾S£¬æÉĶĘÖŖĖįŠŌHClO3£¾H2SO4 | |
| D£® | Čō»Æѧ¼ĘĮæŹża=8£¬b=3£¬ŌņøĆ·“Ó¦×ŖŅʵē×ÓŹżĪŖ8e- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 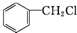 | B£® | 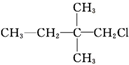 | C£® | CH3CHBrCH3 | D£® | 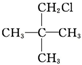 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
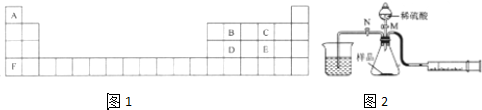
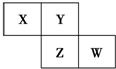 X”¢Y”¢Z”¢W¾łĪŖ¶ĢÖÜĘŚŌŖĖŲ£¬ĖüĆĒŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄĻą¶ŌĪ»ÖĆČēĶ¼ĖłŹ¾£®ČōZŌ×ÓµÄ×īĶā²ćµē×ÓŹżŹĒµŚŅ»²ćµē×ÓŹżµÄ3±¶£¬ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ£Ø””””£©
X”¢Y”¢Z”¢W¾łĪŖ¶ĢÖÜĘŚŌŖĖŲ£¬ĖüĆĒŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄĻą¶ŌĪ»ÖĆČēĶ¼ĖłŹ¾£®ČōZŌ×ÓµÄ×īĶā²ćµē×ÓŹżŹĒµŚŅ»²ćµē×ÓŹżµÄ3±¶£¬ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ£Ø””””£©| A£® | XµÄ×ī³£¼ūĘųĢ¬Ēā»ÆĪļµÄĖ®ČÜŅŗĻŌ¼īŠŌ | |
| B£® | ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļµÄĖįŠŌW±ČZČõ | |
| C£® | ZµÄµ„ÖŹÓėĒāĘų·“Ó¦±ČYµ„ÖŹÓėĒāĘų·“Ó¦¾ēĮŅ | |
| D£® | X”¢WµÄĘųĢ¬Ēā»ÆĪļĻą»„·“Ó¦£¬Éś³ÉĪļÖŠÖ»ŗ¬Ąė×Ó¼ü²»ŗ¬¹²¼Ū¼ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¼ĘĖćĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com