
【题目】下列叙述不正确的是( )
A.氯气在通常情况下呈黄绿色
B.氯气可用于自来水消毒
C.氯气、液氯和氯水是同一种物质
D.氯气有毒,氯离子无毒
科目:高中化学 来源: 题型:
【题目】某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中的溶质足量),当闭合该装置的电键K时,观察到电流表的指针发生了偏转。

请回答下列问题:
(1)甲池为_________(填“原电池”、“电解池”或“电镀池”),A电极的电极反应式为______。
(2)丙池中F电极为____(填“正极”、“负极”、“阴极”或“阳极”),该池总反应的方程式为_____。
(3)当乙池中C极质量减轻4.32g时,甲池中B电极理论上消耗O2的体积为_____mL(标准状况)。
(4)一段时间后,断开电键K。下列物质能使乙池恢复到反应前浓度的是______(填字母)。
A.Cu B.CuO C.Cu(OH)2 D.Cu(OH)2CO3
(5)甲醇和乙醇都可以做燃料。已知乙醇液体完全燃烧生成CO2气体和1mol液态水时放出热量453.3kJ,请写出乙醇燃烧的热化学方程式:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质按混合物、酸、碱顺序排列的是( )
A.干冰、醋酸、苛性钠
B.氯水、亚硫酸、氢氧化铜
C.蔗糖水、硫酸铜、氢氧化铁
D.水玻璃、硝酸、纯碱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下,用一定量的水吸收氨气后制得浓度为12.0 mol·L-1、密度为0.915 g·cm-3的氨水。试计算1体积水吸收多少体积的氨气可制得上述氨水。(本题中氨的式量以 17.0计,氨水的溶质以溶解的NH3为准,水的密度以1.00g·cm-3计)_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是用实验室制得的乙烯(C2H5OH![]() CH2=CH2↑+H2O)与溴水作用制取1,2﹣二溴乙烷的部分装置图,根据图示判断下列说法正确的是
CH2=CH2↑+H2O)与溴水作用制取1,2﹣二溴乙烷的部分装置图,根据图示判断下列说法正确的是

A. 装置①和装置③中都盛有水,其作用相同
B. 装置②和装置④中都盛有NaOH溶液,其吸收的杂质相同
C. 产物可用分液的方法进行分离,1,2﹣二溴乙烷应从分液漏斗的上口倒出
D. 制备乙烯和生成1,2﹣二溴乙烷的反应类型分别是消去反应和加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是SO2制取、性质检验、收集、尾气处理的装置,有关说法正确的是
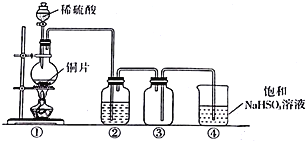
A. 上图中有两处错误
B. 装置①也可以用于制取氨气、氯气
C. 在②中加入品红或紫色石蕊试液都可以验证SO2的漂白性
D. 在②中加入BaCl2溶液,先生成白色沉淀,随后沉淀慢慢消失
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物G是合成某种耐热聚合物的单体,其合成方法如下:

已知:R1COOR2+R3OH ![]() RCOOR3+R2OH
RCOOR3+R2OH
(1)根据系统命名法,A的名称为___ .
(2)上述流程中的取代反应除②、③外还有___(填序号).第⑤步反应中,可使用含有18O的F,将之与C反应,并检测产物中18O的分布情况,从而推断反应机理,这种研究方法称为___ .
(3)化合物E的核磁共振氢谱图中共有多个吸收峰,各峰的峰面积比为___ .
(4)按下列合成路线可得到F的同分异构体H,则可鉴别H与F的试剂是___ .

(5)C与足量NaOH溶液反应的化学方程式为___ .
(6)J与C互为同分异构体,其具有如下性质.符合要求的有机物有___种(不考虑立体异构)
①能与NaOH溶液反应,且1mol J完全反应消耗4mol NaOH
②能发生银镜反应,且1mol J与足量的银氨溶液反应生成4mol Ag
③分子中苯环上的一氯取代物只有一种.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修3:物质结构与性质]
铜、银、金与社会生活联系密切。
(1)在周期表中, 铜、银、金位于同一族,它们基态原子的外围电子排布式的通式为__________________(用n表示电子层数),它们位于元素周期表的________区。
(2)化学上,银氨溶液可以检验醛基的存在,例如:H3CHO+2Ag(NH3)2OH![]() CH3COONH4+2Ag↓+3NH3
CH3COONH4+2Ag↓+3NH3
+H2O。1个CH3CHO分子中所含π键的数目为________,碳原子的杂化轨道类型为________;CH3 CH2OH、CH3CHO的相对分子质量仅相差2,但沸点相差很大(分别为78.5℃,20.8℃),其主要原因是________________________;NH3的VSEPR模型为________。
(3)金不溶于硝酸,但溶于“王水”,发生反应:Au+4HCl+HNO3=H[AuCl4]+NO↑+2H2O。金溶于王水的主要原因是形成了[AuCl4],提高了金的活动性。在[AuCl4]-中,金离子的配位数为________,画出该配离子的结构式:________。
(4)金、银、铜都有良好的延展性,解释其原因:________________________________。
(5)金、银的一种合金具有较强的储氢能力。该合金的晶胞为面心立方结构,银原子位于面心,金原子位于顶点。若该晶胞边长为anm,金、银原子的半径分别为bnm、cnm。则该晶胞的空间利用率(φ)
为________ (用含a、b、c和圆周率π的式子表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示细胞内某些有机物的元素组成和功能的关系,其中A、B代表元素,Ⅰ、Ⅱ、Ⅲ、Ⅳ是生物大分子,图中X、Y、Z、P分别为构成生物大分子的基本单位.请回答下列问题:

(1)图中Ⅰ在人体肝脏中是指______________.
(2)图中Ⅱ是__________,使用甲基绿、吡罗红混合染液染色Ⅲ,可使Ⅲ呈现_____色.
(3)图中P一定含有的元素是__________。P的结构通式为_________________
(4)Y和Z彻底水解都可以产生______种物质。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com