
【题目】已知常温下![]() 的电离平衡常数
的电离平衡常数![]() ,
,![]() 的电离平衡常数
的电离平衡常数![]() ,
,![]() 的电离平衡常数
的电离平衡常数![]() 。若溶液混合引起的体积变化可忽略,则室温时下列指定溶液中微粒物质的量浓度关系正确的是( )
。若溶液混合引起的体积变化可忽略,则室温时下列指定溶液中微粒物质的量浓度关系正确的是( )
A.![]() 溶液:
溶液:![]()
B.![]() 的
的![]() 溶液和
溶液和![]() 的
的![]() 溶液等体积混合:
溶液等体积混合:![]()
C.![]() 的
的![]() 和
和![]() 的
的![]() 溶液等体积混合:
溶液等体积混合:![]()
D.![]() 氨水和
氨水和![]() 溶液等体积混合:
溶液等体积混合:![]()
【答案】BC
【解析】
A.根据SH-的电离程度和水解程度的大小分析;
B.据物料守恒分析;
C.根据电荷守恒分析;
D.由电荷守恒和物料守恒综合分析。
A.![]() 溶液中,存在
溶液中,存在![]() 的水解平衡
的水解平衡![]() ,以及
,以及![]() 的水解平衡
的水解平衡![]() ,由
,由![]() 的电离平衡常数
的电离平衡常数![]() 和
和![]() 的电离平衡常数
的电离平衡常数![]() 可知,溶液以
可知,溶液以![]() 的水解平衡为主,
的水解平衡为主,![]() ,再结合溶液中弱酸根和弱碱根的水解是微弱的特点,溶液中相关微粒浓度大小顺序为
,再结合溶液中弱酸根和弱碱根的水解是微弱的特点,溶液中相关微粒浓度大小顺序为![]() ,故A错误;
,故A错误;
B.据物料守恒![]() ,
,![]() ,
,![]() ,故
,故![]() ,故B正确;
,故B正确;
C.据电荷守恒![]() ,即
,即![]() ,类比A选项可知混合溶液
,类比A选项可知混合溶液![]() ,
,![]() ,又因为
,又因为![]() 水解,混合后
水解,混合后![]() 小于
小于![]() ,所以
,所以![]() ,故C正确;
,故C正确;
D.![]() ,
,![]() 的氨水和
的氨水和![]() 的
的![]() 溶液等体积混合后,得到溶质为
溶液等体积混合后,得到溶质为![]() 氨水和
氨水和![]() 的
的![]() 混合溶液,电荷守恒有
混合溶液,电荷守恒有![]() ①,物料守恒有
①,物料守恒有![]() ②,
②,![]() ③,①
③,①![]() ②
②![]() ③,得
③,得![]() ,故D错误。
,故D错误。
答案选BC。


科目:高中化学 来源: 题型:
【题目】已知A→C必须加热,否则会发生钝化现象。请回答下列问题:
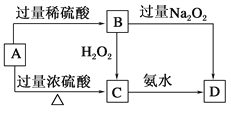
(1)A是________,你推断的理由是___________________。
(2)B在酸性条件下与H2O2反应的离子方程式:_____________________。
(3)A与过量浓H2SO4反应的化学方程式:_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向10.00 mL 0.1mol/L某二元酸H2X溶液中逐滴加入0.1 mol/L NaOH溶液,其pH变化如图所示(忽略温度变化),已知:常温下,H2X的电离常数Ka1=1.1×10-5,Ka2=1.3×10-8。下列叙述正确的是
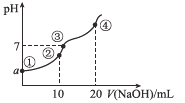
A.a近似等于3
B.点②处c(Na+)+2c(H+)+c(H2X)=2c(X2-)+c(HX-)+2c(OH-)
C.点③处为H2X和NaOH中和反应的滴定终点
D.点④处c(Na+)=2c(X2-)>c(OH-)>c(HX-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在恒容密闭容器中发生如下反应:2N2O4(g)+N2O(g)![]() 3N2O3(g),若反应开始时充入2molN2O4和2mol N2O,达平衡后N2O4的体积分数为a%。其他条件不变时,若按下列四种配比作为起始物质,平衡后N2O4的体积分数大于a%的是( )
3N2O3(g),若反应开始时充入2molN2O4和2mol N2O,达平衡后N2O4的体积分数为a%。其他条件不变时,若按下列四种配比作为起始物质,平衡后N2O4的体积分数大于a%的是( )
A.2molN2O3
B.2mol N2O4、2molN2O和1molHe(不参加反应)
C.1molN2O和1molN2O3
D.2molN2O4、3molN2O和3molN2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物在工农业生产中具有重要作用。
(1)某小组进行工业合成氨N2(g)+3H2(g)2NH3(g)+Q的模拟研究,在1L密闭容器中,分别加入0.1molN2和0.3molH2。实验①、②、③中c(N2)随时间(t)的变化如图所示,实验②从开始到达平衡状态的过程中,用H2表示的平均反应速率为____。与实验①相比,实验②所采用的实验条件可能为____(填字母)
a.增大压强 b.减小压强 c.升高温度 d.降低温度 e.使用催化剂

(2)NH3用于处理废气中的氮氧化物,其反应原理为2NH3(g)+NO(g)+NO2(g)2N2(g)+3H2O(g)+Q,欲提高废气中氮氧化物的转化率,可采取的措施是____(填字母);
a.升高温度 b.增大压强 c.增大NH3的浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸(H2C2O4)是一种重要的化学试剂。下面是利用草酸探究外界条件对反应速率影响的实验。
(1)该反应是溶液之间发生的不可逆反应,改变压强对其反应速率的影响是___(填序号)。
A.可能明显加快 B.可能明显减慢 C.几乎无影响,可以忽略
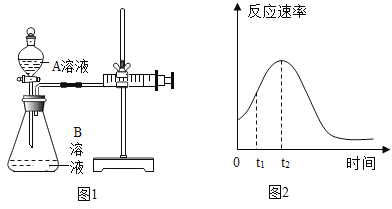
(2)用酸性KMnO4和H2C2O4反应研究影响反应速率的因素。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
实验序号 | A溶液 | B溶液 |
① | 20mL0.1molL-1H2C2O4溶液 | 30mL0.01molL-1KMnO4溶液 |
② | 20mL0.2molL-1H2C2O4溶液 | 30mL0.01molL-1KMnO4溶液 |
①该反应的离子方程式____。
②该实验探究的是___因素对化学反应速率的影响。相同时间内针筒中所得CO2的体积大小关系是___>__(填实验序号)。
(3)若实验①在2min末收集了4.48mLCO2(标准状况下),用CO2表示2min内的反应速率为___mol/min,则在2min末c(MnO4-)=___mol/L(假设混合液体积为50mL)。
(4)小组同学发现反应速率总是如图2,其中t1~t2时间内速率变快的主要原因可能是:①____;②____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可由![]() 、
、![]() 、
、![]() 为原料制备
为原料制备![]() ,若反应后废液中的
,若反应后废液中的![]() 排入水中,则过量的氮元素会使水体富营养化。此外考虑到其他污染源,污水一般还会含有
排入水中,则过量的氮元素会使水体富营养化。此外考虑到其他污染源,污水一般还会含有![]() 、
、![]() 、
、![]() 等。
等。
(1)已知![]() 化学式可表示为
化学式可表示为![]() ,由常温下逐渐升温的过程中会发生分解。已知起始状态到A点是失去了部分结晶水,B点对应的物质是钒的氧化物,如下图所示。
,由常温下逐渐升温的过程中会发生分解。已知起始状态到A点是失去了部分结晶水,B点对应的物质是钒的氧化物,如下图所示。
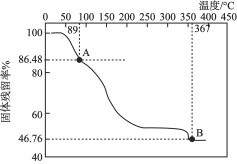
①写出起始状态到A点发生分解反应的化学方程式:________________。
②B点对应物质的化学式是______________。
(2)废水中![]() 和
和![]() 的处理。通过形成铁炭(铁和活性炭)原电池可对废水中的有机物及含氮物质等进行处理,将酸性废水中以
的处理。通过形成铁炭(铁和活性炭)原电池可对废水中的有机物及含氮物质等进行处理,将酸性废水中以![]() 和
和![]() 形式存在的氮元素转化为
形式存在的氮元素转化为![]() 除去。
除去。
①写出![]() 在正极发生的电极反应式______________。
在正极发生的电极反应式______________。
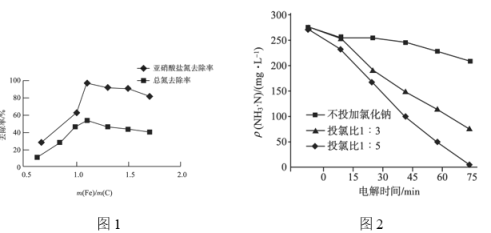
②不同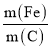 的脱氮效果如图1所示,则合适的
的脱氮效果如图1所示,则合适的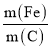 =________。
=________。
③实验测得当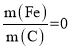 时,对废水中的氮也有一定的脱除率,其原因为________。
时,对废水中的氮也有一定的脱除率,其原因为________。
(3)废水中![]() 的处理。用电解法可对废水进行脱氮处理。
的处理。用电解法可对废水进行脱氮处理。
①电解时含氯离子转化为次氯酸,![]() 与
与![]() 反应生成
反应生成![]() ,当生成
,当生成![]() 时,转移的电子数为________mol。
时,转移的电子数为________mol。
②氯离子含量对废水脱氮效果的影响如图2所示,投氯比是指氨氮与氯离子物质的量的比,三种情况下投料为![]() 时脱氮效果________(填“最好”“最差”或“居中”),原因可能是________。
时脱氮效果________(填“最好”“最差”或“居中”),原因可能是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有168g NaHCO3 固体,加热到质量不再变化为止,试计算:
(1)剩余固体的质量(m);__________
(2) (标准状况下)产生气体的体积v。__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钕铁硼磁铁是目前为止具有最强磁力的永久磁铁。预计在未来20年里,不可能有替代钕铁硼磁铁的磁性材料出现。生产钕铁硼磁铁的主要原材料有稀土金属钕、纯铁、铝、硼以及其它稀土原料。
(1)钕(Nd)为60号元素,在元素周期表中的位置是___;
(2)实验测得气态A1C13的实际存在形式为A12C16双聚分子,其中A1原子的杂化方式是___;A12C16与过量NaOH溶液反应生成Na[Al(OH)4];[A1(OH)4]-中存在的化学键有___。
A.离子键 B.共价键 C.配位键 D.金属键 E.氢键
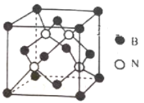
(3)已知立方BN晶体晶胞结构如图所示,设晶胞中最近的B、N原子之间的距离为a nm,晶体的密度为b gcm-3,则阿伏加德罗常数为____mol-1 (列式即可)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com