
ΓΨΧβΡΩΓΩΡΣΕϊ―ΈΒΡΜ·―ß ΫΈΣ![]() Θ®œύΕ‘Ζ÷Ή”÷ ΝΩΈΣ392Θ©Θ§Ρή»ή”ΎΥ°Θ§≤Μ»ή”Ύ““¥ΦΘ§ «“Μ÷÷÷Ί“ΣΒΡΜΙ‘≠ΦΝΘ§‘ΎΩ’Τχ÷–±»“ΜΑψΒΡ―«Χζ―ΈΈ»Ε®ΓΘœ¬Οφ «Ρ≥―ßœΑ–ΓΉι…ηΦΤ÷Τ±Η…ΌΝΩΡΣΕϊ―ΈΒΡ Β―ιΉΑ÷ΟΦΑ≤Ϋ÷ηΓΘΜΊ¥πœύΙΊΈ ΧβΘΚ
Θ®œύΕ‘Ζ÷Ή”÷ ΝΩΈΣ392Θ©Θ§Ρή»ή”ΎΥ°Θ§≤Μ»ή”Ύ““¥ΦΘ§ «“Μ÷÷÷Ί“ΣΒΡΜΙ‘≠ΦΝΘ§‘ΎΩ’Τχ÷–±»“ΜΑψΒΡ―«Χζ―ΈΈ»Ε®ΓΘœ¬Οφ «Ρ≥―ßœΑ–ΓΉι…ηΦΤ÷Τ±Η…ΌΝΩΡΣΕϊ―ΈΒΡ Β―ιΉΑ÷ΟΦΑ≤Ϋ÷ηΓΘΜΊ¥πœύΙΊΈ ΧβΘΚ
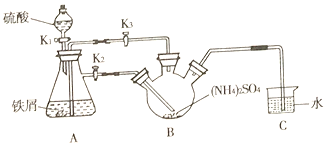
≤Ϋ÷η“ΜΘΚ÷Τ»ΓΡΣΕϊ―Έ
Θ®1Θ©Ν§Ϋ”ΉΑ÷ΟΘ§Φλ≤ιΉΑ÷ΟΤχΟή–‘ΚσΦ”»κ“©ΤΖΓΘ‘ΎΉΕ–ΈΤΩ÷–Φ”»κ![]() Χζ–ΦΚΆ…ΌΝΩΒΡΧΦΖέΘ§‘Ύ»ΐΨ±…’ΤΩ÷–Φ”»κ
Χζ–ΦΚΆ…ΌΝΩΒΡΧΦΖέΘ§‘Ύ»ΐΨ±…’ΤΩ÷–Φ”»κ![]() ΨßΧεΘ°Φ”»κ…ΌΝΩΧΦΖέΒΡΉς”Ο «_____ΓΘ
ΨßΧεΘ°Φ”»κ…ΌΝΩΧΦΖέΒΡΉς”Ο «_____ΓΘ
Θ®2Θ©œρΖ÷“Κ¬©ΕΖ÷–ΉΔ»κ![]() œΓΝρΥαΚσΘ§ΙΊ±’Μν»ϊ
œΓΝρΥαΚσΘ§ΙΊ±’Μν»ϊ![]() Θ§¥ρΩΣ
Θ§¥ρΩΣ![]() ΓΔ
ΓΔ![]() Θ§¥ΐœΓΝρΥαΉΔ»κΉΕ–ΈΤΩΚσΙΊ±’
Θ§¥ΐœΓΝρΥαΉΔ»κΉΕ–ΈΤΩΚσΙΊ±’![]() ΓΘ
ΓΘ![]() ΉΑ÷Ο÷–Ζ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣ______ΓΘ
ΉΑ÷Ο÷–Ζ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣ______ΓΘ
Θ®3Θ©¥ΐ¥σ≤ΩΖ÷ΧζΖέ»ήΫβΚσΘ§¥ρΩΣ![]() ΓΔΙΊ±’
ΓΔΙΊ±’![]() Θ§¥Υ ±Ω…“‘Ω¥ΒΫΒΡœ÷œσΈΣ_____Θ§‘≠“ρ «_____ΓΘ
Θ§¥Υ ±Ω…“‘Ω¥ΒΫΒΡœ÷œσΈΣ_____Θ§‘≠“ρ «_____ΓΘ
Θ®4Θ©ΙΊ±’Μν»ϊ![]() ΓΔ
ΓΔ![]() Θ§≤…”Ο100ΓφΥ°‘Γ’τΖΔ
Θ§≤…”Ο100ΓφΥ°‘Γ’τΖΔ![]() ÷–Υ°Ζ÷Θ§“ΚΟφ≤ζ…ζΨßΡΛ ±Θ§ΆΘ÷ΙΦ”»»Θ§ά以ΫαΨßΓΔ____Θ®Χν≤ΌΉςΟϊ≥ΤΘ©ΓΔ”ΟΈόΥ°““¥Φœ¥Β”ΨßΧεΓΘΗΟΖ¥”Π÷–ΝρΥα–ηΙΐΝΩΘ§±Θ≥÷»ή“ΚΒΡ
÷–Υ°Ζ÷Θ§“ΚΟφ≤ζ…ζΨßΡΛ ±Θ§ΆΘ÷ΙΦ”»»Θ§ά以ΫαΨßΓΔ____Θ®Χν≤ΌΉςΟϊ≥ΤΘ©ΓΔ”ΟΈόΥ°““¥Φœ¥Β”ΨßΧεΓΘΗΟΖ¥”Π÷–ΝρΥα–ηΙΐΝΩΘ§±Θ≥÷»ή“ΚΒΡ![]() ‘Ύ1~2÷°ΦδΘ§ΤδΡΩΒΡΈΣ_____ΓΘ
‘Ύ1~2÷°ΦδΘ§ΤδΡΩΒΡΈΣ_____ΓΘ
Θ®5Θ©ΉΑ÷Ο![]() ΒΡΉς”ΟΈΣ______ΓΘ
ΒΡΉς”ΟΈΣ______ΓΘ
≤Ϋ÷ηΕΰΘΚ≤βΕ®ΡΣΕϊ―Έ―υΤΖΒΡ¥ΩΕ»
Θ®6Θ©≥Τ»ΓΥυΒΟΡΣΕϊ―Έ―υΤΖ![]() Θ§”Ο÷σΖ–Κσά以ΒΡ’τΝσΥ°≈δ≥…
Θ§”Ο÷σΖ–Κσά以ΒΡ’τΝσΥ°≈δ≥…![]() »ή“ΚΘ§»Γ
»ή“ΚΘ§»Γ![]() »ή“ΚΦ”»κœΓΝρΥαΘ§”Ο
»ή“ΚΦ”»κœΓΝρΥαΘ§”Ο![]() ΒΡ
ΒΡ![]() »ή“ΚΒΈΕ®Θ§¥οΒΫΒΈΕ®÷’Βψ ±œϊΚΡ
»ή“ΚΒΈΕ®Θ§¥οΒΫΒΈΕ®÷’Βψ ±œϊΚΡ![]() »ή“ΚΘ°ΒΈΕ®Ζ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣ________Θ§ΗΟ―υΤΖΒΡ¥ΩΕ»ΈΣ________ΓΘ
»ή“ΚΘ°ΒΈΕ®Ζ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣ________Θ§ΗΟ―υΤΖΒΡ¥ΩΕ»ΈΣ________ΓΘ
ΓΨ¥πΑΗΓΩ”κΧζΓΔœΓΝρΥαΙΙ≥…‘≠Βγ≥ΊΘ§Φ”ΩλΖ¥”ΠΥΌ¬ ![]()
![]() ÷–ΒΡ“ΚΧε±Μ―Ι»κ
÷–ΒΡ“ΚΧε±Μ―Ι»κ![]() ÷–
÷– ![]() ÷–≤ζ…ζ«βΤχΘ§ Ι
÷–≤ζ…ζ«βΤχΘ§ Ι![]() ÷–―Ι«Ω‘ω¥σ Ιΐ¬Υ “÷÷Τ
÷–―Ι«Ω‘ω¥σ Ιΐ¬Υ “÷÷Τ![]() Υ°Ϋβ “ΚΖβΉς”ΟΘ§Ζά÷ΙΩ’ΤχΫχ»κ»ΐΨ±…’ΤΩ―θΜ·
Υ°Ϋβ “ΚΖβΉς”ΟΘ§Ζά÷ΙΩ’ΤχΫχ»κ»ΐΨ±…’ΤΩ―θΜ· ![]() 98%
98%
ΓΨΫβΈωΓΩ
≤Ϋ÷η“ΜΘ°÷Τ»ΓΡΣΕϊ―ΈΘΚ¥ρΩΣΖ÷“Κ¬©ΕΖ…œΩΎ»ϊΉ”Θ§ΙΊ±’Μν»ϊK3Θ§¥ρΩΣK2ΓΔK1Θ§Φ”Άξ55.0mL2molL-1œΓΝρΥαΘ§ΝρΥαΚΆΧζΖ¥”Π…ζ≥…«βΤχΘ§ΫΪΉΑ÷ΟΡΎΒΡΩ’Τχ≈≈≥ωΘ§¥ΐ¥σ≤ΩΖ÷ΧζΖέ»ήΫβΚσΘ§¥ρΩΣK3ΓΔΙΊ±’K2Θ§A÷–ΒΡ“ΚΧε±Μ―Ι»κB÷–Θ§ΙΊ±’Μν»ϊK2ΓΔK3Θ§≤…”Ο100ΓφΥ°‘Γ’τΖΔB÷–Υ°Ζ÷Θ§Ω……ζ≥…ΡΣΕϊ―ΈΘ§ά以ΫαΨßΘ§Ιΐ¬ΥΘ§”ΟΈόΥ°““¥Φœ¥Β”Θ§Ω…ΒΟΒΫΡΣΕϊ―ΈΨßΧεΘ§ΉΑ÷ΟCΩ…”Ο”Ύ“ΚΖβΘ§Ζά÷ΙΩ’ΤχΫχ»κ»ΐΨ±…’ΤΩ―θΜ·Fe2+ΘΜ
≤Ϋ÷ηΕΰΘ°≤βΕ®ΡΣΕϊ―Έ―υΤΖΒΡ¥ΩΕ»ΘΚΖΔ…ζ5Fe2++MnO4-+8H+®T5Fe3++Mn2++4H2OΘ§ΫαΚœάκΉ”ΖΫ≥Χ ΫΦΤΥψΘΜ
(1) ‘ΎΉΕ–ΈΤΩΡΎ”–![]() Χζ–ΦΚΆ…ΌΝΩΒΡΧΦΖέΚΆœΓΝρΥαΘ§Χζ”κΝρΥαΖ¥”ΠΙΐ≥Χ÷–Θ§ΧζΓΔΧΦΚΆœΓΝρΥαΙΙ≥…ΝΥ‘≠Βγ≥ΊΘ§Φ”ΩλΝΥΖ¥”ΠΥΌ¬ ΘΜ
Χζ–ΦΚΆ…ΌΝΩΒΡΧΦΖέΚΆœΓΝρΥαΘ§Χζ”κΝρΥαΖ¥”ΠΙΐ≥Χ÷–Θ§ΧζΓΔΧΦΚΆœΓΝρΥαΙΙ≥…ΝΥ‘≠Βγ≥ΊΘ§Φ”ΩλΝΥΖ¥”ΠΥΌ¬ ΘΜ
¥πΑΗΈΣΘΚ”κΧζΓΔœΓΝρΥαΙΙ≥…‘≠Βγ≥ΊΘ§Φ”ΩλΖ¥”ΠΥΌ¬ ΘΜ
(2)Χζ”κΝρΥαΖ¥”Π…ζ≥…ΝρΥα―«ΧζΚΆ«βΤχ,άκΉ”ΖΫ≥Χ ΫΈΣ![]() ΘΜ
ΘΜ
¥πΑΗΈΣΘΚ![]() ΘΜ
ΘΜ
(3)¥ΐ¥σ≤ΩΖ÷ΧζΖέ»ήΫβΚσΘ§¥ρΩΣ![]() ΓΔΙΊ±’
ΓΔΙΊ±’![]() Θ§¥Υ ±Ω…“‘Ω¥ΒΫΘ§A÷–ΒΡ“ΚΧε±Μ―Ι»κB÷–Θ§‘≠“ρ «ΙΊ±’
Θ§¥Υ ±Ω…“‘Ω¥ΒΫΘ§A÷–ΒΡ“ΚΧε±Μ―Ι»κB÷–Θ§‘≠“ρ «ΙΊ±’![]() “‘Κσ«βΤχ»‘‘Ύ≤ζ…滥÷ΆΝτ‘ΎΉΕ–ΈΤΩΡΎΘ§Ι A÷–―Ι«Ω‘ω¥σΑ―“ΚΧε―Ι»κB÷–ΘΜ
“‘Κσ«βΤχ»‘‘Ύ≤ζ…滥÷ΆΝτ‘ΎΉΕ–ΈΤΩΡΎΘ§Ι A÷–―Ι«Ω‘ω¥σΑ―“ΚΧε―Ι»κB÷–ΘΜ
¥πΑΗΈΣΘΚA÷–ΒΡ“ΚΧε±Μ―Ι»κB÷–ΘΜA÷–≤ζ…ζ«βΤχΘ§ ΙA÷–―Ι«Ω‘ω¥σΘΜ
(4) Ιΐ¬ΥΩ…ΫΪΨßΧε¥”»ή“Κ÷–Ζ÷άκ≥ωά¥Θ§ΝρΥα―«Χζ ««ΩΦν»θΥα―ΈΜαΥ°ΫβΘ§ΝρΥαΙΐΝΩΩ…“÷÷Τ―«ΧζάκΉ”Υ°ΫβΘΜ
¥πΑΗΈΣΘΚΙΐ¬ΥΘΜ“÷÷Τ![]() Υ°ΫβΘΜ
Υ°ΫβΘΜ
(5)ΒΦΙή≤ε»κ“ΚΟφ“‘œ¬Ω…ΤπΒΫ“ΚΖβΉς”ΟΘ§Ζά÷ΙΩ’ΤχΫχ»κ»ΐΨ±…’ΤΩ―θΜ·Fe2+ΘΜ
¥πΑΗΈΣΘΚ“ΚΖβΉς”ΟΘ§Ζά÷ΙΩ’ΤχΫχ»κ»ΐΨ±…’ΤΩ―θΜ·ΘΜ
(6)―«ΧζάκΉ””κΥα–‘ΗΏΟΧΥαΦΊΖΔ…ζ![]() n(KMnO4)=0.01LΓΝ0.1mol/L=0.001molΘ§‘ρ20.00mL»ή“Κ÷–n(Fe2+)=0.005molΘ§‘ρ10.0g―υΤΖ÷–
n(KMnO4)=0.01LΓΝ0.1mol/L=0.001molΘ§‘ρ20.00mL»ή“Κ÷–n(Fe2+)=0.005molΘ§‘ρ10.0g―υΤΖ÷–![]() ΒΡΈο÷ ΒΡΝΩΈΣ0.025molΘ§―υΤΖΒΡΚ§ΝΩΈΣ
ΒΡΈο÷ ΒΡΝΩΈΣ0.025molΘ§―υΤΖΒΡΚ§ΝΩΈΣ![]() ΘΜ
ΘΜ
Ι ¥πΑΗΈΣΘΚ![]() ΘΜ98%ΓΘ
ΘΜ98%ΓΘ


 Ή÷¥ ΨδΤΣ”κΆ§≤ΫΉςΈΡ¥ο±ξœΒΝ–¥πΑΗ
Ή÷¥ ΨδΤΣ”κΆ§≤ΫΉςΈΡ¥ο±ξœΒΝ–¥πΑΗ
| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩH2O2ΉςΈΣ¬Χ…Ϊ―θΜ·ΦΝ±Μ”Π”Ο”ΎΖœΥ°¥ΠάμΓΔ‘λ÷ΫΚΆΜ·―ßΚœ≥…Β»––“ΒΓΘ
Θ®1Θ©“―÷ΣΘΚH2(g)+![]() O2(g)=H2O(l) ΠΛH1=Θ≠285.8kJΓΛmol-1
O2(g)=H2O(l) ΠΛH1=Θ≠285.8kJΓΛmol-1
H2(g)+O2(g)=H2O2(l) ΠΛH2=Θ≠135.8kJΓΛmol-1
ΔΌH2(g)”κO2(g)ΒΡΖ¥”Π÷–Θ§‘Ύ»»ΝΠ―ß…œΗϋ”–άϊΒΡ≤ζΈο «__Θ§‘≠“ρ «__ΓΘ
ΔΎ≥ΘΈ¬œ¬Θ§H2O2Ζ÷ΫβΒΡ»»Μ·―ßΖΫ≥Χ ΫΈΣ__ΓΘ
Θ®2Θ©Έ“ΙζΩΤ―ßΦ“ Ι”ΟAg9Ά≈¥ΊΉς¥ΏΜ·ΦΝΘ§―–ΨΩH2O2ΒΡΚœ≥…ΓΘΗς≤Ϋ÷ηΒΡΜνΜ·ΡήΚΆΖ¥”Π»»Θ§»γ±μΥυ ΨΘ§άϊ”ΟΦΤΥψΜζΡΘΡβΖ¥”Πάζ≥Χ»γΆΦΥυ ΨΘ®TS±μ ΨΙΐΕ…Χ§Θ§±μ Ψ±Μ¥ΏΜ·ΦΝΈϋΗΫΒΡΈο÷÷Θ©ΓΘ
Ag9Ά≈¥Ί…œ…ζ≥…H2O2ΒΡΜνΜ·ΡήEaΚΆΖ¥”Π»»![]()
≤Ϋ÷η | ΙΐΕ…Χ§ | Ea/kJ |
| |
A | Ag9 | TS1 | 74.1 | +68.7 |
B | HΓΣAg9 | TS2 | 108.7 | -27.2 |
C | HΓΣAg9ΓΣH+ O2 | TS3 | 78.4 | -75.4 |
D | HOO | TS4 | 124.7 | +31.3 |

ΔΌΆ®ΙΐΫΒΒΆ≤Ϋ÷η___Θ®ΧνΉ÷ΡΗΘ©ΒΡΡήάίΘ®ΜνΜ·ΡήΘ©Θ§Ω…“‘Ϋœ¥σΖυΕ»ΧαΗΏΚœ≥…Ζ¥”ΠΒΡΥΌ¬ ΓΘ
ΔΎΖ¥”Πάζ≥Χ÷–2ΒΫ3ΕœΝ―ΒΡΜ·―ßΦϋΈΣ___Θ®Χν–ρΚ≈Θ©ΓΘ
A.O2÷–ΒΡ―θ―θΦϋ B.H2÷–ΒΡ«β«βΦϋ C.Ag9OOH÷–ΒΡ―θ«βΦϋ
Θ®3Θ©άϊ”Ο“θ―τΦΪΆ§≤ΫΖ≈Βγ≤ζ…ζH2O2ΚΆΙΐΝρΥαοß[(NH4)2S2O8]ΒΡ‘≠άμ»γΆΦΥυ ΨΓΘ―τΦΪ…œΖ≈ΒγΒΡάκΉ” «___Θ§“θΦΪΒΡΒγΦΪΖ¥”Π ΫΈΣ___ΓΘ

Θ®4Θ©≥ΘΈ¬œ¬Θ§H2O2Ζ÷ΫβΥΌ¬ ΖΫ≥Χv=0.0625ΓΛc(H2O2)mgΓΛL-1ΓΛs-1Θ§c(H2O2)Υφ ±Φδ±δΜ·»γœ¬±μΘΚ
C(H2O2) (mg | 10000.0 | 8000.0 | 4000.0 | 2000.0 | 1000.0 |
Ζ÷Ϋβ ±Φδ(s) | 0 | 7 | 23 | 39 | 55 |
ΔΌΒ±c(H2O2)=8000.0mgΓΛL-1 ±Θ§v=__mgΓΛL-1ΓΛs-1ΘΜ
ΔΎΒ±c(H2O2)ΫΒΈΣ5000.0mgΓΛL-1 ±Θ§Ζ÷Ϋβ ±ΦδΈΣ___sΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΡ≥Ά§―ß≥Τ»Γ9.00gΒμΖέ»ή”ΎΥ°Θ§≤βΕ®ΒμΖέΒΡΥ°ΫβΑΌΖ÷¬ Θ°Τδ≥Χ–ρ»γœ¬ΘΚ
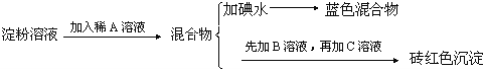
‘ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
Θ®1Θ©Ης≤ΫΦ”»κΒΡ ‘ΦΝΈΣΘΚA_________Θ§B_________Θ§C_________ΘΜ
Θ®2Θ©Φ”»κA»ή“ΚΕχ≤ΜΦ”»κB»ή“Κ «ΖώΩ…“‘_________Θ§Τδάμ”… «_________ΘΜ
Θ®3Θ©–¥≥ωΒμΖέΥ°ΫβΒΡΖΫ≥Χ Ϋ_________ΘΜ
Θ®4Θ©Β±Έω≥ω1.44gΉ©Κλ…Ϊ≥ΝΒμ ±Θ§ΒμΖέΥ°Ϋβ¬ «_________ΘΜ[“―÷ΣΤœΧ―Χ«”κCuΘ®OHΘ©2Ζ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΈΣΘΚCH2OHΘ®CHOHΘ©4CHO+2CuΘ®OHΘ©2![]() CH2OHΘ®CHOHΘ©4COOH+Cu2OΓΐ+2H2O]ΓΘ
CH2OHΘ®CHOHΘ©4COOH+Cu2OΓΐ+2H2O]ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ‘Ύ““ΥαΚΆ““¥ΦΒΡΖ¥”Π÷–Θ§≈®ΝρΥαΒΡΉς”Ο «
A.Ά―Υ°Ής”ΟB.¥ΏΜ·Ής”ΟC.¥ΏΜ·ΓΔΈϋΥ°Ής”ΟD.―θΜ·Ής”Ο
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ Β―ι ““‘Βγ ·Θ®÷ς“Σ≥…Ζ÷ «CaC2Θ©ΈΣ‘≠άμ÷Τ±Η““»≤Θ§ΉΑ÷Ο»γΆΦΥυ ΨΓΘΆξ≥…œ¬Ν–ΧνΩ’ΘΚ

Θ®1Θ©“«ΤςAΒΡΟϊ≥Τ «______________ΓΘ
Θ®2Θ© Β―ι “÷Τ»Γ““»≤ΒΡΜ·―ßΖΫ≥Χ ΫΈΣΘΚ___________________________________ ΓΘ
Θ®3Θ©ΈΣ±ήΟβΒγ ·ΚΆΥ°Ζ¥”ΠΙΐ”ΎΦΛΝ“Θ§≥ΐ”Ο±ΞΚΆ ≥―ΈΥ°¥ζΧφΥ°ΆβΘ§ΜΙ–η≤…»ΓΒΡ¥κ © «ΘΚ__________ΓΘ
Θ®4Θ©ΈΣ≥ΐ»Ξ““»≤÷–Μλ”–ΒΡ…ΌΝΩΝρΜ·«β‘”÷ Θ§Ω…ΫΪΤχΧεΆ®Ιΐ____________Θ®―ΓΧν±ύΚ≈Θ©ΓΘ
aΘ°Υα–‘KMnO4»ή“Κ bΘ°CCl4 cΘ°NaOH»ή“Κ
Θ®5Θ©““»≤ τ”Ύ_______________Θ®ΧνΓΑ±ΞΚΆΧΰΓ±ΜρΓΑ≤Μ±ΞΚΆΧΰΘ©ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΫΪagΡ≥Έο÷ ‘ΎΉψΝΩ―θΤχ÷–≥δΖ÷»Φ…’‘ΌΫΪΤχΧε…ζ≥…ΈοΆ®»κΉψΝΩΒΡNa2O2≥δΖ÷Ζ¥”ΠΘ§ΙΧΧε‘ω÷ΊΈΣbgΘ§»τa<bΘ§‘ρΗΟΈο÷ Ω…Ρή «Θ® Θ©
A. H2B. COC. ““Υα(CH3COOH)D. ΦΉΆι(CH4)
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ‘ΎΟή±’»ίΤς÷–Ϋχ––Ζ¥”Π:X(g)+3Y(g)![]() 2Z(g)Θ§”–ΙΊœ¬Ν–ΆΦœώΒΡΥΒΖ®¥μΈσΒΡ «
2Z(g)Θ§”–ΙΊœ¬Ν–ΆΦœώΒΡΥΒΖ®¥μΈσΒΡ «
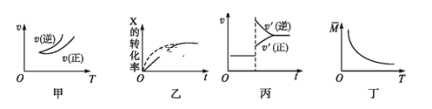
A.“άΨίΆΦΦΉΩ…≈–Εœ’ΐΖ¥”ΠΈΣΖ≈»»Ζ¥”Π
B.‘ΎΆΦ““÷–Θ§–ιœΏΩ…±μ Ψ Ι”ΟΝΥ¥ΏΜ·ΦΝ
C.»τ’ΐΖ¥”ΠΒΡΠΛH<0Θ§ΆΦ±ϊΩ…±μ Ψ…ΐΗΏΈ¬Ε» ΙΤΫΚβœρΡφΖ¥”ΠΖΫœρ“ΤΕ·
D.”…ΆΦΕΓ÷–ΤχΧεΤΫΨυœύΕ‘Ζ÷Ή”÷ ΝΩΥφΈ¬Ε»ΒΡ±δΜ·«ιΩωΘ§Ω…ΆΤ÷Σ’ΐΖ¥”ΠΒΡΠΛH>0
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ![]() «ΑΔΖϋΌΛΒ¬¬ό≥Θ ΐΒΡ÷ΒΘ§œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «( )
«ΑΔΖϋΌΛΒ¬¬ό≥Θ ΐΒΡ÷ΒΘ§œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «( )
A.23 g Na‘Ύ―θΤχ÷–≥δΖ÷»Φ…’…ζ≥…![]() Θ§ΉΣ“ΤΒγΉ” ΐΈΣ2
Θ§ΉΣ“ΤΒγΉ” ΐΈΣ2![]()
B.![]() ΒΡNaOH»ή“Κ÷–Θ§Κ§”–
ΒΡNaOH»ή“Κ÷–Θ§Κ§”–![]() ΒΡ ΐ»’ΈΣ0.01
ΒΡ ΐ»’ΈΣ0.01![]()
C.ΒγΉ” ΐΈΣ![]() ΒΡ
ΒΡ![]() Ζ÷Ή”ΒΡ÷ ΝΩΈΣ1.6g
Ζ÷Ή”ΒΡ÷ ΝΩΈΣ1.6g
D.±ξΉΦΉ¥Ωωœ¬Θ§3.36 LΒΡ![]() ÷–Κ§”–―θ‘≠Ή”ΒΡ ΐΡΩΈΣ0.45
÷–Κ§”–―θ‘≠Ή”ΒΡ ΐΡΩΈΣ0.45![]()
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–άκΉ”ΖΫ≥Χ Ϋ’ΐ»ΖΒΡ «![]()
![]()
A. œρΚ§2molFeBr2ΒΡ»ή“Κ÷–Ά®»κ2molCl2ΘΚ2Fe2++Cl2®T2Cl-+2Fe3+
B. œρ2molNaAlO2»ή“Κ÷–ΒΈΦ”5molHCl»ή”ΎΥ°÷–ΘΚ2AlO2- + 5H+ = Al3+ + Al(OH)3Γΐ+ H2O
C. œρBa(OH)2»ή“Κ÷–ΒΈΦ”NaHSO4»ή“Κ÷Ν÷––‘ΘΚBa2++OH-+H++SO42-®TBaSO4Γΐ+H2O
D. Άυ«β―θΜ·ΡΤ»ή“Κ÷–Ά®»κ…ΌΝΩSO2”κΥ°Ζ¥”ΠOH- + SO2 = HSO3-
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΑΌΕ»÷¬–≈ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com