
| A、可用NaOH溶液除去乙酸乙酯中混有的少量乙酸和乙醇 |
| B、可用水区别四种有机溶剂:苯、四氯化碳、己烯、无水乙醇 |
| C、淀粉水解的最终产物能与新制的氢氧化铜悬浊液反应生成砖红色的沉淀 |
| D、蒸馏“地沟油”可以获得甘油 |


科目:高中化学 来源: 题型:
| A、基态原子第四电子层只有2个电子,则该原子第三电子层的电子数肯定为8或18个 | ||
| B、Li、Be、B三种元素的第一电离能(I1)差别不大,而I2差别很大,则三种原子中最难失去第二个电子的是Be | ||
C、R为第二周期元素,其原子具有的电子层数为最外层电子数的
| ||
| D、核外电子数为奇数的基态原子,其原子轨道中一定含有未成对电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ni:[Ar]3d8 |
| B、Cu:[Ar]3d94s2 |
| C、S2-:[Ne]2s23p6 |
| D、Si:[Ne]3s23p2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
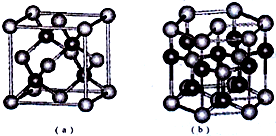 已知:周期表中前四周期的六种元素A、B、C、D、E、F核电荷数依次增大,其中A原子核外有三个未成对电子;化合物B2E的晶体为离子晶体,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的熔点在同周期元素形成的单质中是最高的;F2+离子核外各层电子均充满.请根据以上信息,回答下列问题:
已知:周期表中前四周期的六种元素A、B、C、D、E、F核电荷数依次增大,其中A原子核外有三个未成对电子;化合物B2E的晶体为离子晶体,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的熔点在同周期元素形成的单质中是最高的;F2+离子核外各层电子均充满.请根据以上信息,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
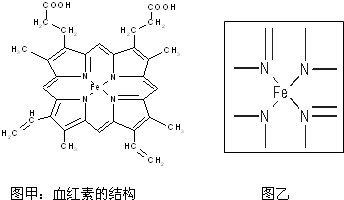
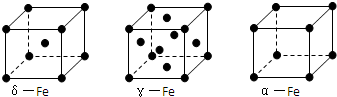
查看答案和解析>>
科目:高中化学 来源: 题型:
A、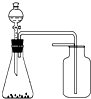 选择合适的试剂,装置可分别制取少量CO2、NO和O2 |
B、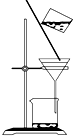 洗涤沉淀时(如图),向漏斗中加适量水,搅拌并滤干 |
| C、制备乙酸乙酯时,向乙醇中缓慢加入浓硫酸和冰醋酸 |
| D、用广泛pH试纸测得0.10 mol?L-1 NH4Cl溶液的pH=5.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、除去乙酸乙酯中的乙酸,可以用饱和的碳酸钠溶液 |
| B、配制溶液时,俯视刻度线来定容,会使得所配溶液浓度偏高 |
| C、用托盘天平称取8.7克食盐 |
| D、实验室可以用新制氢氧化铜悬浊液来检验甘油,观察到的现象是出现绛蓝色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com