
下列对各组物质性质的比较中,正确的是 ( )。
A.熔点:Li<Na<K
B.导电性:Ag>Cu>Al>Fe
C.密度:Na>Mg>Al
D.空间利用率:体心立方堆积<六方最密堆积<面心立方最密堆积
科目:高中化学 来源: 题型:
COCl2(g)CO(g)+Cl2(g) ΔH>0。当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO的浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是( )
A.①②④ B.①④⑥
C.②③⑥ D.③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
喷水溶液法是科学家近期研制出的一种使沙漠变绿洲的新技术。它是先在沙漠中喷洒一定量的聚丙烯酸酯(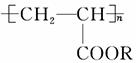 )“水溶液”,“水溶液”中的高分子化合物与沙土粒子相结合,在地表下30~50 cm处形成一个厚0.5 cm的隔水层,既能阻止地下的盐分上升,又有拦截蓄积雨水的作用。下列关于聚丙烯酸酯的说法中,不正确的是 ( )。
)“水溶液”,“水溶液”中的高分子化合物与沙土粒子相结合,在地表下30~50 cm处形成一个厚0.5 cm的隔水层,既能阻止地下的盐分上升,又有拦截蓄积雨水的作用。下列关于聚丙烯酸酯的说法中,不正确的是 ( )。
A.合成它的小分子化合物是CH3—CH2—COOR
B.它可由CH2==CH—COOR经过加成聚合反应而得到
C.在一定条件下能发生水解反应
D.不能发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
将0.48 g Mg粉加入到500 mL 0.1 mol·L-1的硝酸中恰好完全反应,则还原产物可能是 ( )。
A.NO2 B.NO
C.N2O3 D.NH
查看答案和解析>>
科目:高中化学 来源: 题型:
高锰酸钾分别在酸性、中性、碱性条件下发生的反应如下:
MnO +5e-+8H+===Mn2++4H2O
+5e-+8H+===Mn2++4H2O
MnO +3e-+2H2O===MnO2↓+4OH-
+3e-+2H2O===MnO2↓+4OH-
MnO +e-===MnO
+e-===MnO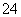 (溶液呈绿色)
(溶液呈绿色)
(1)从上述三个半反应中可以看出高锰酸根离子被还原的产物受溶液的________影响。
(2)将SO2通入高锰酸钾溶液中,发生还原反应的离子反应过程为________________________________________________________。
(3)将PbO2投入酸性MnSO4溶液中搅拌,溶液变为紫红色。下列说法正确的是________(填序号)。
a.氧化性:PbO2>KMnO4
b.还原性:PbO2>KMnO4
c.MnSO4溶液可以用盐酸酸化
查看答案和解析>>
科目:高中化学 来源: 题型:
在核电荷数1~18的元素中,其单质属于金属晶体的有____________________;金属中,密度最小的是________,地壳中含量最多的金属元素是________,熔点最低的是________,既能与酸反应又能碱反应的是________,单质的还原性最强的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于蛋白质和氨基酸的说法中,错误的是( )
A.蛋白质降解生成氨基酸属于分解反应
B.可用浓HNO3来鉴别蛋白质和淀粉
C.氨基酸既能与盐酸又能与氢氧化钠溶液反应
D.可采用渗析的方法来除去蛋白质溶液中的氨基酸
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室用燃烧法测定某种氨基酸(CxHyOzNp)的分子组成,取Wg该种氨基酸放在纯氧中充分燃烧,生成CO2、H2O和N2。现用下图所示装置进行实验 (铁架台、铁夹、酒精灯等未画出)。请回答有关问题:
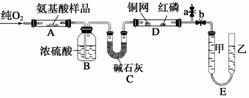
(1)实验开始时,首先打开止水夹a,关闭止水夹b,通入一段时间的氧气,这样做的目的是____________________________,之后关闭止水夹a。
(2)由装置B、C可分别确定待测氨基酸中含有的________和________的质量。
(3)E装置的作用是测量________的体积,并由此确定待测氨基酸中含有的____________的质量,为了较准确地测量该气体的体积,在读反应前后甲管液面的读数求其差值的过程中,应注意________(填序号)。
a.视线与凹液面最低处相平
b.等待片刻,待乙管中液面不再上升时,立刻读数
c.读数时应上下移动乙管,使甲、乙管液面相平
d.读数时不一定使甲、乙两管液面相平
(4)实验中测定的哪一数据可能不准确
________________________________________________________________________,
其理由是
________________________________________________________________________。
(5)严格地说,按上述方案只能确定氨基酸的________________。
若要确定此氨基酸的分子式,还要测定该氨基酸的____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
反应A(g)B(g)+C(g)在容积为1.0 L的密闭容器中进行,A的初始浓度为0.050 mol·L-1。温度T1和T2下A的浓度与时间关系如图所示。回答下列问题:
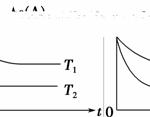
(1)上述反应的温度T1________T2,平衡常数K(T1)________K(T2)。(填“大于”、“小于”或“等于”)
(2)若温度T2时,5 min后反应达到平衡,A的转化率为70%,则:
①平衡时体系总的物质的量为_______________________________________。
②反应的平衡常数K=________________________________________。
③反应在0~5 min区间的平均反应速率v(A)=________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com