
通常把原子总数和价电子总数相同的分子或离子称为等电子体。人们发现等电子体的空间结构相同,则下列有关说法中正确的是( )
A.CH4和NH是等电子体,键角均为60°
B.NO和CO是等电子体,均为平面正三角形结构
C.H3O+和PCl3是等电子体,均为三角锥形结构
D.B3N3H6和苯是等电子体,B3N3H6分子中不存在“肩并肩”式重叠的轨道
科目:高中化学 来源:2016届福建省高三下学期周考五理科综合化学试卷(解析版) 题型:填空题
黄铜矿是炼铜的最主要矿物,在野外很容易被误会为黄金,又称愚人金。
(1)向CuSO4溶液中加入过量的氨水,可生成[Cu(NH3)4]SO4,下列说法正确的是
A.氨气极易溶于水,是因为NH3分子和水分子之间形成3种不同的氢键
B.[Cu(NH3)4]SO4组成元素中。N、O、S第一电离能大小顺序是O>N>S
C. [Cu(NH3)4]SO4所含有的化学键有离子键、极性键和配位键
D. NH3分子和H2O分子的空间构型不同,且氨气分子的键角小于水分子的键角
(2)Te位于周期表中__________族,H2Te比H2S沸点__________(填“高”或“低”)。某处于激发态的S原子,其中1个3s电子跃迁到3p轨道中,该激发态S原子的核外电子排布式为__________。
(3)S有+4和+6两种价态的氧化物,回答下列问题:
①下列关于气态SO3和SO2的说法中,正确的是__________
A.中心原子的价层电子对数目相等 B.都是极性分子
C.中心原子的孤对电子数目相等 D.都含有极性键
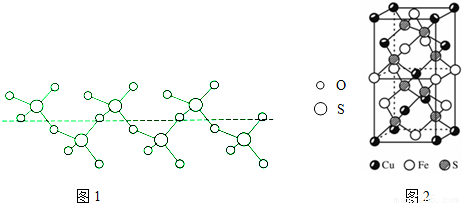
②将纯液态SO3冷却到289.8K时凝固得到一种螺旋状单链结构的固体,其结构如图1,此固态SO3中S原子的杂化轨道类型是__________。
(4)Cu有+1和+2两种价态的化合物,回答下列问题:
①Cu+的价层轨道示意图为__________,Cu2+有__________个未成对电子.
②新制的Cu(OH)2能够溶解于过量浓碱溶液中,反应的离子方程式是
(5)CuFeS2的晶胞如图2所示,晶胞参数a=0.524nm,c=1.032nm;CuFeS2的晶胞中每个Cu原子与__________个S原子相连,列式计算晶体密度 ρ= __________g•cm-3.
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁鞍山一中高二下期中化学试卷(解析版) 题型:选择题
下列有关说法不正确的是
A.共价键强弱可决定分子晶体的熔、沸点高低
B.O2、CO2、N2都是非极性分子
C.C3H8中碳原子都采用的是sp3杂化
D.CO的一种等电子体为NO+,它的电子式为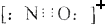
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州省高二下期中化学试卷(解析版) 题型:填空题
已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。其中A、B、C是同一周期的非金属元素。化合物DC为离子化合物,D的二价阳离子与C的阴离子具有相同的电子层结构。AC2为非极性分子。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E的原子序数为24,ECl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2∶1,三个氯离子位于外界。请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C的第一电离能由小到大的顺序为________。
(2)B的氢化物的分子空间构型是________;其中心原子采取________杂化。
(3)一种由B、C组成的化合物与AC2互为等电子体,其化学式为________。
(4)ECl3形成的配合物的化学式为________。
(5)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是______________________________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州省高二下期中化学试卷(解析版) 题型:选择题
氯化硼(BCl3)的熔点为-107℃,沸点为12.5℃,在其分子中键与键之间的夹角为120°,它能水解,有关叙述正确的是( )
A.氯化硼液态时能导电而固态时不导电 B.硼原子以sp杂化
C.氯化硼遇水蒸气会产生白雾 D.氯化硼分子属极性分子
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州省高二下期中化学试卷(解析版) 题型:选择题
按电子排布,可把周期表里的元素划分成5个区,以下元素属于p区的是( )
A.Fe B.Mg C.Br D.Cu
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃会宁一中高一下期中文科化学试卷(解析版) 题型:选择题
在理论上不能用于设计成原电池的化学反应是( )
A.HCl + NaOH = NaCl + H2O B.2CH3OH + 3O2= 2CO2 + 4H2O
C.4Fe(OH)2 + 2H2O + O2 = 4Fe(OH)3 D.2H2 + O2 = 2H2O
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃会宁一中高一下期中理科化学试卷(解析版) 题型:填空题
某温度时,在2 L容器中A、B两种物质间的转化反应中A、B物质的量随时间变化的曲线如图所示,由图中数据分析得:
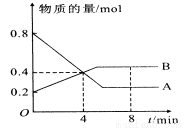
(1)该反应的化学方程式为______________________________。
(2)反应开始时至4 min时,A的平均反应速率为________。
(3)4min时,反应是否达平衡状态?________(填“是”或“否”),8min时,V正________V逆(填“>”“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建师大附中高一下期中化学试卷(解析版) 题型:选择题
1.52g铜镁合金完全溶解于50mL密度为1.40g/mL、质量分数为63%的浓硝酸中,得到NO2和N2O4 的混合气体1120mL(标准状况),向反应后的溶液中加入1.0 mol/LNaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀。下列说法不正确的是( )
A.该合金中铜与镁的物质的量之比是2:1
B.该浓硝酸中HNO3的物质的量浓度是14.0mol/L
C.NO2和N2O4的混合气体中,NO2的体积分数是80%
D.得到2.54g沉淀时,加入NaOH溶液的体积是600mL
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com