
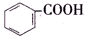
 >H2CO3>
>H2CO3>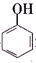 >HCO${\;}_{3}^{-}$,现将
>HCO${\;}_{3}^{-}$,现将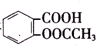 转变为
转变为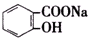 ,可行的方法是( )
,可行的方法是( )| A. | 向该溶液中加入足量的稀硫酸,加热 | |
| B. | 将该物质与稀硫酸共热后,再加入足量的NaOH溶液 | |
| C. | 将该物质与稀硫酸共热后,再加入足量的Na2CO3溶液 | |
| D. | 将该物质与足量的NaOH溶液共热,再通入足量CO2气体 |
分析 要将 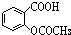 转变为
转变为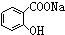 ,
,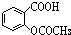 应先在碱性条件下水解生成
应先在碱性条件下水解生成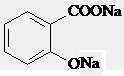 ,由于酸性关系:
,由于酸性关系: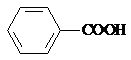
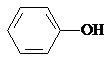
 ,此外
,此外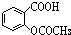 在酸性条件下水解生成
在酸性条件下水解生成 ,根据酸性:
,根据酸性: >HCO3-,加入足量的NaHCO3后生成
>HCO3-,加入足量的NaHCO3后生成 也是可以的.
也是可以的.
解答 解:A.向该溶液中加入足量的稀硫酸,加热,酯基水解生成酚羟基,但羧基不能生成-COONa,故A错误;
B.将该物质与稀硫酸共热后,酯基水解生成酚-OH,羧基、酚羟基都和NaOH反应,所以生成的是-ONa、-COONa,不能实现实验目的,故B错误;
C.将该物质与稀硫酸共热后,酯基水解生成酚-OH,羧基、酚羟基都和Na2CO3反应,所以生成的是-ONa、-COONa,不能实现实验目的,故C错误;
D.与足量NaOH溶液共热,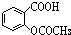 与氢氧化钠溶液反应生成
与氢氧化钠溶液反应生成 ,再通入足量CO2,由于酸性
,再通入足量CO2,由于酸性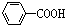 >H2CO3>
>H2CO3>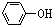 >HCO3-,所以二氧化碳与
>HCO3-,所以二氧化碳与 反应生成
反应生成 ,故D正确;
,故D正确;
故选D.
点评 本题考查有机物结构和性质,明确官能团及其性质关系是解本题关键,注意酚羟基和碳酸钠反应但和碳酸氢钠不反应,为易错点.


 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

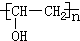 ;检验B常用的试剂为银氨溶液或新制氢氧化铜悬浊液;
;检验B常用的试剂为银氨溶液或新制氢氧化铜悬浊液;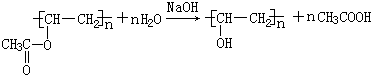 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
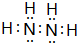 ,Z由两个相同基团构成,该基团的名称是羟基.
,Z由两个相同基团构成,该基团的名称是羟基.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 吸入氯气、氯化氢气体时,可吸入少量酒精或乙醚的混合蒸气解毒 | |
| B. | 移液管放液时,将移液管稍倾斜放入直立的容器中,并使管尖与容器内壁接触,松开食指使溶液全部流出,数秒后,取出移液管 | |
| C. | 生物体死亡后,体内含有的碳-14会逐渐减少,因此可通过测量生物体遗骸中碳-14的含量,来计算它存活的年代.碳-14减少的变化为化学变化 | |
| D. | 当用电解法除去溶液中的Cr2O72-离子时,因其具有强氧化性易得电子,故可在阴极直接放电生成Cr3+,最后生成Cr(OH)3沉淀除去 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 自来水厂常用氯气给自来水消毒 | |
| B. | 澄清石灰可用于水鉴别Na2CO3和NaHCO3溶液 | |
| C. | 合金的机械性能一般比组分金属好,但有可能更加容易被腐蚀 | |
| D. | 加碘盐是在食盐中加入一定量的碘酸钾,以确保人体对碘的摄入量,可预防甲状腺肿大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水、二氧化硫和干冰都属氧化物 | B. | H2SO4、HNO3和H2CO3都属于酸 | ||
| C. | KNO3、CuSO4和NH4Cl都属于盐 | D. | 烧碱、纯碱、熟石灰都属于碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3COOH与C6H5COOH为同系物 | |
| B. | 戊烷比丙烷的沸点高 | |
| C. | 烷烃的化学性质与甲烷类似,通常较稳定 | |
| D. | 用燃烧法可鉴别甲烷和乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
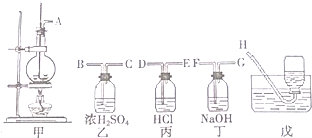
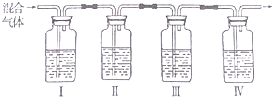
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com