
����Ŀ���±�ΪԪ�����ڱ���һ���֣������Ԫ�آ١����ڱ��е�λ�ã��ش��������⣺ 
��1���ؿ��к�����ߵĽ���Ԫ�������ڱ��е�λ���� ��
��2�����γɵĵ�����ˮ��Ӧ�����ӷ���Ϊ ��
��3���ڢߵķǽ�����ǿ����ͨ���Ƚ�������Ԫ�������ţ�
a��ԭ�ӵĵõ��ӵ����� b�������������
c����̬�⻯����ȶ��� d�����ʵ��۷е�
��4��д��һ���ɢܢݢ�Ԫ���γɵļȺ������Ӽ��ֺ��й��ۼ������ʵĵ���ʽ ��
��5��������ҵ����ϳ�����Ԫ�آں͢��γɵĻ������Ӳ�ȱȽ��ʯ�����������γɵľ��廹���ܾ��е����ʻ��ص��������ţ�
���۵�ܸ� �ڿ��Ե��� �۲����ڵ������� �ܾ��пռ���״�ṹ
��6���ٺ͢��γɵ�ijҺ̬������Ħ��������������ͬ���ڳ��³�ѹ��0.25mol��Һ̬��������������������ȫȼ�����ɢ۵���̬���ʺ�Һ̬ˮ��ͬʱ�ų�QkJ��������д���÷�Ӧ���Ȼ�ѧ����ʽ ��
���𰸡�
��1���������ڢ�A��
��2��Cl2+H2OHClO+H++Cl��
��3��a��c
��4��![]()
��5���٢ۢ�
��6��N2H4��l��+O2��g���TN2��g��+2H2O��l����H=��4Q kJmol��1
���������⣺��1���ؿ��к�����ߵĽ���Ԫ�������������ڱ��е�λ���ǵ������ڢ�A�壬�ʴ�Ϊ���������ڢ�A�壻��2��������ˮ��Ӧ�����ӷ���ΪCl2+H2OHClO+H++Cl�� �� �ʴ�Ϊ��Cl2+H2OHClO+H++Cl������3��Ԫ�صķǽ�����Խǿ��ԭ�ӵĵõ��ӵ�������Խǿ����۵ĺ���������Ծ�Խǿ����̬�⻯����ȶ���ҲԽǿ������a��c��ȷ��
�ʴ�Ϊ��a��c����4���ɢܢݢ�Ԫ���γɵļȺ������Ӽ��ֺ��й��ۼ�������ΪNaClO�ȣ������ʽΪ ![]() ��
��
�ʴ�Ϊ�� ![]() ����5����Ԫ�آں͢��γɵĻ������Ӳ�ȱȽ��ʯ��������������γɵľ���Ϊԭ�Ӿ��壬����ԭ�Ӿ��ݿ�֪���������۵�ܸߡ������ڵ������ӡ����пռ���״�ṹ��ԭ�Ӿ���һ�㲻���磬
����5����Ԫ�آں͢��γɵĻ������Ӳ�ȱȽ��ʯ��������������γɵľ���Ϊԭ�Ӿ��壬����ԭ�Ӿ��ݿ�֪���������۵�ܸߡ������ڵ������ӡ����пռ���״�ṹ��ԭ�Ӿ���һ�㲻���磬
��ѡ���٢ۢܣ���6���ٺ͢��γɵ�ijҺ̬������Ħ��������������ͬ���������ΪN2H4 �� �ڳ��³�ѹ��0.25mol��Һ̬��������������������ȫȼ�����ɵ�����Һ̬ˮ��ͬʱ�ų�QkJ����������1molN2H4��Ӧ�ɷų�4QkJ���������÷�Ӧ���Ȼ�ѧ����ʽΪ��N2H4��l��+O2��g���TN2��g��+2H2O��l����H=��4Q kJmol��1 ��
�ʴ�Ϊ��N2H4��l��+O2��g���TN2��g��+2H2O��l����H=��4Q kJmol��1 ��
��Ԫ�������ڱ��е�λ�ÿ�֪������H������C������N������O������Na������Al������Si������Cl����1���ؿ��к�����ߵĽ���Ԫ��Ϊ��Ԫ�أ���2�����γɵĵ���Ϊ������������ˮ��Ӧ��������ʹ������3��Ԫ�صķǽ�����Խǿ��ԭ�ӵĵõ��ӵ�������Խǿ����۵ĺ���������Ծ�Խǿ����̬�⻯����ȶ���ҲԽǿ����4���ɢܢݢ�Ԫ���γɵļȺ������Ӽ��ֺ��й��ۼ�������ΪNaClO�ȣ���5����Ԫ�آں͢��γɵĻ������Ӳ�ȱȽ��ʯ��������������γɵľ���Ϊԭ�Ӿ��壬����ԭ�Ӿ��ݿ��ܾ��е����ʻ��ص��жϣ���6���ٺ͢��γɵ�ijҺ̬������Ħ��������������ͬ���������ΪN2H4 �� �ڳ��³�ѹ��0.25mol��Һ̬��������������������ȫȼ�����ɵ�����Һ̬ˮ��ͬʱ�ų�QkJ����������1molN2H4��Ӧ�ɷų�4QkJ��������ע�����ʵľۼ�״̬�뷴Ӧ����д�Ȼ�ѧ����ʽ��


 ͬ����ϰ���ϴ�ѧ������ϵ�д�
ͬ����ϰ���ϴ�ѧ������ϵ�д� ͬ����ϰ����ʦ����ѧ������ϵ�д�
ͬ����ϰ����ʦ����ѧ������ϵ�д� ����ϰ�⽭��ϵ�д�
����ϰ�⽭��ϵ�д� ѧ���쳵��������������������ϵ�д�
ѧ���쳵��������������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�ǵ��CuCl2��Һ��װ�ã�����c��dΪʯī�缫���������й��ж���ȷ����( )
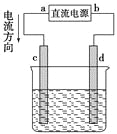
A. a������b����
B. a������b����
C. �������У�d�缫��������
D. �������У�������Ũ�Ȳ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A. ʹ��pH��ֽ��������������ʱ������ʪ
B. ʵ����������������Һ��ȥ�����е�����HCl
C. �������ʱ���¶ȼ�ˮ����Ӧ������Һ��
D. ������Һ����ʱ����������ƿ�Ŀ̶��ߣ�����������Һ��Ũ��ƫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֤������Ϊǿ���ʵ����ʵ��
A. �������ָʾ������ B. 0.1mol/L�������У����c(H+)=0.2mol/L
C. �������п��Ӧ�������� D. ����ʳ�ι��干�Ȳ��������Ȼ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£����и���������ָ����Һ���ܴ����������(����)
A. ���ܽ�����������Һ�У�K����NH![]() ��HCO
��HCO![]() ��NO
��NO![]()
B. c(OH��)Ϊ1��10��12 mol��L��1����Һ�У�Na����Al3����I����SiO![]()
C. �����̪�Ժ�ɫ����Һ�У�Na����AlO![]() ��SO
��SO![]() ��Cl��
��Cl��
D. ����KNO3����Һ�У�Fe2����H����Cl����SO![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�ǵ��CuCl2��Һ��װ�ã�����c��dΪʯī�缫���������й��ж���ȷ����( )
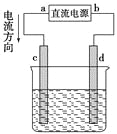
A. a������b����
B. a������b����
C. �������У�d�缫��������
D. �������У�������Ũ�Ȳ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�ֺ��ᾧˮ����ɫ����ɱ�ʾΪAnH2O�����нᾧˮ����������Ϊ28.57%���þ������ˮ��A��̼���⡢������Ԫ�ص����������ֱ�Ϊ26.67%��2.23%��71.1%��
�Իش��������⣺
��1������ˮ��A�����ʽ��
��2��A��NaOH��Һ�����кͷ�Ӧ��������ʽ�κ�һ�����Σ�0.9g��ˮ��Aǡ�ú�0.1molL��1NaOH��Һ200mL��ȫ��Ӧ�������Σ���û�����A�ķ���ʽ����ṹ��ʽ������ʾ����COOH��һ�����Թ����ţ�����д��������A������NaOH��Ӧ�Ļ�ѧ����ʽ
��3����AnH2O��n��ֵ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(���14��)ij��(H)��һ�ֺϳɶ��������м��壬��������·�ߺϳ�(���ַ�Ӧ������ȥ)��
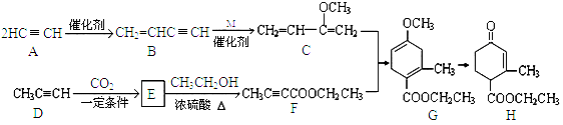
��1��A��B�ķ�Ӧ������ ��B��CΪ�ӳɷ�Ӧ������M�Ľṹ��ʽ�� ��
��2��H�г����ʻ�(![]() )�⣬���еĹ����������� ��
)�⣬���еĹ����������� ��
��3��ʵ������A�Ļ�ѧ����ʽΪ ��
��4��E�� F�Ļ�ѧ����ʽ�� ��
��5������˵����ȷ���� ��
a. D��F�о�����Ȳ��������
b. A�ܺ�HCl��Ӧ�õ�������ϩ�ĵ���
c. 1mol G��ȫȼ������7mol H2O
d. H�ܷ����ӳɡ�ȡ����Ӧ
��6��TMOB��H��ͬ���칹�壬�������нṹ�������ٺ˴Ź������ױ����������г������⣬������ԭ�ӻ�ѧ������ͬ���ڴ��ڼ�����(CH3O-)��TMOB�Ľṹ��ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��25 ��ʱ�� Kb(NH3��H2O)��1.8��10��5�� ���¶��£��� 0.100mol��L��1 �İ�ˮ�ζ� 10.00 mL 0.100mol��L��1 ��һԪ�� HA ����Һ�� �ζ������м��백ˮ�������V������Һ�� �Ĺ�ϵ��ͼ��ʾ������˵������ȷ����

A. HA Ϊǿ��
B. a��10
C. 25 ��ʱ��NH4����ˮ��ƽ�ⳣ��Ϊ![]()
D. ������ 20 mL ��ˮʱ����Һ�д��� c(NH4��)��c(A��)
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com