
| A.化合价 | B.原子半径 | C.最外层电子排布 | D.相对原子质量 |
科目:高中化学 来源:不详 题型:单选题
| A.由14N2和15N2组成的物质是混合物 |
| B.在常温常压下,11.2L氧气所含的原子数目为NA |
| C.第三周期的元素从左往右非金属性逐渐增强 |
| D.电解MgCl2饱和溶液,可制得金属镁 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 离子化合物 | AB | CD | EF |
| 离子电荷数 | 1 | 1 | 2 |
| 键长(10-10m) | 2.31 | 3. 18 | 2.10 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 I健康相关知识答问”中指出,
I健康相关知识答问”中指出, I是人工放射性核素,正常情况下自然界中不会存在,日本核泄漏事故释放的放射性核素中含有这种核素。下列有关
I是人工放射性核素,正常情况下自然界中不会存在,日本核泄漏事故释放的放射性核素中含有这种核素。下列有关 I的叙述正确的是
I的叙述正确的是| A.是碘的一种同素异形体 | B.是一种新发现的元素 |
| C.核内的中子数与核外电子数之差为25 | D.位于元素周期表中第4周期ⅦA族 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.131I、132I、134Cs、137Cs是四种不同的核素 | B.食用碘盐不能防辐射 |
| C.碘片的主要成分是I2 | D.核能仍然是重要能源之一 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NaOH的碱性介于KOH和Mg(OH)2之间 |
| B.Li、Na、K、Rb元素金属性依次增强 |
| C.Na+、Mg2+、Al3+的离子半径依次增大 |
| D.H2SiO3、H2CO3、HClO4酸性依次增强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 物一定是离子化合物⑦所有的原子晶体都不导电
物一定是离子化合物⑦所有的原子晶体都不导电| A.①② | B.①⑥ | C.③④⑤ | D.⑥ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 元素 | 结构或性质信息 |
| M | M的一种单质是自然界最硬的物质 |
| Q | 基态原子最外层未成对电子数在该元素所在周期中最多 |
| Y | 单质常温、常压下是气体。基态原子的M层上有1个未成对的p电子 |
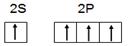 ,请判断对错,并加以解释
,请判断对错,并加以解释  电子式___________
电子式___________ 查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com