


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:阅读理解
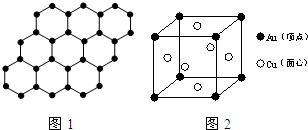 瑞典皇家科学院宣布,将2010年诺贝尔物理学奖授予 英国曼彻斯特大学科学家安德烈?海姆和康斯坦丁?诺沃肖洛夫,以表彰他们在石墨烯材料方面的卓越研究.石墨烯是由碳原子构成的单层片状结构的新材料.具有原子级的厚度、优异的电学性能、出色的化学稳定性和热力学稳定性.制备石墨烯方法有石墨剥离法、化学气相沉积法等.石墨烯的球棍模型及分子结构如图1所示.
瑞典皇家科学院宣布,将2010年诺贝尔物理学奖授予 英国曼彻斯特大学科学家安德烈?海姆和康斯坦丁?诺沃肖洛夫,以表彰他们在石墨烯材料方面的卓越研究.石墨烯是由碳原子构成的单层片状结构的新材料.具有原子级的厚度、优异的电学性能、出色的化学稳定性和热力学稳定性.制备石墨烯方法有石墨剥离法、化学气相沉积法等.石墨烯的球棍模型及分子结构如图1所示.查看答案和解析>>
科目:高中化学 来源:2012-2013年四川昭觉中学高二上学期期中考试化学试卷(带解析) 题型:单选题
下列对分子的性质的解释中,不正确的是
| A.水很稳定(1000℃以上才会部分分解),但与水中含有大量氢键无关 |
| B.[Cu(NH3)4]SO4和(NH4)2SO4两种物质中都有配位键,所以都是配合物 |
| C.碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶原理解释 |
| D.由下图知酸性:H3PO4>HClO,因为H3PO4的非羟基氧原子数大于次氯酸的非羟基氧原子数 |

查看答案和解析>>
科目:高中化学 来源:2014届四川昭觉中学高二上学期期中考试化学试卷(解析版) 题型:选择题
下列对分子的性质的解释中,不正确的是
A.水很稳定(1000℃以上才会部分分解),但与水中含有大量氢键无关
B.[Cu(NH3)4]SO4和(NH4)2SO4两种物质中都有配位键,所以都是配合物
C.碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶原理解释
D.由下图知酸性:H3PO4>HClO,因为H3PO4的非羟基氧原子数大于次氯酸的非羟基氧原子数

查看答案和解析>>
科目:高中化学 来源:专项题 题型:填空题
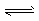 CH3CH2OH(g) +3H2O(g) △H=akJ.mol-1 在一定压强下,测得上述反应的实验数据如下表。
CH3CH2OH(g) +3H2O(g) △H=akJ.mol-1 在一定压强下,测得上述反应的实验数据如下表。 

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com