
����Ŀ����������ش�����
��1�������£��ڴ�ˮ�м���ijһԪ������NaAʹ��Һ��pH=9�������Һ��ˮ���������C��OH����=molL��1 �� KWֵ��������С�䣩��
��2����пƬ��ͭƬ�õ������Ӳ�������ͭ��Һʱ��пƬ���ͷŵĵ���������ͭƬ�������Ӵ��������������Ľ�����Ͻ�������е�ˮ��Һ�Ӵ�������ԭ��ط�Ӧ����ʴ�Ĺ����ǽ�����ʴ����Ҫ��ʽ�������������ˮĤ���Խ�ǿʱ������ʴ���为���ĵ缫��ӦʽΪ �� �����ĵ缫��ӦʽΪ �� ��ˮĤ���Ժ����������ʱ�������ĵ缫��ӦΪ ��
���𰸡�
��1��1��10��5������
��2�����ߣ������������⣻Fe��2e=Fe2+��2H++2e=H2����O2+4e+2H2O=4OH��
���������⣺��1������Һ�������Ӻ����������Ӿ���ˮ����ģ��ڴ�ˮ�м���ijһԪ������NaAʹ��Һ��pH=9����������Ũ��Ϊ1��10��9mol/L��C��OH����= ![]() =1��10��5mol/L��KWֻ���¶��йأ��¶Ȳ��䣬��KW��ֵ���䣻���Դ��ǣ�1��10��5�����䣻��2����пƬ��ͭƬ�õ������Ӳ�������ͭ��Һʱ��ZnΪ������CuΪ������ԭ����е��ӴӸ������ŵ���������������Һ�������ӴӸ����������������������£�Fe�������ⸯʴ������Feʧ���������������ӣ������ĵ缫��ӦʽΪFe��2e=Fe2+ �� ���������ӵõ������������������ĵ缫��ӦʽΪ��2H++2e=H2������ˮĤ���Ժ����������ʱ������������ʴ�������������õ����������������ӣ��������ĵ缫��ӦʽΪ��O2+4e+2H2O=4OH�������Դ��ǣ����ߣ������������⣻Fe��2e=Fe2+��2H++2e=H2����O2+4e+2H2O=4OH�� ��
=1��10��5mol/L��KWֻ���¶��йأ��¶Ȳ��䣬��KW��ֵ���䣻���Դ��ǣ�1��10��5�����䣻��2����пƬ��ͭƬ�õ������Ӳ�������ͭ��Һʱ��ZnΪ������CuΪ������ԭ����е��ӴӸ������ŵ���������������Һ�������ӴӸ����������������������£�Fe�������ⸯʴ������Feʧ���������������ӣ������ĵ缫��ӦʽΪFe��2e=Fe2+ �� ���������ӵõ������������������ĵ缫��ӦʽΪ��2H++2e=H2������ˮĤ���Ժ����������ʱ������������ʴ�������������õ����������������ӣ��������ĵ缫��ӦʽΪ��O2+4e+2H2O=4OH�������Դ��ǣ����ߣ������������⣻Fe��2e=Fe2+��2H++2e=H2����O2+4e+2H2O=4OH�� ��


 ��Уͨ��֤��Ч��ҵϵ�д�
��Уͨ��֤��Ч��ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A�Ƿ���ʽΪC7H8�ķ���������֪����������һϵ��ת����ϵ������C��һ��һԪ����D��A�Ķ�λһȡ���H��E��I��F�ֱ�Ϊͬ���칹�壺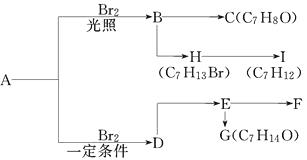
��1��������I�Ľṹ��ʽ�� ��
��ӦB��C�Ļ�ѧ����ʽ��.
��2�����ʵ��֤��H�к�����ԭ�ӣ������õ����Լ���.
��3��Ϊ��֤E��F�ķ�Ӧ������E��G��ͬ������ʵ�鷽����ʵ���е���_____________��
A.��E��F��Ӧ��Ļ��Һ�м��������ữ���ټ���AgNO3��Һ�õ�����ɫ����
B.��E��F��Ӧ��Ļ��Һ�м�����ˮ��������ˮ������ɫ
C.��E��F��Ӧ��Ļ��Һ�м��������ữ�������CCl4��Һ��ʹ֮��ɫ
D.��E��F��Ӧ��Ļ��Һ�м�������KMnO4��Һ�����Һ��ɫ��dz
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z��M��G����Ԫ�ط������������ڣ���ԭ��������������X��Zͬ���壬���γ����ӻ�����ZX��Y��Mͬ���壬���γ�MY2��MY3���ַ��ӣ���ش��������⣺
��1��Y��Ԫ�����ڱ��е�λ��Ϊ ��
��2������Ԫ�ص�����������Ӧ��ˮ����������ǿ������д��ѧʽ�����ǽ�����̬�⻯�ﻹԭ����ǿ������д��ѧʽ����
��3��Y��G�ĵ��ʻ���Ԫ��֮���γɵĻ��������ˮ������������д�������������ʵĻ�ѧʽ����
��4��ZX�ĵ���ʽΪ��ZX��ˮ��Ӧ�ų�����Ļ�ѧ����ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ij100mL�������Һ�У�HNO3��H2SO4�����ʵ���Ũ�ȷֱ�Ϊ0.4molL��1��0.2molL��1 �� ��û��Һ�м���1.92gͭ�ۣ����ȳ�ַ�Ӧ��������Һ��Cu2+�����ʵ���Ũ��Ϊ�� ��
A.0.15 molL��1
B.0.225 molL��1
C.0.3 molL��1
D.����ȷ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й����ʵ���������ȷ����
A. ����ˮ������Ƶ�������
B. ��ƿ�ʹϸ�������������ʱ��Զ�����
C. �����������Ի�����������Ӧ������
D. ��֬�����ܷ����ӳɷ�Ӧ��������һ�������·���ˮ�ⷴӦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ʵ�ˮ��Һ�ܵ��磬�����������ڷǵ���ʵ���
A. �Ȼ��� B. �ɱ� C. ���� D. ���ᱵ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Է�������ΪM����̬������vL����״����������mgˮ�У��õ���������Ϊw����Һ�����ʵ���Ũ��ΪcmolL��1 �� �ܶ�Ϊ��gcm��3 �� ������˵������ȷ���ǣ� ��
A.��Է�������M= ![]()
B.���ʵ���Ũ��c= ![]()
C.��������w= ![]()
D.��Һ�ܶȦ�= ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ס��������ڱ���ͬһ���������Ԫ�أ�����ԭ������ΪX�����ҵ�ԭ��������������( )
A.X+2B.X+4C.X+8D.X+18
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ������FeO��Fe2O3�Ļ�����м���120mL 4molL��1��ϡ���ᣬǡ��ʹ�������ȫ�ܽ⣬�ų�1.344L NO����״��������������Һ�м���KSCN��Һ����Ѫ��ɫ���֣����������������ڼ��������»�ԭ��ͬ�����Ļ����ܵõ��������ʵ���Ϊ�� ��
A.0.24 mol
B.0.21 mol
C.0.16 mol
D.0.14 mol
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com