
����Ŀ����ʯӢ����̿Ϊԭ�ϵIJ��ֻ���������ͼ��ʾ��

�ش��������⣺
(1)��ӦI�ڹ�ҵ�ϵ������������ֹ裬Ϊ������ƷR���Ƿ������������ʣ�ȡ����R����ϡ�����ܽ⣬ȡ�ϲ���Һ�����ټ�����Լ���______������ĸ����
a����ˮ b����ˮ c��KSCN��Һ d��NaCl��Һ
(2)��Ӧ��Ҫ�ڸ��ﻷ���±��У���ԭ����______���������õ���SiHCl3���е�Ϊ33.0�棩�к�������SiCl4�е�Ϊ57.6�棩��HC1���е�Ϊ- 84.7�棩�����ᴿSiHCl3�ķ���Ϊ______________��
(3)��ˮ����ͨ�����ȵ�ú�ۿɲ���ˮú��������Ҫ�ɷ���CO��H2����ҵ�Ͻ�ˮú��Һ�����Ƶõ�CH3OH�к��еĻ�ѧ������Ϊ________������Ӽ������ۼ�����������ͼ�еķ�Ӧ��Ϊ������ԭ��Ӧ���仯ѧ����ʽΪ_______________��
���𰸡� bc ��ֹ���ɵ�SiHCl3��ˮ��Ӧ ���� ���ۼ� SiHCl3+(n+2)H2O =SiO2��nH2O+ H2��+3HC1��
��������(1)���ƷR�к������������ʣ���ϡ�����ܽ����ϲ���Һ�к���Fe2+������ʱ��Ҫ�ȵμ�KSCN��Һ����ɫ���ٵμ���ˮ���ɫ���ʴ�Ϊbc��
(2)SiHCl3��ˮ�⣬��Ӧ��Ҫ�ڸ��ﻷ���½��У�Ŀ�ĵ�Ϊ�˷�ֹ���ɵ�SiHCl3��ˮ��Ӧ��SiHCl3��SiCl4���ڷе���죬������������������з����ᴿ��
(3)CH3OH�ǹ��ۻ����ֻ���й��ۼ�������ͼ�еķ�Ӧ��Ϊ������ԭ��Ӧ������SiHCl3��HԪ��Ϊ-1�ۣ��������ͼ�з�Ӧ������������ݵ����غ��ԭ���غ㼴�ɵõ���Ӧ����ʽΪSiHCl3+(n+2)H2O =SiO2��nH2O+ H2��+3HC1����


 �������ϵ�д�
�������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ũ��Ϊ0.1molL-1HF��Һ��ˮ����ϡ�ͣ����и���ʼ�ձ���������ǣ� ��
A��c(F��) B��Ka(HF) C��![]() D��
D��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�������£���C��s����H2O��g���ֱ����ס��������ܱ�������������Ӧ��C��s��+2H2O��g�� ![]() CO2��g��+2H2��g����������������±���ʾ��
CO2��g��+2H2��g����������������±���ʾ��
���� | �ݻ�/L | �¶�/�� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ���� ��ʱ��/min | |
C��s�� | H2O��g�� | H2��g�� | ||||
�� | 2 | T1 | 2 | 4 | 3.2 | 2.8 |
�� | 1 | T2 | 1 | 2 | 1.2 | 3.0 |
��1��T1 _________T2 ������>������<������=����
��2���ﵽƽ������¶Ⱥ�������䣬����������ٳ���0.8molH2O��3.2molH2�����ʱV��________V��������>������<������=����
��3�����ܱպ��ݵ������У��ܱ�ʾ������Ӧ�ﵽ��ѧƽ��״̬����_______________.
A��V����CO2��=2V����H2��
B���������ܶȱ��ֲ���
C��c��H2O����c��CO2����c��H2��=2��1��2
D����������ƽ����Է����������ֲ���
��4��ijͬѧΪ���о���Ӧ�����Ի�ѧƽ���Ӱ�죬����淴Ӧ������ʱ��Ĺ�ϵ��ͼ��ʾ��

�ɼ���t1��t3��t5��t7ʱ��Ӧ�����˵�ƽ��״̬�����t2��t4��t6��t8ʱ��ֻ�ı���һ����Ӧ��������t6ʱ�̸ı��������_______________,���t1��t8�ĸ�ʱ���H2O ��g����ƽ��ת�������_________��������t1��t2,�Դ�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ��谢���ӵ���������ֵΪNA���� ��
A. �ڱ�״���£�22.4Lˮ����������ĿΪNA
B. 1mol��L-1K2SO4��Һ����K+��ĿΪ2NA
C. 1 mol����������Ӧ����Na2O��Na2O2ʱ��ʧ������Ŀ��ΪNA
D. O2��Ħ�����ԼΪ22.4 L��mol-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ij�¶��£���������ʼ�����Ϊ1L���ܱ������а��±���ʾͶ�ϣ�������Ӧ��2SO2(g)+O2(g) ![]() 2SO3(g)��H��0���ﵽƽ���������˵����ȷ����
2SO3(g)��H��0���ﵽƽ���������˵����ȷ����
������� | �������� | ��ʼ���ʵ���/mol | ƽ��ʱSO3�� ���ʵ���/mol | ||
SO2 | O2 | SO3 | |||
�� | ���º��� | 2 | 1 | 0 | 1.2 |
�� | ���Ⱥ��� | 0 | 0 | 2 | a |
�� | ���º�ѹ | 2 | 1 | 0 | b |
A. ƽ��ʱSO3�����ʵ�����a��1.2��b��1.2
B. ��������ƽ�ⳣ����ͬ
C. ����I��SO2��ת��������������SO3��ת����֮��С��1
D. ����ʼʱ���������г���1.0molSO2(g)��0.40molO2(g)��1.40molSO3(g)�����ʱV����V��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����OH��������ͬ�������͵�����������
A. F2 B. Cl�� C. NH3 D. NH2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶Ⱥ�ѹǿ�£�1���X2������3���Y2���廯������2������廯���������廯����Ļ�ѧʽΪ�� ��
A.X2Y3
B.XY3
C.XY
D.X3Y
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����±�ΪԪ�����ڱ���һ���֣�����X��Y��Z��WΪ������Ԫ�أ�WԪ�صĺ˵����ΪXԪ�ص�2��������˵����ȷ���ǣ� ��
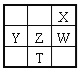
A. X��W��ZԪ�ص�ԭ�Ӱ뾶�����ǵ���̬�⻯������ȶ��Ծ����ε���
B. Y��Z��WԪ������Ȼ���о�����������̬���ڣ����ǵ�����������ˮ������������ε���
C. ����Ԫ�������ɣ������Ʋ�TԪ�صĵ��ʾ��а뵼�����ԣ�T2X3���������Ժͻ�ԭ��
D. YX2�����ۻ���Һ̬WX3��������˷����Ӽ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�л���A. B֮�����ת����ϵ��A(C6H12O2) +H2O![]() B+HCOOH������ƽ�������ϸ÷�Ӧ�������л���B�У����������칹��
B+HCOOH������ƽ�������ϸ÷�Ӧ�������л���B�У����������칹��
A. 6�� B. 7�� C. 8�� D. 9��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com