
【题目】【加试题】(10分)碳、硫和氮元素及其化合物的处理是资源利用和环境保护的重要研究课题。
(1)CO可转化成二甲醚,原理为:2CO(g) + 4H2(g)![]() CH3OCH3(g) + H2O(g),已知一定条件下,该反应中CO的平衡转化率随温度、投料比[n(H2)/n(CO)]的变化曲线如图1
CH3OCH3(g) + H2O(g),已知一定条件下,该反应中CO的平衡转化率随温度、投料比[n(H2)/n(CO)]的变化曲线如图1
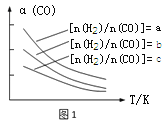
若温度升高,则反应的平衡常数K将 (填“增大”、“减小”或“不变”)。
(2)SO2的水溶液呈酸性,某温度下,0.02 molL﹣1亚硫酸水溶液的pH等于2,若忽略亚硫酸的二级电离和H2O的电离,则该温度下亚硫酸的一级电离常数Ka1= 。
(3)已知:反应1:2SO2(g) + O2(g) 2SO3(g) △H1;
反应2:2NO(g) + O2(g) 2NO2(g) △H2;
反应3:SO2(g) + NO2(g) SO3(g) + NO(g) △H3;
若△H1<△H2<0,则反应3属于 (填“放热”或“吸热”)反应。
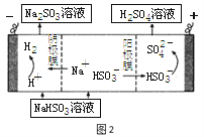
(4)若用少量NaOH溶液吸收SO2气体,对产物NaHSO3进一步电解可制得硫酸,电解原理示意图如图2。电解时阳极的电极反应式为 。
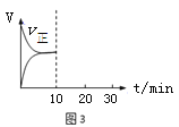
(5)在恒温密闭容器中通入SO2和NO2各1mol发生反应3:SO2(g) + NO2(g) SO3(g) + NO(g),当反应达到平衡后,维持温度和容积不变,10min时再通入各1mol的SO2和NO2的混合气体,20min时再次平衡。两次平衡时NO2的转化率α1 α2(填“>”、“<”、“=”);请在图3画出正反应速率v正在10至30min间随时间变化的曲线图。
【答案】(1)减小(1分) (2)0.01(2分)
(3)放热(1分) (4)HSO3﹣+H2O﹣2e﹣=SO42﹣+3H+(2分)
(5)=(2分) 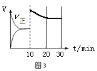 (2分)
(2分)
【解析】
试题分析:(1)根据图1可以看出,对于反应2CO(g) + 4H2(g)![]() CH3OCH3(g) + H2O(g),在相同投料比[n(H2)/n(CO)]时,温度升高,CO的平衡转化率降低,说明平衡逆向移动,即升高温度,平衡左移,平衡常数减小。
CH3OCH3(g) + H2O(g),在相同投料比[n(H2)/n(CO)]时,温度升高,CO的平衡转化率降低,说明平衡逆向移动,即升高温度,平衡左移,平衡常数减小。
(2)由于0.02molL-1亚硫酸水溶液的pH等于2,即溶液中的氢离子浓度为0.01mol/L,而c(HSO3-)=c(H+),列三段式:H2SO3 HSO3- + H+
初始浓度mol/L 0.02 0 0
转化浓度mol/L 0.01 0.01 0.01
平衡浓度mol/L 0.01 0.01 0.01
电离平衡常数Ka1=0.01mol/L×0.01mol/L÷0.01mol/L=0.01。
(3)已知反应1:2SO2(g) + O2(g) 2SO3(g) △H1;;反应2NO(g) + O2(g) 2NO2(g) △H2,根据盖斯定律,将①/2-②/2可得目标反应:SO2(g)+NO2(g)SO3(g)+NO(g),则△H3=(△H1-△H2)÷2,由于△H1<△H2<0,△H3=(△H1-△H2)÷2<0,此反应放热。
(4)电解池中阳极和电源正极相连,失去电子,发生氧化反应,电解NaHSO3溶液可制得硫酸,硫的化合价升高,所以阳极是HSO3-失去电子被氧化生成SO42-,阳极电极反应式是HSO3﹣+H2O﹣2e﹣=SO42﹣+3H+。
(5)在恒温密闭容器中通入SO2和NO2各1mol发生反应3:SO2(g) + NO2(g) SO3(g) + NO(g) △H3,当反应达到平衡后,维持温度和容积不变,10min时再通入各1mol的SO2和NO2的混合气体,而由于SO2(g)+NO2(g)SO3(g)+NO(g)是气体的物质的量不变的反应,平衡不移动,则两次平衡时NO2的转化率α1=α2;由于10min时再通入各1mol的SO2和NO2,反应物的浓度立即增大,则正反应速率v正立即增大,后逐渐减小,最后20min达到平衡,正反应速率v正在10至30min间随时间变化的曲线图为 。
。


科目:高中化学 来源: 题型:
【题目】工农业及城市生活污水中含磷。家用洗涤剂是污水中磷的一个重要来源(洗涤剂中含有磷酸钠),处理污水时要不要除去磷,下列说法中正确的是 ( )
A.磷是生物的营养元素,不必除去
B.含磷的污水是很好的肥料,不必除去
C.含磷的污水排到自然水中,引起藻类增殖,使水变质,必须除去
D.磷对人无毒,除去与否都无关紧要
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知维生素有20多种,它们多数在人体内不能合成,需要从食物中摄取。人体缺乏下列哪种维生素会引起夜盲症( )
A.维生素A B.维生素B1 C.维生素C D.维生素D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 焓变是一个与反应能否自发进行有关的因素,多数能自发进行的反应是放热反应
B. 在同一条件下不同物质有不同的熵值,其体系的混乱程度越大,熵值越大
C. 一个反应能否自发进行取决于该反应是放热还是吸热
D. 一个反应能否自发进行,与焓变和熵变的共同影响有关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现代以石油化工为基础的三大合成材料是
①合成氨②塑料 ③医药 ④合成橡胶 ⑤合成尿素 ⑥合成纤维⑦合成洗涤剂
A. ②④⑦ B. ②④⑥ C. ①③⑤ D. ④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在100mLHNO3和H2SO4混合溶液中,两种酸物质的量浓度之和0.6mol/L,向该溶液中加入足量铜粉,加热,待充分反应后,所得溶液中Cu2+ 的 物质的量浓度(mol/L)最大值为
A.0.225 B.0.30 C.0.36 D.0.45
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关食品添加剂的说法中错误的是( )
A.食品添加剂可改善食品的色、香、味 B.食品添加剂可补充食品的营养成分
C.食品添加剂可延长食品的储存时间 D.食品添加剂都是有益于人体健康的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】55g铁铝混合物与足量的盐酸反应生成标准状况下的氢气44. 8L,则混合物中铁和铝的物质的量之比为
A. 1:1 B. 1:2 C. 1:3 D. 2:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列叙述正确的是( )
A.常温常压下,46 g NO2与N2O4的混合气体中含有的分子总数为NA
B.0.1 mol乙烯和乙醇的混合物完全燃烧所消耗O2的分子数为0.3NA
C.25 ℃时,pH=13的Ba(OH)2溶液中含有OH-的数目为0.1NA
D.一定量的钠与8 g氧气作用,若两者均无剩余,转移的电子数为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com