
【题目】芳香烃X,相对分子质量为92。以X为原料合成E路线如下(部分产物和反应条件已略去)。
![]()
回答下列问题:
(1)X的结构简式为__________________;C所含的官能团是______________(写名称)。
(2)A→B的反应条件为___________________;D→E的反应类型为_____________________。
(3)C→D转化中①的化学方程式为_________________________________________________。
(4)E在NaOH溶液中水解的化学方程式为__________________________________________。
(5)下列关于B的说法正确的是___________。
a.核磁共振氢谱有5个峰 b.能发生消去反应和氧化反应
c.能与钠反应放出氢气 d.能和NaOH溶液反应
(6)E有多种同分异构体,同时符合下列条件的同分异构体共有________种。其中不含甲基的有机物的结构简式为____________________。
①与NaHCO3溶液作用有气体放出 ②芳香族化合物
【答案】 ![]() 醛基 NaOH水溶液、加热 酯化反应(取代反应) C6H5-CHO + 2Ag(NH3)2OH
醛基 NaOH水溶液、加热 酯化反应(取代反应) C6H5-CHO + 2Ag(NH3)2OH![]() H2O+2Ag↓+3NH3+ C6H5-COONH4
H2O+2Ag↓+3NH3+ C6H5-COONH4 ![]() +NaOH →
+NaOH →![]() + C2H5OH ac 14
+ C2H5OH ac 14 ![]()
【解析】相对分子质量为92的某芳香烃X,令分子组成为CxHy,则92/12=7…8,由烷烃中C原子与H原子关系可知,该烃中C原子数目不能小于7,故该芳香烃X的分子式为C7H8,其结构简式为![]() ,X与氯气发生取代反应生成A,A转化生成B,B催化氧化得C,C能与银氨溶液反应,酸化后生成D,故B含有醇羟基、C含有醛基,则A为
,X与氯气发生取代反应生成A,A转化生成B,B催化氧化得C,C能与银氨溶液反应,酸化后生成D,故B含有醇羟基、C含有醛基,则A为![]() ,B为
,B为![]() ,C为
,C为![]() ,D为
,D为![]() ,苯甲酸与乙醇发生酯化反应生成E为
,苯甲酸与乙醇发生酯化反应生成E为![]() ;
;
(1)X的结构简式为![]() ;C
;C![]() 所含的官能团是醛基(写名称)。(2)A为
所含的官能团是醛基(写名称)。(2)A为![]() ,B为
,B为![]() ,A→B的反应条件为NaOH水溶液、加热;D为
,A→B的反应条件为NaOH水溶液、加热;D为![]() ,苯甲酸与乙醇发生酯化反应生成E为
,苯甲酸与乙醇发生酯化反应生成E为![]() ,D→E的反应类型为酯化反应(取代反应)。(3)C→D转化中①的化学方程式为C6H5-CHO + 2Ag(NH3)2OH
,D→E的反应类型为酯化反应(取代反应)。(3)C→D转化中①的化学方程式为C6H5-CHO + 2Ag(NH3)2OH![]() H2O+2Ag↓+3NH3+ C6H5-COONH4 。(4)E在NaOH溶液中水解的化学方程式为
H2O+2Ag↓+3NH3+ C6H5-COONH4 。(4)E在NaOH溶液中水解的化学方程式为![]() +NaOH →
+NaOH →![]() + C2H5OH 。(5)a.B
+ C2H5OH 。(5)a.B![]() 中含有5种氢原子,则核磁共振氢谱有5个峰,故正确;b.含有苯环,能和氢气发生还原反应,因为连接醇羟基碳原子相邻碳原子上不含氢原子,则不能发生消去反应,故错误;c.含有醇羟基,则能与钠反应放出氢气,故正确;d.不含酚羟基或羧基,所以没有酸性,不能和NaOH溶液反应,故错误;故选ac;(4)E
中含有5种氢原子,则核磁共振氢谱有5个峰,故正确;b.含有苯环,能和氢气发生还原反应,因为连接醇羟基碳原子相邻碳原子上不含氢原子,则不能发生消去反应,故错误;c.含有醇羟基,则能与钠反应放出氢气,故正确;d.不含酚羟基或羧基,所以没有酸性,不能和NaOH溶液反应,故错误;故选ac;(4)E![]() 的同分异构体同时符合下列条件:
的同分异构体同时符合下列条件:
①遇NaHCO3溶液有气体放出,说明含羧基,②芳香族化合物,说明含有苯环,分为以下几种情况:含有一个取代基为-CH2CH2COOH或者-CH(CH3)COOH,含有2个取代基为-CH3、-CH2COOH,或者-CH2CH3、-COOH,各有邻、间、对3种,含有3个取代基为2个-CH3、-COOH,2个-CH3处于邻位,-COOH有2种位置,2个-CH3处于间位,-COOH有3种位置,2个-CH3处于对位,-COOH有1种位置,共有14种。其中不含甲基的有机物的结构简式为![]() 。
。


科目:高中化学 来源: 题型:
【题目】Ⅰ.铂(Pt)单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示:

(1)由图可知,金属晶体铂的堆积方式为_________,一个晶胞中含有___个铂原子,距离每个铂原子最近且等距离的铂原子有_______个。
Ⅱ.铂元素的一种化合物:PtCl2(NH3)2可以形成两种固体,一种为淡黄色,在水中的溶解度较小,另一种为黄绿色,在水中的溶解度较大,请回答下列问题:
(2)PtCl2(NH3)2立体结构是______________;
(3)黄绿色固体物质是由___________组成(填“极性分子”或“非极性分子”);
(4)两种固体在水中的溶解性差异,可以用____________原理来解释;
Ⅲ.碳铂是1,1-环丁二羧酸二氨合铂(Ⅱ)的简称,是第二代铂族抗癌药物,碳铂的结构为:
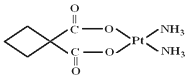
(5)化学键种类很多,如:①极性共价键、②非极性共价键、③配位键、④离子键、⑤金属键、⑥σ键、⑦π键,碳铂中含有的作用力有____(填字母);
A.①②③⑥⑦ B.①②④⑥ C.①③⑤⑦ D.④⑤
(6)在碳铂分子中,C原子的杂化方式有_____ 种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠(NaNO2)外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂,但使用过量会使人中毒。某学习小组针对亚硝酸钠设计了如下实验:
【实验Ⅰ】制取NaNO2
该小组先查阅资料知:①2NO+Na2O2 →2NaNO2;2NO2+Na2O2 →2NaNO3;②NO能被酸性高锰酸钾氧化为NO3-,然后设计制取装置如下图(夹持装置略去):
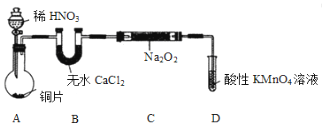
(1)装置A中用于盛放稀HNO3溶液的仪器名称为________;写出装置A中发生主要反应的离子方程式:__________。
(2)装置D的作用是____________;
(3)如果没有B装置,C中发生的副反应的化学方程式①_______ 、②______。
(4)甲同学检查完装置气密性良好后进行实验,发现制得的NaNO2中混有较多的NaNO3杂质。下列哪种方案可以提高NaNO2纯度________。
A.将B中的药品换为碱石灰 B.将稀硝酸换为浓硝酸
C.实验开始前通一段时间CO2 D.在A、B之间增加盛有水的洗气瓶
【实验Ⅱ】测定NaNO2样品中NaNO3的含量
步骤:(1)配置KMnO4标准溶液并酸化,酸化KMnO4的酸应选择________(填化学式)
(2)已知在酸性溶液中,NO2-可将MnO4-还原为Mn2+。为测定亚硝酸钠的含量,称取4.000 g样品溶于水配成250 mL溶液,取25.00 mL溶液于锥形瓶中,用0.1000 mol·L-1酸性KMnO4溶液进行滴定,消耗KMnO4 20.00mL,酸性KMnO4的作用是______和_______,计算所得固体中亚硝酸钠的质量分数__________。(结果保留一位小数)
【扩展实验Ⅲ】该学习小组为再了解氧族元素的一些典型化合物的性质,进行了如下实验探究。
经查知:硫酸铜受热分解生成氧化铜和气体,受热温度不同,该气体成分也不同。气体成分 可能是SO2、SO3和O2中的一种、两种或三种。他们通过设计一探究性实验,测定反应产生的SO2、SO3和O2的物质的量,并经计算确定各物质的化学计量数,从而确定CuSO4分解的化学方程式。实验用到的仪器如图所示:
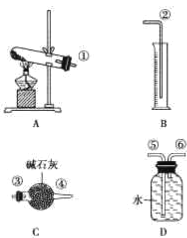
(1)提出猜想
①所得气体的成分可能只含________一种;
②所得气体的成分可能含有________两种;
③所得气体的成分可能含有SO2、SO3和O2三种。
(2)实验探究
实验操作过程(略)。已知实验结束时,硫酸铜完全分解。
请回答下列问题:
①请你组装探究实验的装置,按从左至右的方向,则仪器接口的连接顺序为______ (填序号)。
②由于加热时的温度不同,实验结束后测得相关数据也不同。数据如下:
实验 | 称取CuSO4的质量/g | 仪器C 增加的质量/g | 量筒中水的体积折算成标准状况下气体的体积/mL |
第一组 | 6.4 | 2.88 | 224 |
第二组 | 6.4 | 2.56 | 448 |
请通过计算,推断出第一组和第二组的实验条件下CuSO4分解反应的化学方程式:
第一组_________________; 第二组_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学校化学学习小组为探究二氧化氮的性质,按下图所示装置进行实验。

(1)装置甲中盛放浓硝酸的仪器A的名称是______,该装置中发生反应的化学方程式为________________________。
(2) 装置丙中的试管内发生反应的离子方程式为:_______________________。
(3)为了探究NO的还原性,可以在装置丁的导气管C中通入一种气体,通入的这种气体的名称是________。
(4)取下装置丙中的试管D,在其中滴加FeSO4溶液,溶液变为________色,为了证明铁元素在该反应中的产物,可以再在溶液中滴加KSCN溶液,溶液变为________色。
(5)硝酸厂常用催化还原方法处理尾气。CH4在催化条件下可以将NO2还原为N2。
已知:CH4(g)+2O2(g)===CO2(g)+2H2O(g)ΔH=-889.6 kJ·mol-1①
N2(g)+2O2(g)===2NO2(g)ΔH=+67.7 kJ·mol-1②
则CH4还原NO2生成水蒸气和氮气的热化学方程式是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,集气瓶内充满某混合气体,置于光亮处,将滴管内的水挤入集气瓶后,烧杯中的水会进入集气瓶,集气瓶内气体是( )

①CO、O2 ②Cl2、CH4 ③NO2、O2 ④N2、H2
A. ①② B. ②④ C. ③④ D. ②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在指定的溶液中,能大量共存的是( )
A. c(H+)=0.1 mol·L-1的溶液:Na+、NH、SO![]() 、S2O
、S2O![]()
B. 与铝粉反应放出H2的无色溶液:NO、Al3+、Na+、SO![]()
C. 中性溶液:Fe3+、Al3+、NO、SO![]()
D. 常温下c(H+)/c(OH-)=1×10-12的溶液:K+、AlO、CO![]() 、Na+
、Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于化学反应中能量变化的说法错误的是( ) 
A.如图所示的反应为吸热反应
B.化学反应中有物质变化也有能量变化
C.需要加热才有发生的反应一定是吸热反应
D.化学键断裂吸收能量,化学键生成放出能量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com