
【题目】恒温恒容条件下,下列叙述中不是可逆反应2A(g)+3B(g)![]() 2C(g)达到平衡的标志的是
2C(g)达到平衡的标志的是
①C的生成速率与C的分解速率相等②单位时间生成amolA,同时消耗1.5molB;③各组分的浓度不再变化;④混合气体的密度不再变化;⑤混合气体的总压强不再变化;⑥混合气体的物质的量不再变化;⑦混合气体的平均摩尔质量不再变化;⑧A、B、C的分子数目比为2: 3: 2.
A. ⑤⑥⑧ B. ②⑤⑧ C. ①③④ D. ②④⑦
【答案】A
【解析】试题分析:① C的生成速率与C的分解速率相等,则C的浓度不变,反应达到平衡状态,错误;②单位时间生成amol A,同时会产生1.5amol B,还同时消耗1.5amol B,则反应处于平衡状态,错误;③各组分的浓度不再变化,则物质的总物质的量不变,反应处于平衡状态,错误;④由于是恒温恒容,反应前后物质的质量发生改变,若混合气体的密度不再变化,则任何气体的质量不变,气体的物质的量不变,反应处于平衡状态,错误;⑤该反应是反应前后气体体积不变的反应,在任何时刻混合气体的总压强都再变化,因此不能据此判断反应处于平衡状态,正确;⑥该反应是反应前后气体的物质的量不变的反应,因此在任何时刻混合气体的物质的量都不变,因此不能据此判断反应处于平衡状态,正确;⑦该反应反应前后气体的质量发生变化,而气体的物质的量不变,因此若混合气体的平均摩尔质量不再变化,说明反应处于平衡状态,错误;⑧A、B、C的分子数目比为2:3:2,反应可能处于平衡状态,也可能不处于平衡状态,这与开始加入的物质的量的多少及反应条件有关,错误。因此符合题意的是⑤⑥⑧,选项A正确。


科目:高中化学 来源: 题型:
【题目】现有三种可溶物质A、B、C,其中A、B是盐,一种是酸式盐,一种是正盐,C是碱,它们溶于水后电离产生的所用离子如下表所示:
阳离子 |
|
阴离子 |
|
请根据下列叙述回答问题:
(1)C的化学式为_________________。
(2)A溶液与B溶液反应可生成气体X,则X的化学式为_______________,该反应的化学反应方程式为___________________.
(3)A、B溶液与C溶液反应可分别生成白色沉淀D和E,其中D可溶于稀硝酸.
①B的化学式为____________,鉴别溶液中B的阴离子的方法是___________________.
②D溶于稀硝酸的离子方程式为___________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
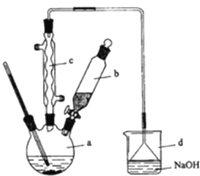
苯 | 溴 | 溴苯 | |
密度/g·cm-3 | 0.88 | 3.10 | 1.50 |
沸点/℃ | 80 | 59 | 156 |
水中溶解度 | 微溶 | 微溶 | 微溶 |
按以下合成步骤回答问题:
(1)在a中加入15mL无水苯和少量铁屑。在b中小心加入4.0mL液态溴.向a中滴入几滴溴,有白雾产生,是因为生成了_________气体,继续滴加至液溴滴完。装置d的作用是_________;
(2)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤.NaOH溶液洗涤的作用是_________;
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤.加入氯化钙的目的是_________;
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为_________,要进一步提纯,下列操作中必须的是____________(填入正确选项前的字母);
A.重结晶 B.过滤 C.蒸馏 D.萃取
(4)在该实验中,a的容积最适合的是_____________(填入正确选项前的字母):
A.25mL B.50mL C.250mL D.500mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化合物含C、H、O、N、S等元素。该化合物在动物体内一定不能( )
A. 抵御病菌和病毒的侵害
B. 做遗传物质
C. 改变化学反应的速度
D. 构成细胞核生物体的结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常用FeCl3溶液制印刷电路板并再生,主要过程如下:
腐蚀Cu:2FeCl3+Cu=CuCl2+2FeC12;
然后回收Cu:Fe+CuCl2=Cu+FeCl2;
再生FeC13:2FeC12+C12=2FeC13。
将某电路板上的Cu腐蚀完全,恰好消耗0.5L2mol/LFeCl3。全过程忽略体积的变化。
回答下列问题:
(1)画出Cl原子结构示意图:________________;
(2)将Cu腐蚀一半时,溶液中的金属阳离子有:_______________;此时c(Cl-)为:____________mol/L;
(3)腐蚀的Cu的总物质的量为:______________mol;
(4)再生FeC13时,溶液由___________色最终变为___________色;消耗的Cl2在标准状况下的体积至少为:________________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某铜矿主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物。实验室以此铜矿石为原料制备CuSO4·5H2O及CaCO3,部分步骤如下:

请回答下列问题:
(1)溶液A除含有Cu2+外,还可能含有的金属离子有________(填离子符号);验证所含离子所用的试剂是在__________。
(2)可用生成的CO2制取优质碳酸钙。制备时,先向氯化钙溶液中通入氨气,再通入CO2。
①实验室通常采用加热氯化铵和氢氧化钙混合物的方法制取氨气。某学习小组选取下图所给部分装置制取并收集纯净的氨气。
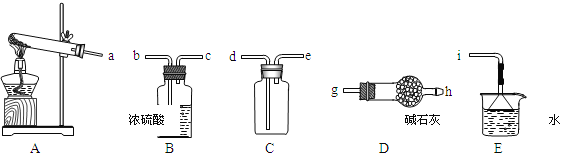
如果按气流方向连接各仪器接口,你认为正确的顺序为
a→_________、_________→_________、_________→i。
其中与i相连漏斗的作用是______________。
②为探究氨气和氯气的反应
a. 装置A、B,B装置内的药品依次是____________、____________。
b.装置C可用于探究氯气与氨气(已知氯气和氨气可发生反应:3Cl2+2NH3=N2+6HCl)的反应。实验打开开关1、3,关闭2,先向烧瓶中通入____________,然后关闭1、3,打开2,向烧瓶中缓缓通入一定量的另一种气体。实验一段时间后向烧瓶内出现浓厚的白烟并在容器内壁凝结。
(3)测定铜矿石中Cu2(OH)2CO3质量百分含量的方法是:
a.将1.25g铜矿石制取的CuSO4·5H2O于锥形瓶中,加入适量水完全溶解;
b.向溶液中加入100mL0.25mol/L的氢氧化钠溶液使Cu2+完全沉淀;
c.过滤;
d.滤液中的氢氧化钠溶液用0.5mol/L盐酸滴定至终点,耗用10mL盐酸。则铜矿石中Cu2(OH)2CO3质量分数为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2SO2(g)+O2(g)![]() 2SO3(g),反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ/mol。请回答下列问题:
2SO3(g),反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ/mol。请回答下列问题:

(1)E的大小对该反应的反应热________影响?(填“有或无”)。该反应通常用V2O5作催化剂,加V2O5会使图中B点______(填“升高或降低”);
(2)图中ΔH=__________kJ/mol;
(3)如果反应速率υ(SO2)为0.05 mol/(L·min),则υ(O2)=___________mol/(L·min);
(4)1 mol SO2(g)氧化为1 mol SO3(g)的反应热ΔH1___________1 mol SO2(g)氧化为1 mol SO3(l)的反应热ΔH2。(填“>、<或=”)
(5)已知单质硫的燃烧热为296 kJ/mol,计算由S(s)生成3 mol SO3(g)的ΔH=____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组数据中,前者刚好是后者两倍的是
A.2 mol水的摩尔质量和1 mol水的摩尔质量
B.200 mL 1 mol/L氯化钙溶液中c(Cl-)和100 mL 2 mol/L氯化钾溶液中c(Cl-)
C.64 g二氧化硫中氧原子数和标准状况下22.4 L一氧化碳中氧原子数
D.20%NaOH溶液中NaOH的物质的量浓度和10%NaOH溶液中NaOH的物质的量浓度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com