
【题目】为探究某固体化合物X(仅含两种元素)的组成和性质,设计并完成如下实验。已知无色气体B能形成酸雨。请回答:
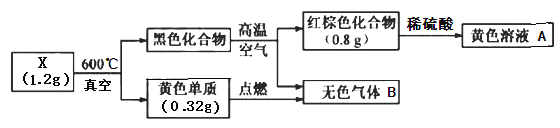
(1)X的化学式是________。
(2)设计实验方案检验黄色溶液中的金属阳离子___________________。
(3)将无色气体B通入黄色溶液A中,发现溶液变成浅绿色。请用离子方程式表示该反应_________
【答案】FeS2 取少量黄色溶液,滴加KSCN溶液,若变血红色,说明存在Fe3+ 2Fe3+ +SO2 + 2H2O=2Fe2+ +SO42- + 4H+
【解析】
X在真空中加热后生成黄色单质,该黄色单质在氧气中燃烧生成能形成酸雨的无色气体,则单质为S,无色气体为SO2;黑色固体在与氧气在高温条件下生成二氧化硫气体和红棕色化合物,该化合物溶于酸显黄色,可知该红棕色化合物为氧化铁,黄色溶液为硫酸铁溶液,褐色化合物黑色化合物由铁元素和硫元素组成,黑色化合物的质量=1.2g-0.32g=0.88g,红棕色化合物中铁的质量=0.8g×![]() =0.56g,则硫元素的质量=0.88g-0.56g=0.32g,所以铁原子和硫原子的个数比=
=0.56g,则硫元素的质量=0.88g-0.56g=0.32g,所以铁原子和硫原子的个数比=![]() ,所以黑色化合物的化学式为FeS,X中还有0.32g硫元素,所以X的化学式为FeS2。
,所以黑色化合物的化学式为FeS,X中还有0.32g硫元素,所以X的化学式为FeS2。
(1)X的化学式是FeS2;
(2)黄色溶液中的金属阳离子是三价铁离子,故检验方法是取少量黄色溶液,滴加KSCN溶液,若变血红色,说明存在Fe3+;
(3)将无色气体B通入黄色溶液A中,发现溶液变成浅绿色的离子方程式为2Fe3++SO2+ 2H2O=2Fe2++SO42-+4H+。


科目:高中化学 来源: 题型:
【题目】已知A、B、D是食品中的常见有机物,A是生物的主要供能物质。以A和水煤气(CO、H2)为原料在一定条件下可获得有机物B、C、D、E、F,其相互转化关系如图。已知E是CO和H2以物质的量之比1:2反应的产物,F为具有特殊香味、不易溶于水的油状液体。
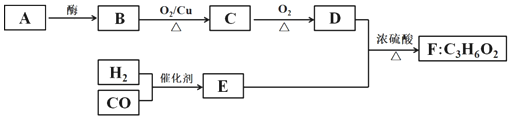
请回答:
(1)有机物A的分子式______,有机物D中含有的官能团名称是______。
(2)B→C的反应类型是______,C的结构简式为______。
(3)B→C化学方程式是______。D+E→F的化学方程式______。
(4)下列说法不正确的是______。
A.有机物B与金属钠反应比水与金属钠反应要剧烈
B.除去F中含有D、E杂质可用NaOH溶液洗涤、分液
C.D和E反应生成F时,浓硫酸主要起强氧化剂作用
D.C在一定条件下可以与H2反应转化为B
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于金属冶炼的叙述中,不正确的是( )
A.电解铝时,以氧化铝—冰晶石熔融液为电解质,也常加入少量CaF2帮助降低熔点
B.电解铝时阴极碳块需定期更换
C.可利用铝热反应从V2O5中冶炼金属V
D.可用加热法从HgO中冶炼Hg
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的CO2气体通入2L未知浓度的NaOH溶液中,在所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的气体与HCl的物质的量的关系如图所示(忽略气体的溶解和HCl的挥发)下列说法正确是( )
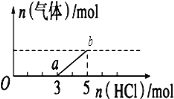
A.oa段反应的离子方程式为:H++OH-=H2O
B.O点溶液中所含溶质的化学式为NaHCO3、Na2CO3
C.标准状况下,通入CO2的体积为4.48L
D.原NaOH溶液的物质的量浓度为2.5molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X是合成一种新型抗肝炎药的中间体,其生产路线如下:
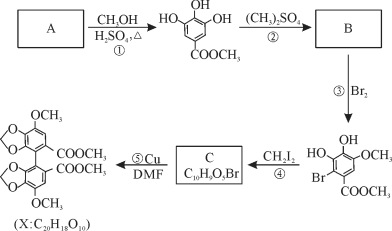
回答下列问题:
(1)反应①的反应类型为_____________。
(2)反应③的化学方程式为____________________________________________________。
(3)反应④生成C的结构简式为______________________,无机产物为_____(填化学式)。
(4)A有多种同分异构体,同时符合下列条件的有______种(不考虑立体异构)。请写出其中一种核磁共振氢谱有4组峰,且峰面积之比为2∶2∶1∶1的结构简式___________。
a.苯环上有4个取代基;
b.与FeCl3溶液发生显色反应;
c.能发生水解反应。
(5)参照上述合成路线及信息,以氯气、苯和一氯乙烯为原料(其它试剂任选),设计制备聚苯乙烯的合成路线____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关。下列说法错误的是
A. PM2.5是指粒径不大于2.5μm的可吸入悬浮颗粒物
B. 绿色化学要求从源头上消除或减少生产活动对环境的污染
C. 燃煤中加入CaO可以减少酸雨的形成及温室气体的排放
D. 天然气和液化石油气是我国目前推广使用的清洁燃料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将8.00gCuO和Fe2O3的混合物分成两等份,其中一份在高温下用足量CO还原后,剩余固体质量为2.88g;另一份固体用200mL某浓度的盐酸恰好溶解,则:
(1)混合物中CuO和Fe2O3的物质的量之比为:________________________
(2)所用盐酸的物质的量浓度为_________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个1L的密闭容器中加2molA和1molB发生反应: 2A(g)+B(g)![]() 3C(g)+D(s),达到平衡时C的浓度为1.2mol/L , C的体积分数为a% 。维持容器的体积和温度不变,按下列配比作为起始物质,达到平衡后,C的浓度仍是1.2mol/L,C的体积分数仍为a% 的是
3C(g)+D(s),达到平衡时C的浓度为1.2mol/L , C的体积分数为a% 。维持容器的体积和温度不变,按下列配比作为起始物质,达到平衡后,C的浓度仍是1.2mol/L,C的体积分数仍为a% 的是
A. 6mol C+2mol D B. 4mol A+2mol B
C. 1mol A+0.5mol B+1.5mol C D. 3mol C+5mol D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢化锂(LiH)在干燥的空气中能稳定存在,遇水或酸剧烈反应,能够引起燃烧。某化学科研小组准备使用下列装置制备LiH固体。下列说法正确的是
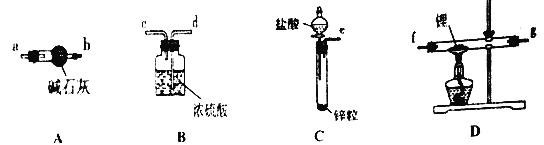
A. 上述仪器装置按气流从左到右连接顺序为:e接d,c接f,g接a,b(和g调换也可以)
B. 实验中所用的金属锂保存在煤油中
C. 在加热D处的石英管之前,应先通入一段时间氢气,排尽装置内的空气
D. 干燥管中的碱石灰可以用无水CaCl2代替
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com