
【题目】已知原子序数为a的元素M位于第6周期第ⅡA族,元素N为同周期的第ⅢA族,则N的原子序数为 .
 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案科目:高中化学 来源: 题型:
【题目】工业上乙醚可用于制造无烟火药。实验室合成乙醚的原理如下。
主反应 2CH3CH2OH![]() CH3CH2OCH2CH3+H2O
CH3CH2OCH2CH3+H2O
副反应CH3CH2OH![]() H2C=CH2↑+H2O
H2C=CH2↑+H2O

【乙醚制备】装置设计如下图(部分装置略)
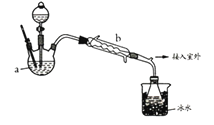
(1)仪器a是__________(写名称);仪器b应更换为下列的_______(填序号)。
A.干燥器 B.直形冷凝管 C.玻璃管 D.安全瓶
(2)实验操作的正确排序为___________(填序号),取出乙醚立即密闭保存。
a.安装实验仪器 b.加入12mL浓硫酸和少量乙醇的混合物c.检查装置气密性
d.熄灭酒精灯 e.通冷却水并加热烧瓶 f.拆除装置 g.控制滴加乙醇速率与馏出液速率相等 (3)加热后发现a中没有添加碎瓷片,处理方法是___________________;反应温度不超过145℃,其目的是___________________________。若滴入乙醇的速率显著超过馏出液速率,反应速率会降低,可能原因是__________________________。
【乙醚提纯】
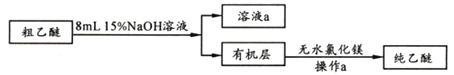
(4)粗乙醚中含有的主要杂质为_____________;无水氯化镁的作用是_____________________。
(5)操作a的名称是____;进行该操作时,必须用水浴代替酒精灯加热,其目的与制备实验中将尾接管支管通入室外相同,均为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组表述中,正确的是( )
A. 基态核外电子的排布为![]() 的原子3p能级有一个空轨道
的原子3p能级有一个空轨道
B. 第四周期中,未成对电子数最多的原子为Mn
C. Fe2+的基态核外电子排布为1s22s22p63s23p63d6
D. 2p能级有2个未成对电子的基态原子的价电子排布一定为2s22p2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某纯碱样品中含有氯化钠杂质,用下图装置测定试样中纯碱的纯度。主要实验步骤如下:
①按图组装仪器并检查装置的气密性
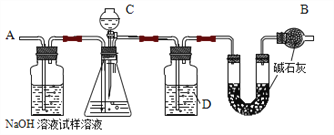
②将 a g 样品放入锥形瓶,加适量水溶解。
③称量装有碱石灰的 U 形管的质量为 b g
④从C 滴下溶液到锥形瓶中无气泡产生
⑤从A 处缓缓鼓入一定量空气后,最终称得U 形管的质量为 c g
(1)B 仪器的名称是_____,其作用为_____。
(2)C 中装的溶液是_____(填字母,下同)D 中装的溶液是_____。
a.稀硫酸 b.浓硫酸 c.氢氧化钠溶液 d.浓盐酸
(3)步骤⑤的目的是_____。
(4)写出纯碱的纯度的计算式_____(用字母表示)。
(5)若实验中发现装置 C 的活塞没塞紧,存在漏气情况,则所测得的结果会_____(填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知![]() (X)、
(X)、![]() (Y)、
(Y)、![]() (Z)的分子式均为C8H8,下列说法正确的是
(Z)的分子式均为C8H8,下列说法正确的是
A. X的同分异构体只有Y和Z
B. Y、Z的二氯代物均只有三种
C. X、Y、Z中只有X的所有原子可能处于同一平面
D. X、Y、Z均可使溴水、酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关叙述正确的是
①水的摩尔质量是18g
②0.5molH2的体积为11.2L
③1 mol 水中含有 2 mol 氢和 1mol 氧
④1mol 任何物质都约含有6.02×1023个分子
⑤0.5mol H2SO4含有的原子数目为3.5NA
⑥只有在标准状况下,体积相同的任何气体所含的分子数相同
⑦质量分数为40%的硫酸溶液与等体积的水混合,所得溶液浓度大于20%
⑧物质的量浓度为4mol/L 的硫酸溶液与等质量的水混合,所得溶液浓度小于2mol/L
A. ①③④⑤⑦⑧ B. ②⑤⑦⑧ C. ⑤⑦⑧ D. ⑤⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)写出下列反应的离子方程式。
①钠和水反应____________________________________。
②硫酸铜溶液中滴加氢氧化钡溶液___________________________________。
(2)3.01×1023个OH-的物质的量为______mol,质量为_______g。
(3)将28g纯净的铁粉投入到200ml足量的稀盐酸中,该反应能够放出标准状况下的气体____L,实验后所得溶液中Fe2+的物质的量浓度为_________mol/L 。
(4)将200 mL 0.5 mol/LNaOH稀释成1000 mL后其物质的量浓度是_________mol/L 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白花丹酸具有镇咳祛痰的作用,其合成路线流程图如下:
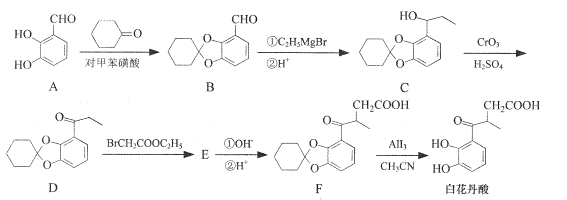
(1)A中的含氧官能团名称为__和_____。
(2)C-D的反应类型为 ___。
(3)白花丹酸分子中混有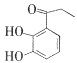 ,写出同时满足下列条件的该有机物的一种同分异构体的结构简式:____。
,写出同时满足下列条件的该有机物的一种同分异构体的结构简式:____。
①分子中有四种不同化学环境的氢;②与FeCl3溶液能发生显色反应,且1 mol该物质最多能与3 mol NaOH反应.
(4)E的结构简式为 ___。
(5)已知:![]() 根据已有知识并结合相关信息写出以
根据已有知识并结合相关信息写出以![]() 和CH3CH2OH为原料制备
和CH3CH2OH为原料制备![]() 的合成路线流程图(合成路线流程图示例见本题题干)____。
的合成路线流程图(合成路线流程图示例见本题题干)____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com